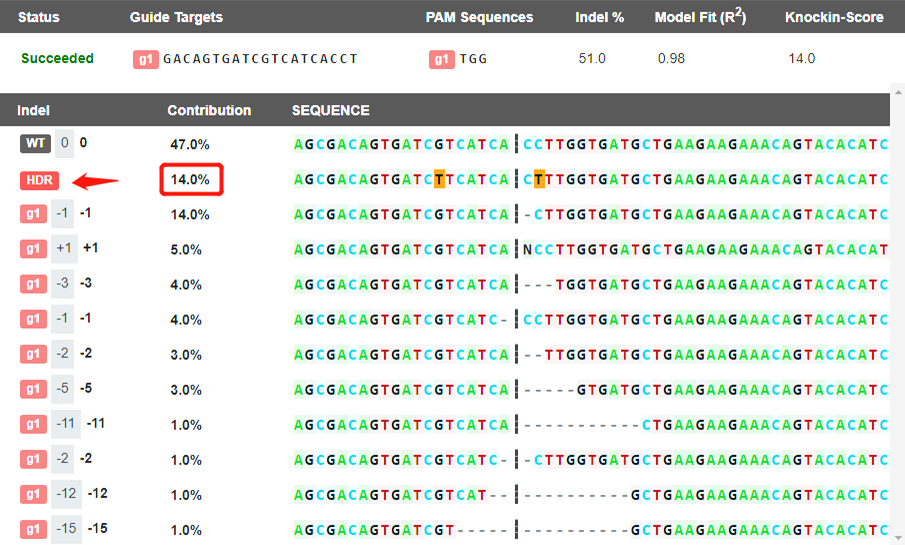
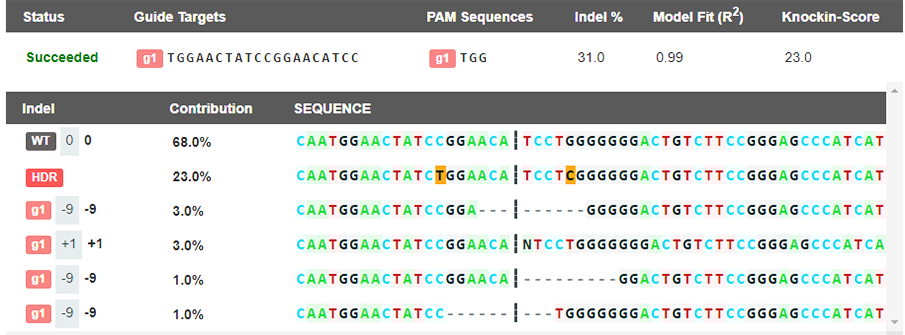
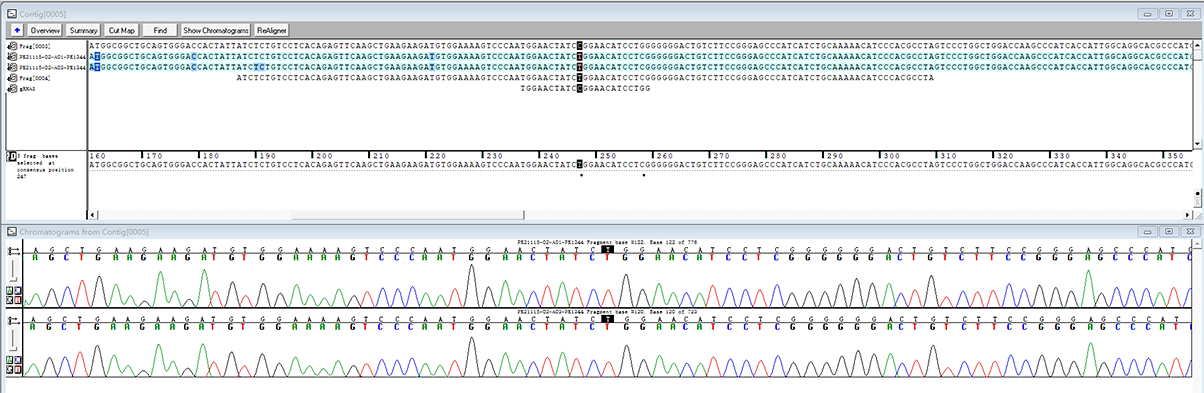
产品(gDNA)
| 突变基因 | 突变碱基 | 突变氨基酸 | 基因型 |
|---|---|---|---|
| BRAF | c.1799T>A | p.V600E | 纯合 |
| EGFR | c.2235_2249del15 | p.E746-A750del(1) | 杂合 |
| c.2369C> T | p.T790M | 杂合 | |
| c.2155G>A | p.G719S | 杂合 | |
| c.2303G>T | p.S768I | 纯合 | |
| c.2236_2250del15 | p.E746-A750del(2) | 杂合 | |
| c.2573T>G | p.L858R | 杂合 | |
| KRAS | c.34G>A | p.G12S | 纯合 |
| c.35G>C | p.G12A | 纯合 | |
| c.38G>A | p.G13D | 杂合 | |
| c.35G>A | p.G12D | 纯合 | |
| c.35G>T | p.G12V | 纯合 | |
| C.182A>T | p.Q61L | 杂合 | |
| c.183A>T | p.Q61H | 纯合 | |
| NRAS | c.35G>A | p.G12D | 杂合 |
| c.181C>A | p.Q61K | 杂合 | |
| c.34G>T | p.G12C | 杂合 | |
| c.34G>A | p.G12S | 杂合 | |
| C.183A>T | p.Q61H | 杂合 | |
| C.182A>T | p.Q61L | 杂合 | |
| PIK3CA | c.1633G>A | p.E545K | 杂合 |
| c.3140A>G | p.H1047R | 杂合 | |
| c.1624G>A | p.E542K | 杂合 |
服务(定制细胞系)
针对罕见肿瘤突变位点或者其他适应症,源井生物自主研发的CRISPR-U™技术可在细胞系中高效引入目的突变。
CRISPR-U™是源井生物自主研发的基因编辑技术,CRISPR-U™技术比普通CRISPR/Cas9技术的基因切割效率更高,同时可以大幅度提升同源重组效率,轻松实现细胞和动物水平的基因敲除(KO)、基因点突变(PM)和基因敲入(KI)。利用CRISPR-U™的技术优势,源井已成功在超过200种细胞系上实现基因编辑。超200种细胞、5000例基因的编辑经验保障实验方案与载体质量;成熟转染体系与转染专用培养基显著提高转染率;单克隆生长培养基显著提高了至少30%单克隆形成率,以及单克隆鉴定试剂盒实现早期单克隆(96孔板阶段)的批量化鉴定等,源井从实验各环节入手全面优化了实验体系,保证基因编辑细胞实验成功率的有效提升,轻松交付阳性克隆!
高频位点清单
| 基因名称 | 突变位点 |
|---|