支气管上皮细胞BEAS-2B与CRISPR/Cas9基因编辑的美妙联动!


使用CRISPR/Cas9构建GENE-33敲除BEAS-2B细胞以研究GENE-33对六价铬致癌性的影响
使用CRISPR/Cas9构建STING敲除BEAS-2B细胞以验证STING在人鼻病毒复制过程的作用
构建DNMT3B敲除支气管上皮BASE-2B细胞发现DNMT3B能抑制铜绿假单胞菌感染期间的肺部免疫反应
支气管上皮细胞BEAS-2B与CRISPR/Cas9基因编辑的美妙联动!

BEAS-2B细胞系是一种广泛使用的永生化但非致瘤性人类细胞系,由Curtis C. Harris小组于1988年从非癌个体获得的正常人支气管上皮细胞建立。该细胞系是通过转染腺病毒12-SV40杂交病毒建立,随后通过连续传代实现细胞永生化。目前,BEAS-2B已被广泛用于研究与肺癌发生有关的细胞和分子机制,如上皮-间质转化 (EMT)在肺癌发生中的作用,以及肺炎球菌感染机制。 此外,BEAS-2B细胞系已被用作体外细胞模型,用于分析或筛选具有潜在肺毒性或肺致癌性的各种化学和生物制剂[1]。


图1.BEAS-2B细胞形态(图片来源于ECACC)
作为永生化细胞,BEAS-2B增殖传代能力强,加上细胞转染效率高,核型也比较简单(基本符合2n=46,图2),因此较容易进行基因编辑,常与CRISPR/Cas9基因编辑技术联用,通过细胞基因敲除、细胞点突变或细胞敲入进一步研究基因功能和疾病发生机制。接下来小源给大家分享一些在BEAS-2B上进行CRISPR/Cas9基因编辑的案例,帮忙大家快速了解BEAS-2B细胞基因编辑相关应用。
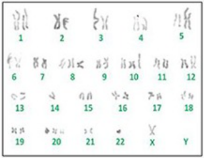
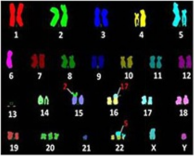
图2.BEAS-2B细胞核型代表[2]
1.在BEAS-2B细胞中敲除GENE-33基因研究GENE-33对六价铬致癌性的影响
GENE-33(Mig6,ERRFI1)是一种具有多种细胞功能的衔接蛋白,此前报道了这种蛋白质的消耗会促进六价铬 [Cr(VI)] 诱导的肺上皮细胞转化。然而,介导这一过程的早期分子事件尚不清楚。Park等人使用单细胞 RNA 测序来比较长期暴露于亚致死剂量 Cr(VI) 且有或没有 CRISPR/cas9 介导的GENE-33 缺失的 BEAS-2B 肺上皮细胞之间的基因表达谱差别。数据揭示了83个差异表达基因,最显着的变化是与细胞粘附、氧化应激、蛋白质泛素化、上皮-间质转化/转移和 WNT 信号相关的基因。一些神经特异性基因的上调也很明显,特别是泛素羧基末端水解酶 L1 (UC HL1)。GENE-33 缺失和/或 Cr(VI) 暴露不会导致细胞形态发生明显变化。然而,无论 Cr(VI) 暴露与否,GENE-33 缺失都会导致细胞周期 G2/M 期细胞适度但显著减,且GENE-33 缺失会引起细胞增殖显著下降。有趣的是,Cr(VI) 暴露消除了两种基因型之间细胞增殖的差异。不仅如此,GENE-33缺失能显著提高细胞的迁移能力。数据表明,GENE-33 缺失和慢性 Cr(VI) 暴露相结合会产生类似于转化肺上皮细胞的基因表达模式和表型[3]。
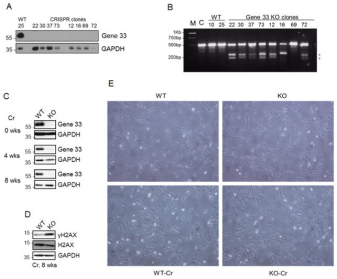
图3.CRISPR/cas9介导的BEAS-2B细胞Gene-33基因敲除
2.验证STING在人鼻病毒复制过程的作用
人鼻病毒(Human rhinovirus, HRV)是引起普通感冒最重要的病原体,该病毒引起的疾病为自限性疾病,一般1周左右自愈。HRV属于小RNA病毒科,感染细胞后会重塑细胞内外膜成分,形成专门促进病毒复制的细胞器,这种细胞器被称为复制器(Replication organelles, ROs),其他单股正链RNA病毒也具有此特点。STING是HRV感染重要的宿主因子,然而STING在HRV复制周期中发挥的功能尚不清楚。为了验证STING对HRV复制的重要性,作者利用CRISPR/Cas9技术在BEAS-2B细胞和气液界面培养的原代人气道上皮细胞(ALI)中实现STING的敲除。结果发现,敲除STING会显著抑制HRV的复制,而对呼吸道合胞病毒和流感病毒无显著影响,这说明HRV的复制依赖STING[4]。
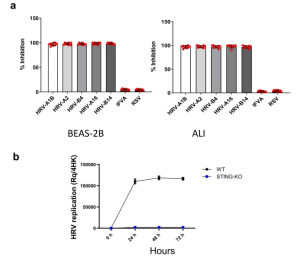
图4.HRV复制需要STING
3.支气管上皮DNMT3B抑制铜绿假单胞菌感染期间的肺部免疫反应
铜绿假单胞菌是一种革兰氏阴性有鞭毛细菌,属于肺炎的常见致病性病原体。呼吸道上皮细胞通过产生物理屏障和释放抗菌肽以及趋化介质来提供抵御呼吸道病原体的第一道防线。DNA 甲基化的程度会影响基因转录和染色质结构,且在细菌感染期间会有所变化。DNA甲基转移酶(DNMT3B)是一种介导DNA从头甲基化的酶,为验证了DNMT3B与气道上皮细胞感染铜绿假单胞菌后产生的免疫反应有关。研究人员使用 CRISPR/Cas9生成了DNMT3B敲除的BEAS-2B支气管上皮细胞和对照 BEAS-2B 细胞(非靶向guide RNA)。两个确认的 DNMT3B敲除克隆和两个对照 BEAS-2B克隆暴露于热灭活的 PAK中12小时之后,收获 mRNA 和上清液。PAK诱导CXCL1、CXCL8和CCL20的mRNA和蛋白质水平显著上调,这一上调情况在DNMT3B 敲掉的细胞中更为明显,表明支气管上皮 DNMT3B参与趋化因子的调节,会通过抑制粘膜对鞭毛蛋白的反应来帮助铜绿假单胞菌破坏宿主防御能力。
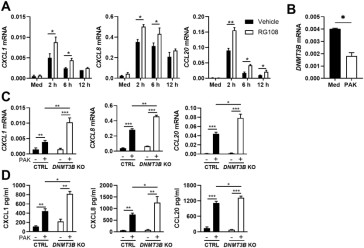
图5.BEAS-2B支气管上皮细胞中的DNMT3B缺失促进体外铜绿假单胞菌诱导的趋化因子产生
基因编辑和细胞模型的建立对于推进功能基因组学、信号通路、新陈代谢、细胞死亡、药物发现、药物反应和癌症研究等领域具有重要的意义。BEAS-2B细胞作为研究药物代谢活化作用和呼吸系统肿瘤以及分子机制的理想细胞模型,已经有许多研究人员利用CRISPR/Cas9技术对其进行编辑以研究癌症特征、耐药机制的披露、癌症治疗、细胞死亡研究、功能基因组学、信号通路、药物发现、药物反应和细胞治疗等多种具有重要意义的课题。
源井生物研发的CRISPR-U™(基于CRISPR/Cas9技术)在DNA双链的切割上比一般的CRISPR/Cas9系统更有效率,不仅可以显著提高同源重组的效率,还能同时在体内外实现高效的基因编辑,对于BEAS-2B细胞的基因编辑实验有着极大的优势。现已推出多种BEAS-2B基因敲除细胞现货,优质纯合1周速递低至¥8000。
[1] Han X, Na T, Wu T, et al. Human lung epithelial BEAS-2B cells exhibit characteristics of mesenchymal stem cells[J]. PLoS One, 2020, 15(1): e0227174.
[2] Zhang P, Li Z, Wang N, Duan G, Wang W, Feng Y, Zhao Y, Wang L, Zhu H, Zhang Q, Liu X, Wu W, Wu Y, Yao W, Wang J, Wu Y, Feng F. Coal tar pitch extract could induce chromosomal instability of human bronchial epithelial cells mediated by spindle checkpoint-related proteins. Oncotarget. 2017 Apr 11;8(34):56506-56517. doi: 10.18632/oncotarget.17025. PMID: 28915607; PMCID: PMC5593578.
[3] Park S, Zhang X, Li C, et al. Single-cell RNA sequencing reveals an altered gene expression pattern as a result of CRISPR/cas9-mediated deletion of Gene 33/Mig6 and chronic exposure to hexavalent chromium in human lung epithelial cells[J]. Toxicology and applied pharmacology, 2017, 330: 30-39.
[4] Triantafilou M, Ramanjulu J, Booty L M, et al. Human rhinovirus promotes STING trafficking to replication organelles to promote viral replication[J]. Nature communications, 2022, 13(1): 1-16.
[5] Qin W, Brands X, Van’t Veer C, et al. Bronchial epithelial DNA methyltransferase 3b dampens pulmonary immune responses during Pseudomonas aeruginosa infection[J]. PLoS pathogens, 2021, 17(4): e1009491.










