文献解读:呼肠孤病毒(reovirus)感染机制的突破性发现——PirB受体


文献解读:呼肠孤病毒(reovirus)感染机制的突破性发现——PirB受体
摘要
2023年,美国匹兹堡大学研究发现,成对免疫球蛋白样受体B(PirB)是呼肠孤病毒(reovirus)感染的关键受体。文章描述,通过文库大规模筛选,结合高通量测序、流式细胞分析仪、原子力显微镜等技术,证明了PirB的细胞外D3D4区域是reovirus附着和感染性所必需,同时在小鼠体内也证明了这一点。这些发现拓展了人们对reovirus的理解,为针对病毒进入途径的治疗策略开辟了新途径。这一发现还凸显了PirB在介导免疫反应中的广泛作用,为免疫疗法的开发提供了理论依据。
研究背景
reovirus是一种具有广泛宿主范围的病原体,能够感染大多数哺乳动物,包括人类。reovirus与多种疾病相关,如乳糜泻和小鼠的脑部疾病。reovirus的感染过程涉及多个步骤,包括与宿主细胞表面的附着因子和内化受体的相互作用。这些相互作用决定了病毒的宿主范围、传播途径、细胞和组织嗜性以及疾病的严重程度。尽管已知reovirus的σ1蛋白能够与唾液酸(SA)和连接粘附分子A(JAM-A)相互作用,但这些已知的受体并不能完全解释reovirus的血清型特异性中枢神经系统(CNS)嗜性和疾病。因此,研究者们需要鉴定新的受体来解释reovirus的这些特性。
研究结果
CRISPRa筛选鉴定PirB为候选受体
研究人员在JAM-A⁻/⁻/NgR1⁻/⁻双敲除(DKO)小鼠胚胎成纤维细胞(MEF)中,利用全基因组CRISPRa技术筛选reovirus受体,发现PirB是候选受体之一。PirB是白细胞免疫球蛋白样受体(LILR)家族的成员,在免疫细胞和神经元上表达,作为主要组织相容性复合体I类(MHC-I)蛋白和髓鞘相关抑制因子(MAIs)的受体。
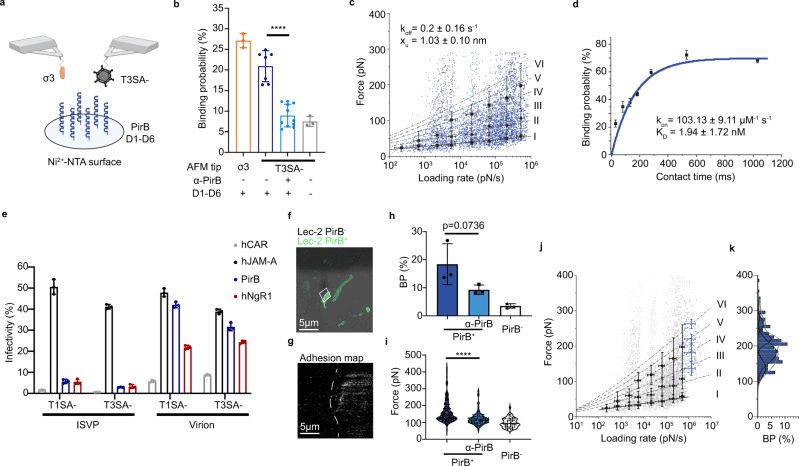
图1 CRISPR激活筛选鉴定出PirB为reovirus的潜在宿主受体
功能验证:PirB介导病毒结合与感染
为了验证PirB作为reovirus受体的功能,研究者在非易感的中国仓鼠卵巢(CHO)细胞中外源表达PirB,并测试了reovirus的结合和感染能力。结果表明,PirB的表达显著增强了reovirus的结合和感染效率。
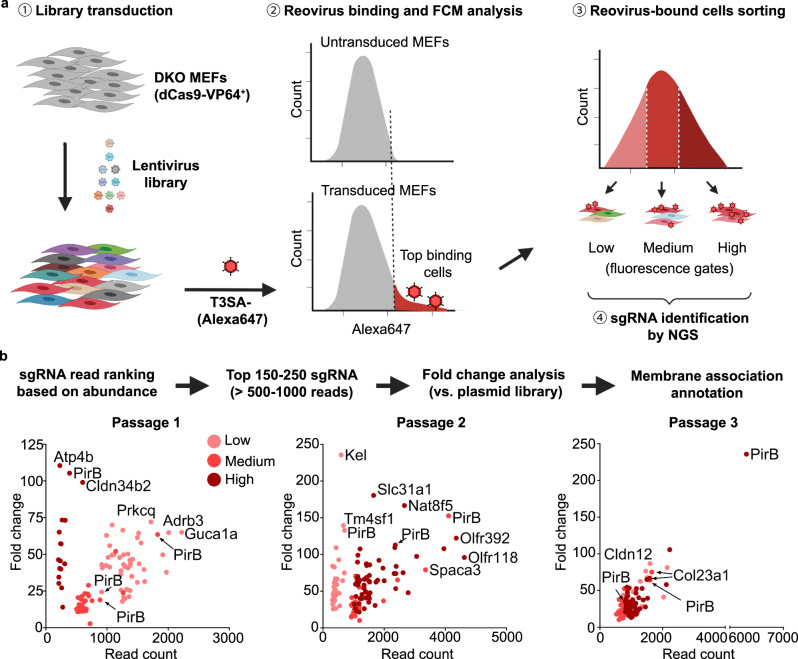
图2 PirB促进reovirus感染和结合
PirB的D3D4结构域是病毒结合关键区域
通过构建PirA和PirB的嵌合受体蛋白,发现交换PirB的D3D4结构域会显著降低reovirus的结合和感染能力,而其他结构域的交换则没有这种影响。这表明PirB的D3D4结构域是reovirus结合和感染的关键区域。
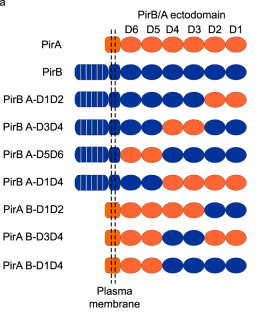
图3 PirB的D3D4结构域是reovirus结合和感染所必需
reovirus与PirB相互作用的高亲和力与特异性
利用原子力显微镜(AFM)技术,研究人员发现reovirus与PirB之间存在高亲和力和特异性的相互作用,解离常数(KD)为1.94 ± 1.72 nM。此外,reovirus的σ3外衣壳蛋白是与PirB相互作用的病毒配体。
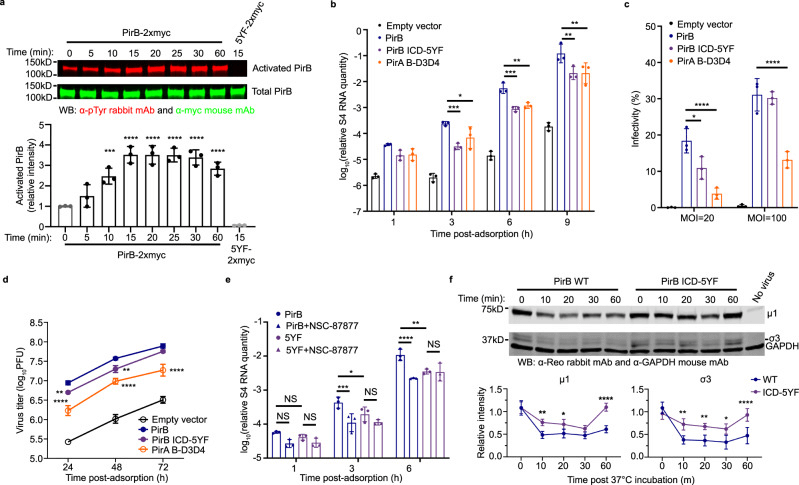
图4 reovirus和PirB互作的生物物理学结果
PirB信号转导促进病毒内化
PirB的细胞内结构域(ICD)含有多个免疫受体酪氨酸基抑制性基序(ITIMs)和一个潜在的免疫受体酪氨酸基转换基序(ITSM)。实验表明,reovirus结合能够激活PirB的信号传导,且PirB的信号传导对于reovirus的进入是必需的。PirB信号传导可能通过SHP-1/2磷酸酶介导,促进reovirus的内化。
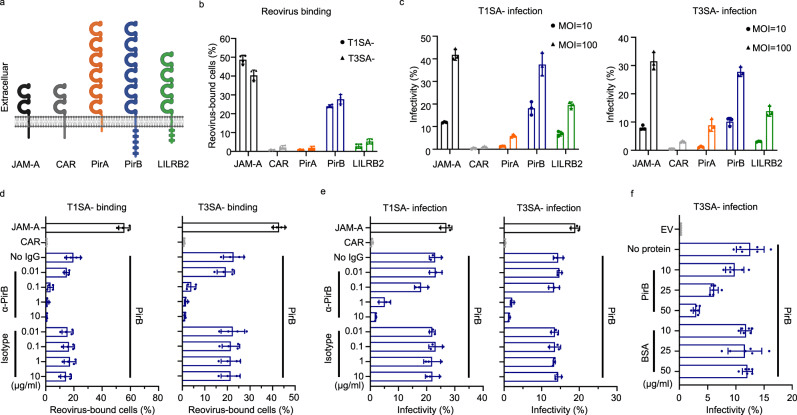
图5 PirB信号传导对于高效的reovirus进入是必需的
PirB在小鼠模型中驱动神经致病性
在PirB基因敲除(PirB−/−)小鼠中,T3 reovirus在大脑中的复制和致病性显著降低,而在野生型(WT)小鼠中则正常。神经特异性PirB敲除(NspPirB−/−)小鼠的实验也显示,PirB在神经细胞中的表达对于T3 reovirus的神经致病性至关重要。此外,PirB特异性抗体能够阻断T3 reovirus对原代皮层神经元的感染,PirB−/−神经元中T3 reovirus的复制也显著降低。
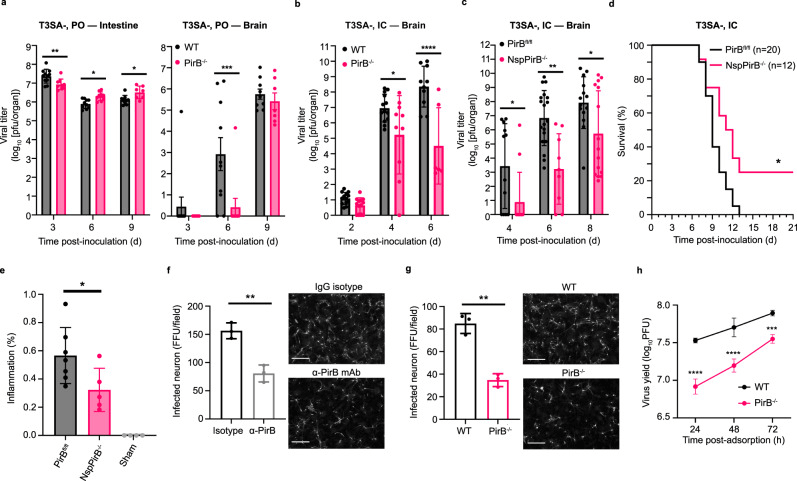
图6 PirB对于T3型reovirus在小鼠中枢神经系统中的高效复制和致病性是必需的
研究结果
本研究通过CRISPRa筛选技术鉴定了PirB作为感染reovirus的受体,并揭示了PirB在reovirus感染和致病性中的关键作用。PirB不仅作为reovirus的结合受体,还通过其细胞内信号传导促进病毒的有效进入。这些发现为理解reovirus的神经致病机制提供了新的视角,并可能为开发针对reovirus感染的治疗策略提供新的靶点。未来的研究可以进一步探索PirB在不同宿主细胞中的功能,以及PirB信号传导在reovirus感染中的具体机制。此外,研究者还可以利用PirB作为靶点,开发新的抗reovirus药物或疫苗,以减轻reovirus感染引起的疾病负担。
Shang, Pengcheng et al. “Paired immunoglobulin-like receptor B is an entry receptor for mammalian orthoreovirus.” Nature communications vol. 14,1 2615. 5 May. 2023, doi:10.1038/s41467-023-38327-6










