结直肠癌宣传月|研究CRC治疗新靶点,CRISPR/Cas9持续立功!


研究CRC治疗新靶点,CRISPR/Cas9持续立功!
结直肠癌 (Colorectal Cancer,CRC) 是一种以基因突变累积和免疫反应失调为主要特征的肠上皮异质性疾病,是第三大最常见的癌症,在全球癌症死亡率中高居第二。据报道,CRC的发病率和死亡率呈现明显的年轻化趋势,尤其在低收入和中等收入国家中居多,这一恶性态势给人类健康带来了严重威胁。因此,研究CRC的发病机制及治疗手段以实现CRC的临床诊断和治疗已经成为广大患者的迫切诉求。
近年来,随着分子生物学和基因工程技术的迅猛发展,人类疾病的神秘面纱正被逐步揭开,当然,CRC也不在例外。其中,以CRISPR/Cas9(一种以gRNA指导工程核酸酶(Cas9)实现对靶向目的基因位点进行快速、轻松及高效的DNA编辑技术)为核心的基因工程技术广受科研人员的青睐,成为挖掘参与CRC调控的关键基因及开发潜在治疗靶点的关键技术。本文精选了近期聚焦于基因敲除细胞、点突变细胞的CRC研究,旨在为广大科研用户开拓更多以基因编辑细胞为工具研究CRC的思路。
案例一:
基于CRISPR/Cas9全基因组敲除筛查确定GRB7是KRAS突变结肠癌对MEK抑制剂产生耐药性的关键基因
靶向KRAS通路是一种兼具前景且富挑战性的结直肠癌治疗方法。尽管MEK抑制剂(MEKi)在BRAF突变的黑色素瘤中显示出疗效,但由于CRC细胞胞内代偿信号转导而产生的药物耐受限制其在CRC临床应用。因此,迫切需要确定与MEKi抗性相关的关键基因并提供联合治疗来克服MEKi耐药性以拓展MEKi的临床应用。
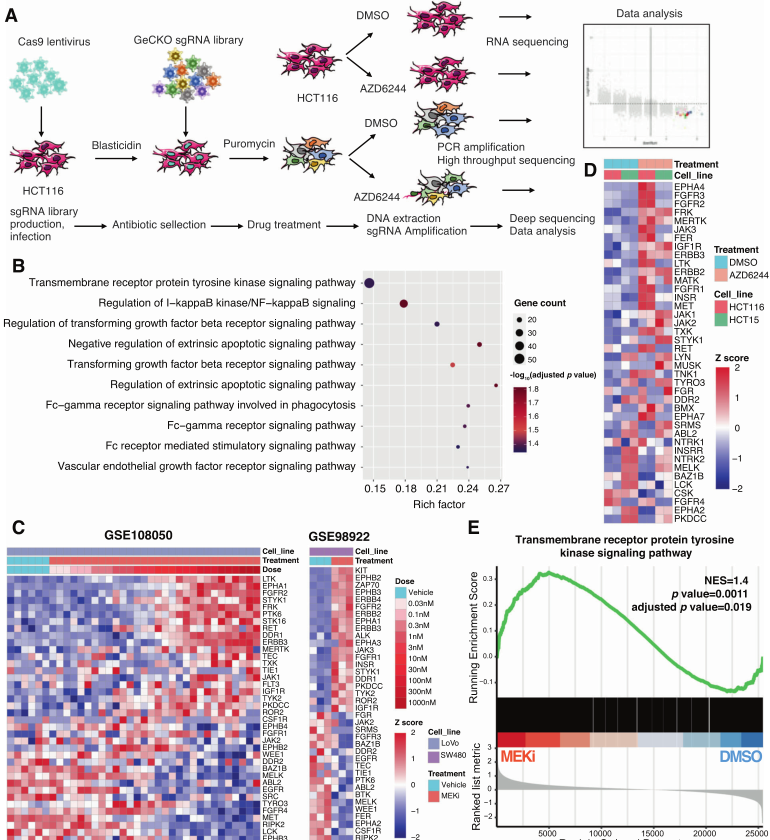
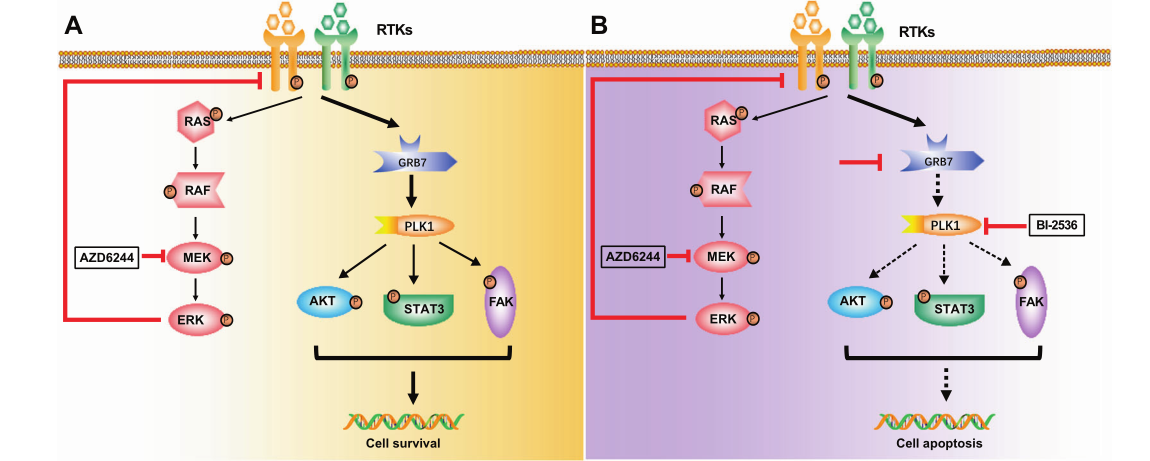
基于此,研究人员设计了一种组合策略,包括全基因组 CRISPR/Cas9敲除文库筛选和 KRAS点突变细胞系(HCT116)的转录组分析。结果显示:几个基因(EGFR、MET、FAK、STAT3及AKT)被确定为与MEKi抗性相关的候选基因,它们在GRB7介导的RTK通路中显著富集。
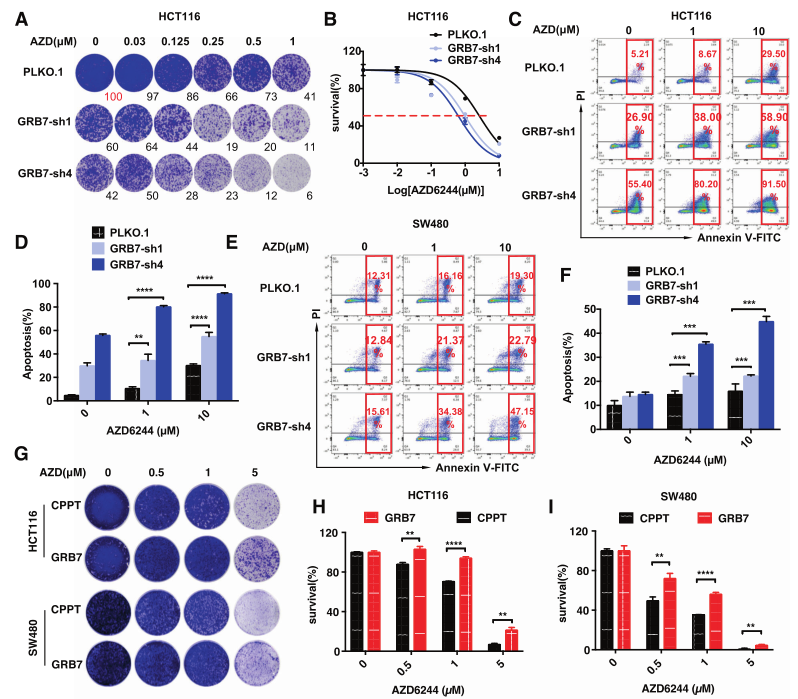
为了验证GRB7在MAPKi抗性方面的关键作用,研究人员评估shRNA敲降GRB7后KRAS突变的CRC细胞在MEKi存在的增殖情况。结果发现:在GRB7敲降后,CRC细胞系(HCT116、SW480、LS174T)在MEKi存在环境中增殖能力显著下降,且细胞凋亡加速。此外,通过过表达GRB7研究在CRC模型细胞系中抗性的获得情况。发现GRB7基因过表达后,CRC细胞克隆形成能力显著提升,且细胞凋亡比例下降。这一系列的结果表明GRB7调控KRAS突变的CRC细胞中MEKi耐药性。
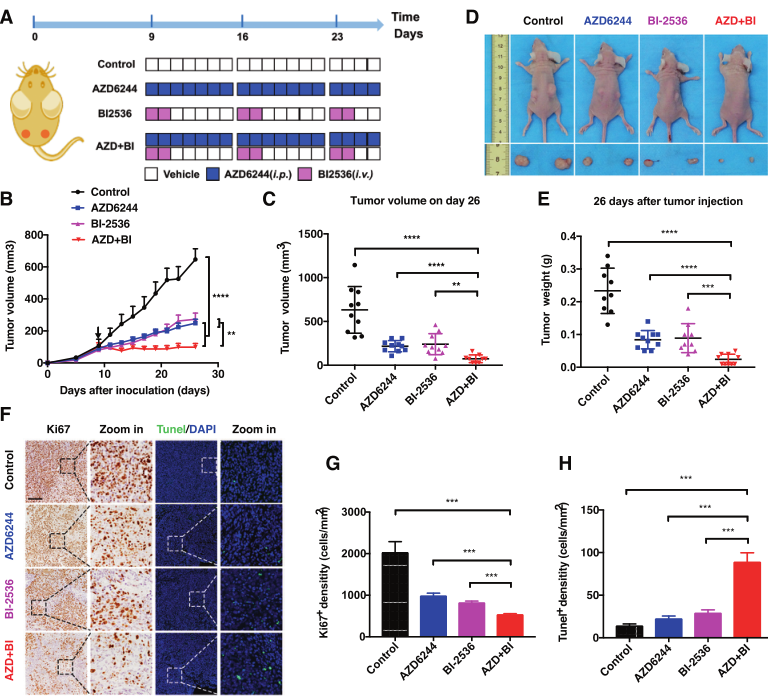
进一步的,研究人员依托免疫共沉淀与质谱联用(IP-MS)技术确定PLK1是GRB7的主要相互作用激酶,并在2D和3D的CRC模型中证实了PLK1和MEK抑制剂的组合在体外和体内协同抑制CRC 细胞增殖并诱导细胞凋亡进程。
综上所述:这项研究将 GRB7-PLK1鉴定为介导RTK的核心轴,导致MEKi药物耐受。因此,PLK1协同MEKi是临床上治疗具有KRAS突变CRC患者的潜在靶点。
案例二:组蛋白甲基转移酶NSD2是结直肠癌重要致癌基因
组蛋白3(H3)甲基化可能导致多种癌基因的转录激活,与CRC疾病的发展及进程密切相关。核受体SET结构域蛋白2(NSD2)是催化组蛋白H3赖氨酸36二甲基化(H3K36ME2)的关键组蛋白甲基转移酶。研究表明,NSD2在几种实体肿瘤中过表达。然而,NSD2在CRC中的表达情况、潜在功能及分子机制未曾报道。
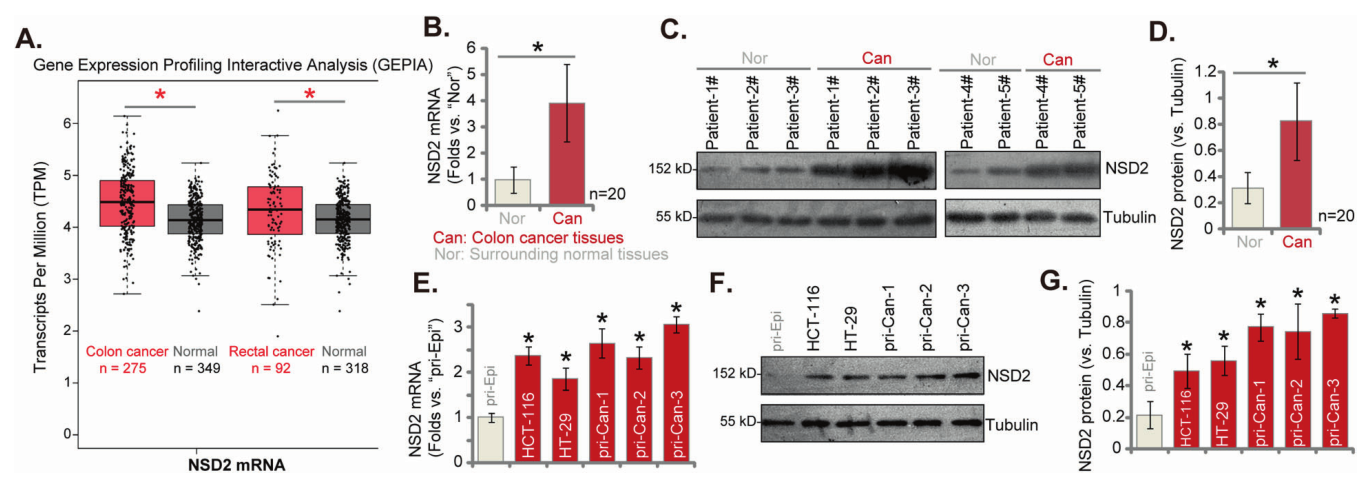
基于此,科研人员展开此项研究。首先,通过基因表达谱交互数据库 (GEPIA)的生物信息学结果表明,NSD2 mRNA表达在结肠癌和直肠癌中升高。此外,局部结肠癌组织中的NSD2 mRNA和蛋白质表达水平显着高于周围正常组织中的mRNA和蛋白质表达水平。
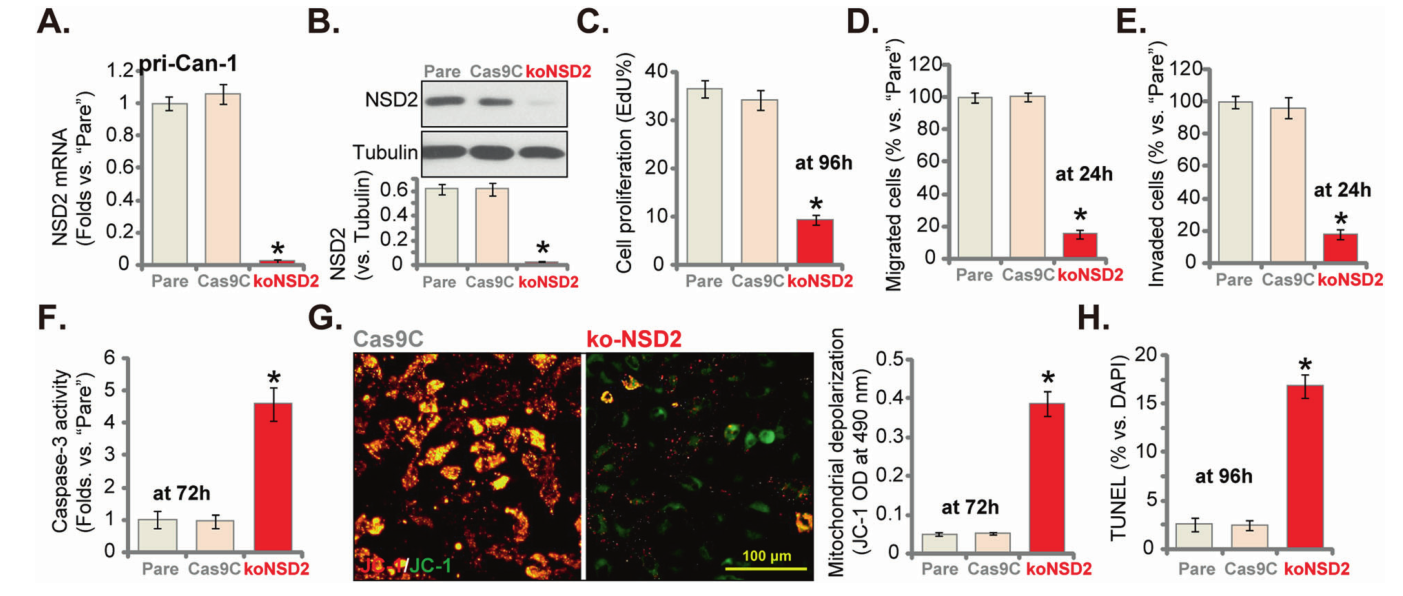
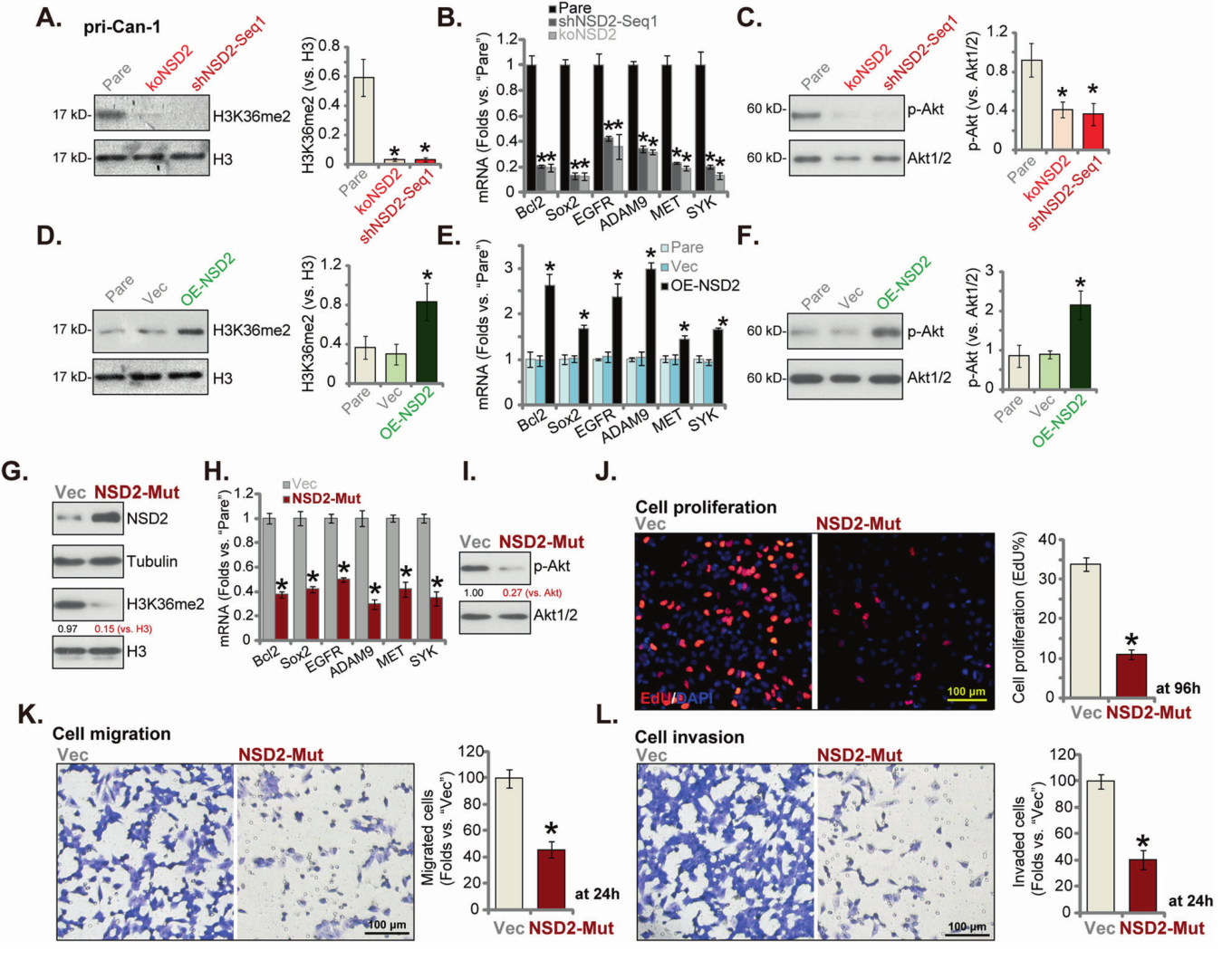
在采用shRNA诱导的沉默或CRISPR/Cas9诱导的NSD2敲除原发性人结肠癌细胞和NSD2敲除CRC细胞系中,细胞增殖、细胞周期进程、迁移及侵袭能力明显得到抑制。
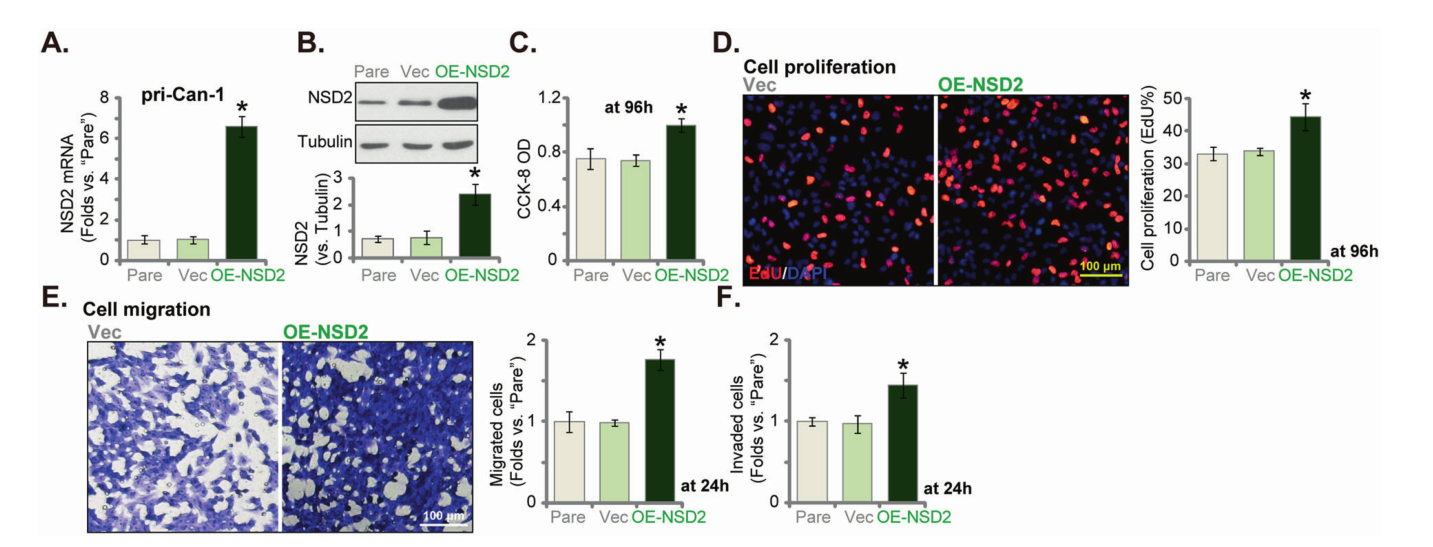
反之,通过慢病毒构建NSD2过表达的原发性人结肠癌细胞株(pri-Can-1),细胞在增殖、侵袭及迁移能力明显上升。
研究人员在进一步的研究中发现,NSD2敲除或沉默的原发性人结肠癌细胞中H3K36me2的水平和NSD2相关致癌基因ADAM9、EGFR、Sox2、Bcl-2、SYK和MET的表达在很大程度上受到抑制。然而,它们的水平随着NSD2过度表达而增加。
最后,体内腹腔注射AAV包装的NSD2 shRNA可在很大程度上抑制了裸鼠中的原发性结肠癌细胞的生长,且定量分析发现H3K36me2的水平和致癌基因的表达明显下降。
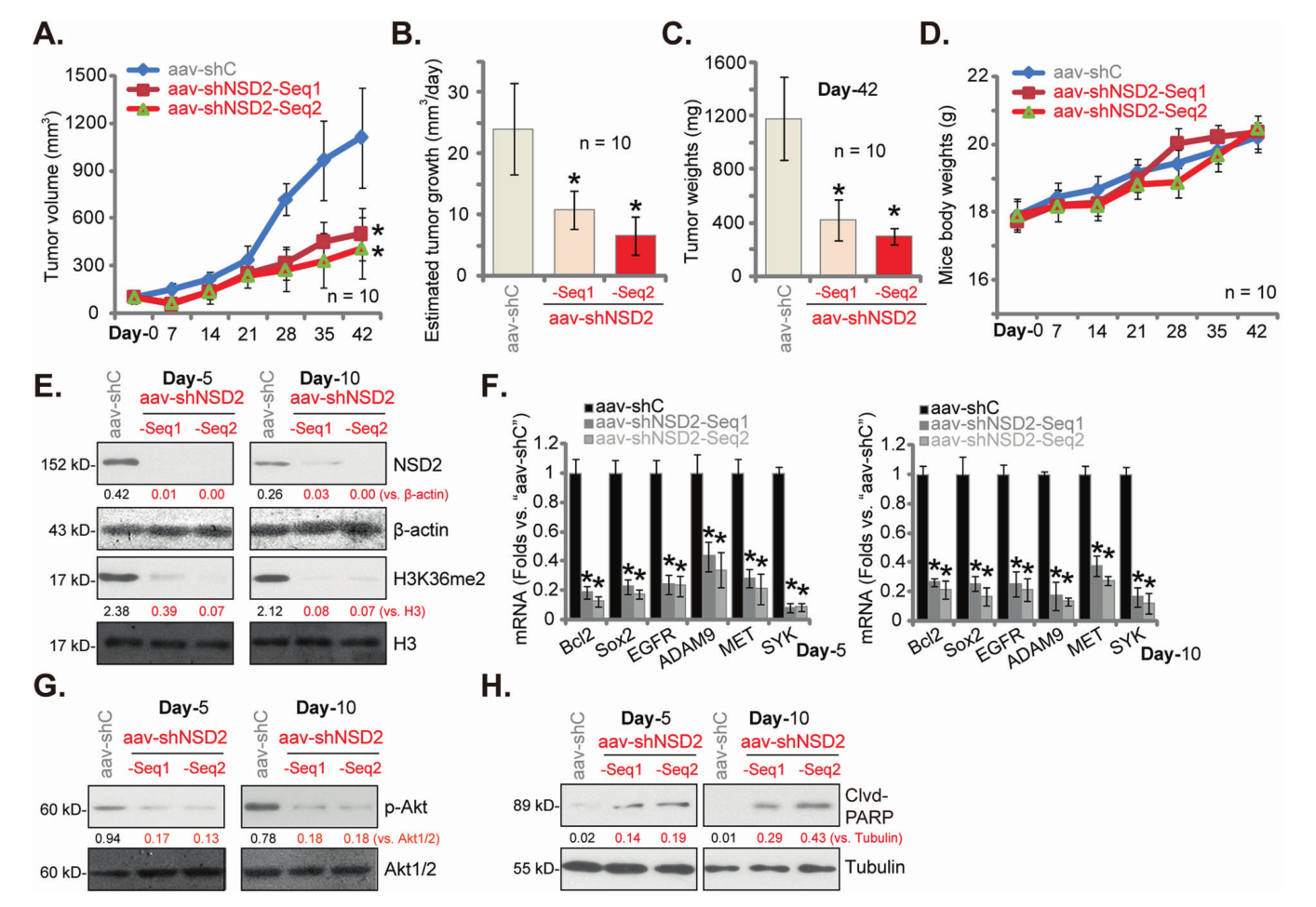
综上所述,NSD2是CRC体外和体内生长所需的一种新的重要致癌基因,靶向NSD2可能是CRC治疗的潜在策略。
没时间自己构建KO细胞株?把实验交给源井吧!低至12800元,KO细胞8周送到家>>
对基因进行沉默或过表达已是研究基因功能的“家常便饭”,源井不仅可为您定制上述基因的干扰/过表达的稳转细胞株和AAV(点击了解开学大促>>),还可提供例如研究中提到的NSD2基因敲除载体等多种载体现货,点击前往搜索心仪的载体现货>>
源井生物是一家专注于细胞基因编辑的企业,可在全球范围内提供优质的基因编辑细胞、稳转细胞株、病毒包装等相关服务,以及近3000种KO细胞现货库,基因敲除试剂盒等基因编辑相关产品,了解更多详情欢迎咨询我们!










