CRISPR文库筛选肿瘤细胞免疫逃逸靶点


CRISPR文库筛选肿瘤细胞免疫逃逸靶点
免疫疗法在癌症治疗中具有重要的临床价值,但肿瘤细胞往往能够通过尚不明确的机制逃避免疫系统的清除,从而限制疗效。为揭示肿瘤免疫逃逸的新型分子机制,研究者以小鼠黑色素瘤细胞 B16 为模型,首先构建了稳定过表达卵清蛋白(OVA)的细胞系,并在此基础上利用 CRISPR 文库技术,针对代谢相关基因开展了系统性筛选。
通过体外和体内联合筛选,研究团队鉴定出Vdac2 基因在肿瘤免疫逃逸中发挥关键作用。结果显示,Vdac2 作为一种免疫信号依赖性的负调控因子,可抑制干扰素-γ(IFN-γ)介导的肿瘤细胞杀伤反应,同时阻碍肿瘤微环境中炎症信号的重编程。进一步研究发现,在肿瘤细胞中敲除 Vdac2 不仅能够显著增强 IFN-γ 诱导的细胞死亡,还可激活cGAS-STING 通路,从而促进抗肿瘤免疫反应的放大。值得注意的是,靶向 Vdac2 明显提升了免疫治疗的疗效,提示其可能作为肿瘤免疫治疗的新型靶点。
综上,本研究通过 CRISPR 文库筛选揭示了 Vdac2 在调控肿瘤免疫逃逸中的核心作用,并为优化现有免疫疗法及开发新型治疗策略提供了重要的理论依据和潜在靶点。
文章亮点(Highlights)
1.建立高特异性免疫应答模型
在肿瘤细胞中稳定过表达 OVA 抗原,并结合 OVA 特异性 CD8⁺ T 细胞(OT-I 细胞),构建了可实现特异性识别与杀伤的免疫应答体系,从而显著增强了 T 细胞介导的抗肿瘤效应。
2.利用不同免疫背景小鼠筛选靶点
将具有完整免疫功能的小鼠与免疫缺陷小鼠相结合,在体内比较筛选结果,能够有效区分免疫依赖性与非免疫依赖性基因靶点,从而精准鉴定与免疫逃逸相关的分子。
3.体内外双重筛选策略。
创新性地结合体外细胞筛选与体内动物模型筛选,提高了CRISPR文库筛选的准确性与生物学相关性,为发现真实有效的免疫调控靶点提供了更强的保障。
一、 CRISPR 文库筛选揭示肿瘤免疫逃逸关键靶点
为系统性鉴定肿瘤细胞介导免疫逃逸的分子机制,研究者采用体内与体外相结合的 CRISPR 文库负向筛选策略,在 B16-OVA 稳定细胞系的基础上进行靶点挖掘。
1. 体内筛选策略
- - 建模:将携带 CRISPR 文库的 B16-OVA 细胞分别接种至T细胞免疫缺陷小鼠(Rag⁻/⁻)与免疫功能完整小鼠(C57BL/6)中。
- - 免疫刺激:在接种后第 7 天,将预先体外激活的OT-I 细胞(可特异识别 OVA 抗原的 CD8⁺ T 细胞)输入 C57BL/6 小鼠,以增强抗肿瘤免疫反应。
- - 数据获取:通过比较 Rag⁻/⁻ 小鼠与 C57BL/6 小鼠肿瘤组织中残存细胞的 sgRNA构成差异,筛选与免疫相关的候选基因。
2. 体外筛选方案
- - 实验分组:将 B16-OVA 文库细胞随机分为两组,其中实验组与激活的 OT-I 细胞共培养,对照组单独培养。
- - 免疫压力:实验组中 OT-I 细胞特异性识别并杀伤 B16-OVA 细胞,从而造成筛选压力。
- - 靶点鉴定:通过比较实验组与对照组存活细胞的 sgRNA丰度差异,识别调控肿瘤细胞对 T 细胞杀伤敏感性的关键基因。
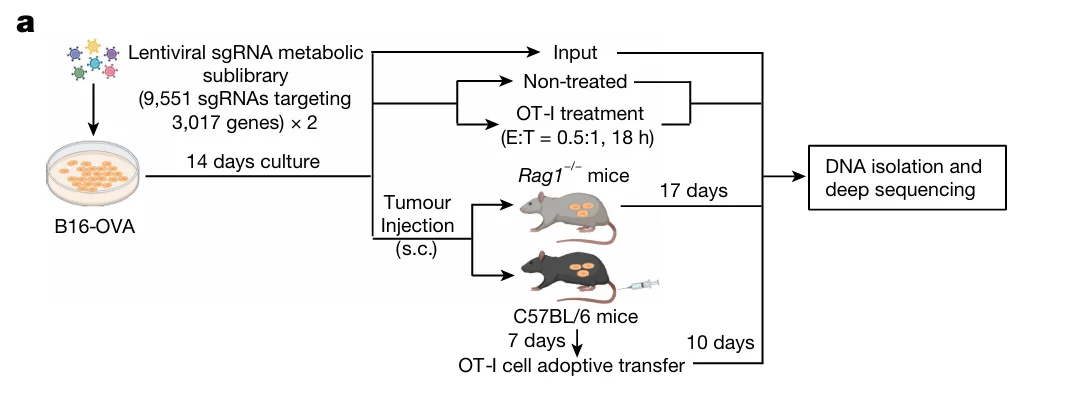
图1 CRISPR文库筛选方案
进一步的比较分析显示,在体内与体外筛选结果中存在显著重叠。具体而言,Vdac2、Pigu、Pigk、Fitm2、Pde4b及Ext1等基因在两种筛选体系的负向富集结果中均被显著检出。这一现象表明,这些基因的缺失能够增强肿瘤细胞对 T 细胞介导杀伤的敏感性,从而提示它们可能作为调控肿瘤免疫逃逸的重要分子靶点。
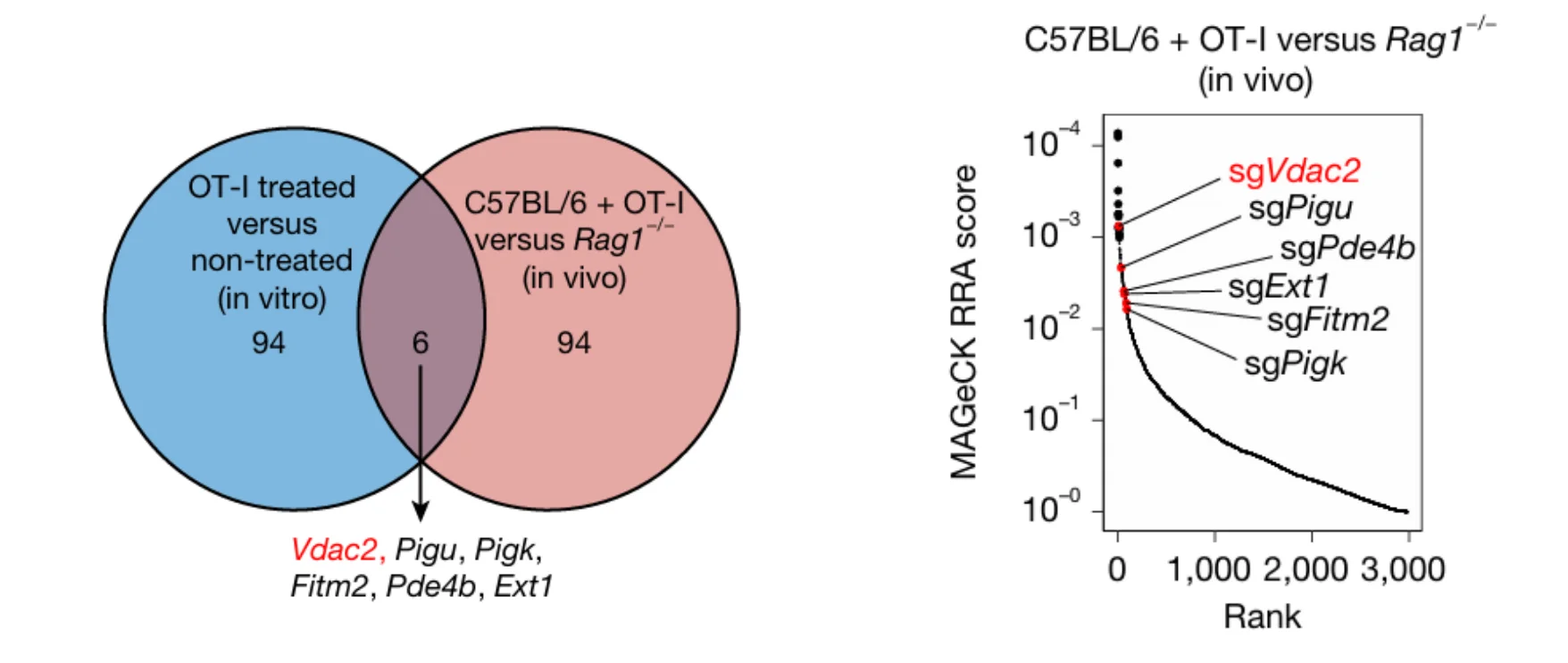
图2 体内和体外筛选鉴定免疫逃逸靶点
二、 Vdac2 基因敲除验证其在肿瘤免疫逃逸中的作用
在前期 CRISPR 文库筛选结果中,Vdac2基因的负向富集最为显著,提示其可能在肿瘤免疫逃逸过程中发挥关键作用。为进一步验证这一推测,研究者在 B16-OVA 细胞中构建了 Vdac2敲除株系,并结合体外 T 细胞共培养实验与体内小鼠移植瘤模型进行功能评估。
结果显示,敲除 Vdac2 明显增强了 OT-I 细胞对 B16-OVA 肿瘤细胞的杀伤能力,且在免疫健全小鼠体内,Vdac2 缺失显著抑制了肿瘤生长。上述结果充分证实,Vdac2 在肿瘤免疫逃逸中具有关键调控功能,其缺失可提升肿瘤细胞对免疫清除的敏感性。
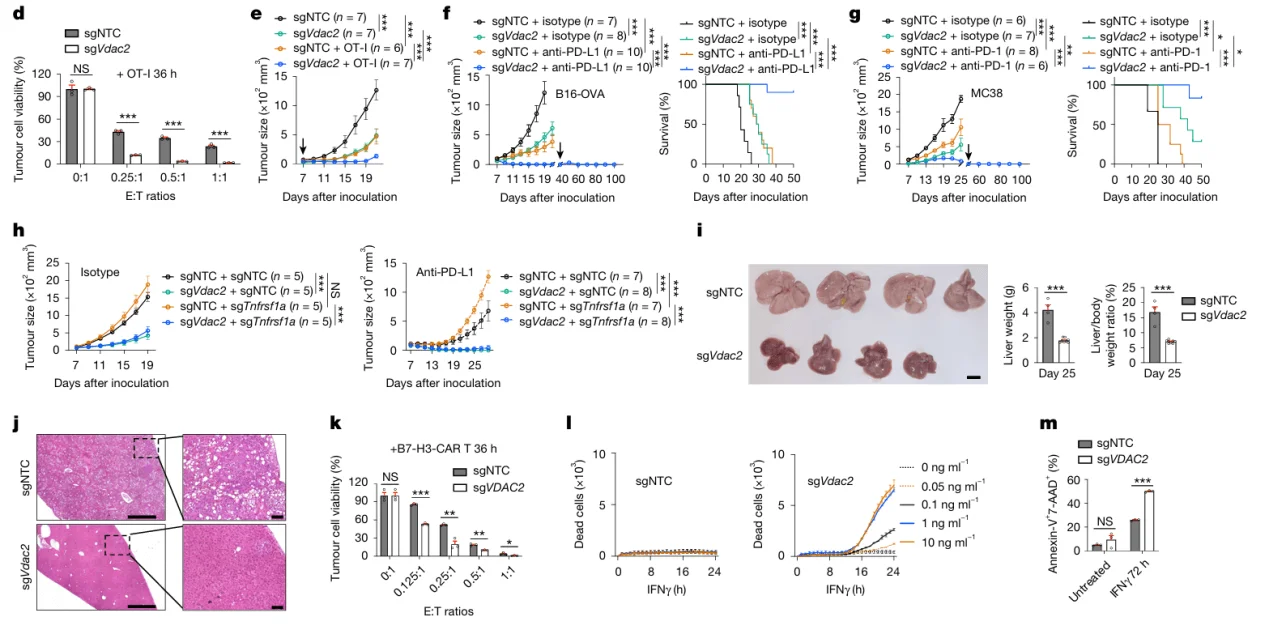
图3 Vadc2基因敲除验证
三、 Vdac2阻碍IFN-γ诱导的STING信号通路
为揭示Vdac2促进肿瘤细胞免疫逃逸的分子机制,研究者对 Vdac2 敲除与对照 B16-OVA 细胞进行了转录组分析。结果显示,Vdac2 缺失导致多条免疫相关通路显著激活,其中IFN-α与IFN-γ应答基因的表达均大幅上调。同时,基因集富集分析(GSEA)进一步揭示 cGAS-STING信号通路的活性显著增强。
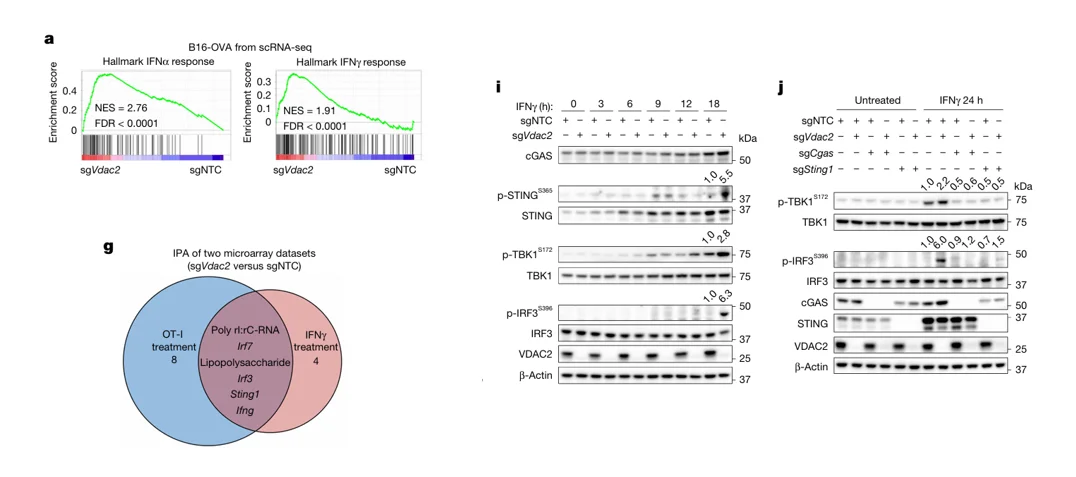
图4 Vdac2阻碍ifnγ诱导的STING信号传导
四、 CRISPR文库筛选揭示IFN-γ依赖性敏感基因
为进一步解析 IFN 通路在介导肿瘤细胞清除中的关键分子,研究者在Vdac2敲除的 B16-OVA 细胞基础上,开展了全基因组 CRISPR 敲除文库筛选。在筛选过程中,研究者给予细胞IFN-γ刺激,并通过比较实验组与对照组中 sgRNA 的丰度差异,寻找影响 IFN-γ诱导杀伤的潜在靶点。
结果显示,Casp9与Bak1(编码促凋亡蛋白 BAK)在筛选结果中显著富集。该结果提示,敲除 BAK 蛋白能够削弱 IFN-γ 对肿瘤细胞的杀伤作用,进一步证明线粒体凋亡通路 在 IFN-γ介导的免疫清除中发挥关键作用。
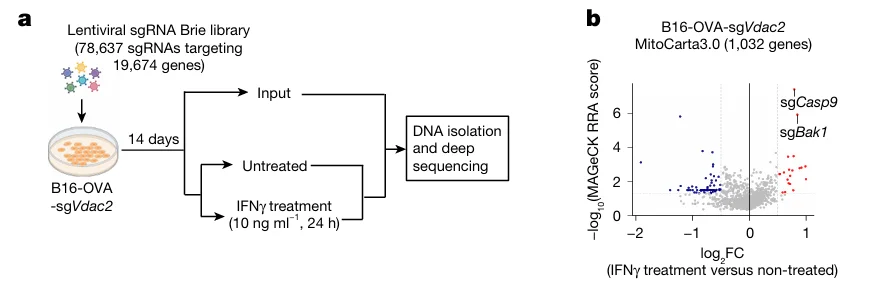
图5 CRISPR文库筛选IFNγ调控肿瘤细胞死亡靶点
五、 基因敲除验证 BAK 蛋白在 IFN-γ 介导的肿瘤细胞死亡中的作用
为验证 CRISPR 文库筛选结果,研究者在 B16-OVA 细胞中敲除Bak1基因,并在体外细胞共培养体系及体内小鼠移植瘤模型中对其功能进行了评估。结果表明,Bak1 缺失显著削弱了 IFN-γ 诱导的肿瘤细胞死亡,表现为细胞凋亡水平下降以及肿瘤在免疫健全小鼠体内的生长得到维持。
上述结果进一步确认,BAK 蛋白在 IFN-γ 依赖性肿瘤细胞凋亡过程中发挥关键作用,其缺失可为肿瘤细胞提供免疫逃逸优势。
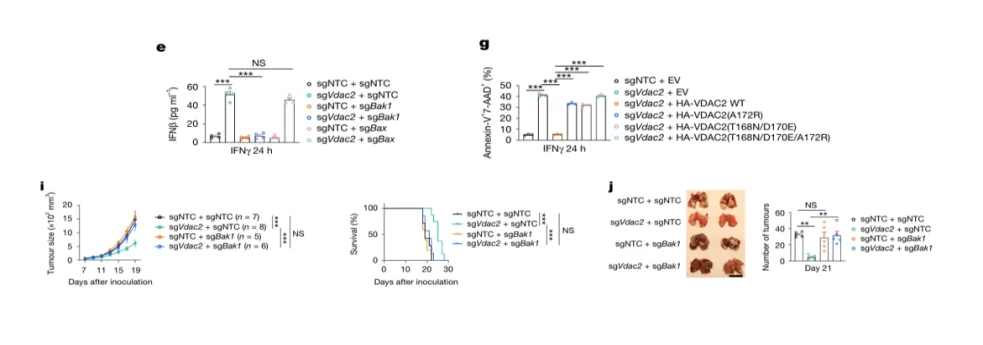
图6 BAK蛋白的敲除抑制IFNγ介导的肿瘤细胞死亡
新学期,新起点,也是科研突破的最佳时机!源井生物现已重磅推出体外+体内双体系文库筛选服务,配合全新iScreenAnlys™文库分析平台,全面开启靶点筛选的加速模式!
- - CRISPR文库体外筛选‒ 全流程筛选服务低至5W,快至6周, 一步到位,立即开筛无等待
- - CRISPR文库体内筛选‒ 在真实生理/肿瘤微环境中检验候选基因,精准还原肿瘤对免疫系统的反应;
- - iScreenAnlys™ 文库分析平台‒ 零代码基础使用,自动质控、MAGeCK 统计、通路富集,一键生成期刊级图表:靶点排名热图、差异基因火山图等,论文初稿或报告模板直接用!
从筛选设计到数据分析,源井生物为高校、研究所及医疗机构科研客户提供全方位支持。让“体内外基因筛选”不再是高门槛挑战,而是转化为科研中的利器;让你的实验进程更快、结果更可靠、靶点发现更具价值。
参考文献
Yuan S, Sun R, Shi H, Chapman NM, Hu H, Guy C, Rankin S, Kc A, Palacios G, Meng X, Sun X, Zhou P, Yang X, Gottschalk S, Chi H. VDAC2 loss elicits tumour destruction and inflammation for cancer therapy. Nature. 2025 Apr;640(8060):1062-1071.












