小细胞肺癌治疗新突破:血管STING调控NK细胞浸润并增强CAR-NK疗效


引言
小细胞肺癌(SCLC)多呈 “冷肿瘤” 表型,免疫浸润稀少,对免疫治疗响应率低。神经内分泌型 SCLC 因 MHC-I 表达缺陷,本应易受 NK 细胞杀伤,但临床中 NK 细胞却被排斥在肿瘤区域外。Marco Campisi 团队在 Cancer Cell 发表的研究,首次揭示 肿瘤血管是 NK 细胞募集的主要屏障, 激活血管 STING 信号 可恢复 NK 细胞迁移与毒性,显著增强 DLL3 靶向 CAR-NK 疗法疗效, 为 SCLC 治疗开辟新方向。

研究背景
SCLC 的免疫抑制微环境是治疗抵抗的关键,其神经内分泌亚型存在 MHC-I 抗原呈递缺陷,但 NK 细胞浸润不足导致免疫优势无法发挥。肿瘤血管作为免疫细胞进入 TME 的物理屏障,其调控作用尚未明确。STING 信号可激活炎症反应,但 SCLC 肿瘤细胞中 STING 常被沉默,而血管及基质细胞中的 STING 功能是否可利用仍需探究。此外,CAR-NK 疗法在实体瘤中受限于浸润不足,亟需优化联合策略。
研究目的
- 明确 SCLC 中 NK 细胞浸润不足的核心机制,验证肿瘤血管的调控作用;
- 阐明血管 STING 激活对 NK 细胞功能的影响;
- 开发 STING 激动剂与 DLL3 CAR-NK 的联合治疗策略,改善 SCLC 免疫治疗效果。
研究方法
临床样本分析:
收集 34 例 SCLC 患者样本,通过多重免疫荧光、空间转录组学分析 NK 细胞浸润及血管状态;整合公共数据集验证预后相关性。
动物模型:
构建同源 SCLC 模型、人源化血管化异种移植模型,评估 STING 激动剂与 CAR-NK 联合治疗的体内疗效。
细胞实验:
采用 SCLC 细胞系、原代 NK 细胞等,通过共培养、细胞毒性实验验证 NK 细胞敏感性;利用 CRISPR-Cas9 敲除关键基因,探究调控机制;STING 激动剂处理检测血管黏附分子及趋化因子表达。
分子机制验证:
通过 DynaMITE-seq、CellChat 分析等,解析 STING 激活后血管 - 免疫细胞信号交流。
治疗验证:
构建 DLL3 靶向 CAR-NK 细胞,在体内外模型中评估 STING 激动剂的增强效应。
研究路线
1. 理论验证
验证 MHC-I⁻ˡᵒʷ/ⁿᵉᵍ SCLC 对 NK 细胞的体外敏感性与体内浸润不足的悖论;
2. 关键屏障鉴定
鉴定肿瘤血管为 NK 细胞浸润的关键屏障;
3. 迁移与活化的机制阐明
阐明血管 STING 激活促进 NK 细胞迁移与活化的机制;
4. 抗 SCLC 效果验证
验证 STING 激动剂与 CAR-NK 联合治疗的抗 SCLC 效果。
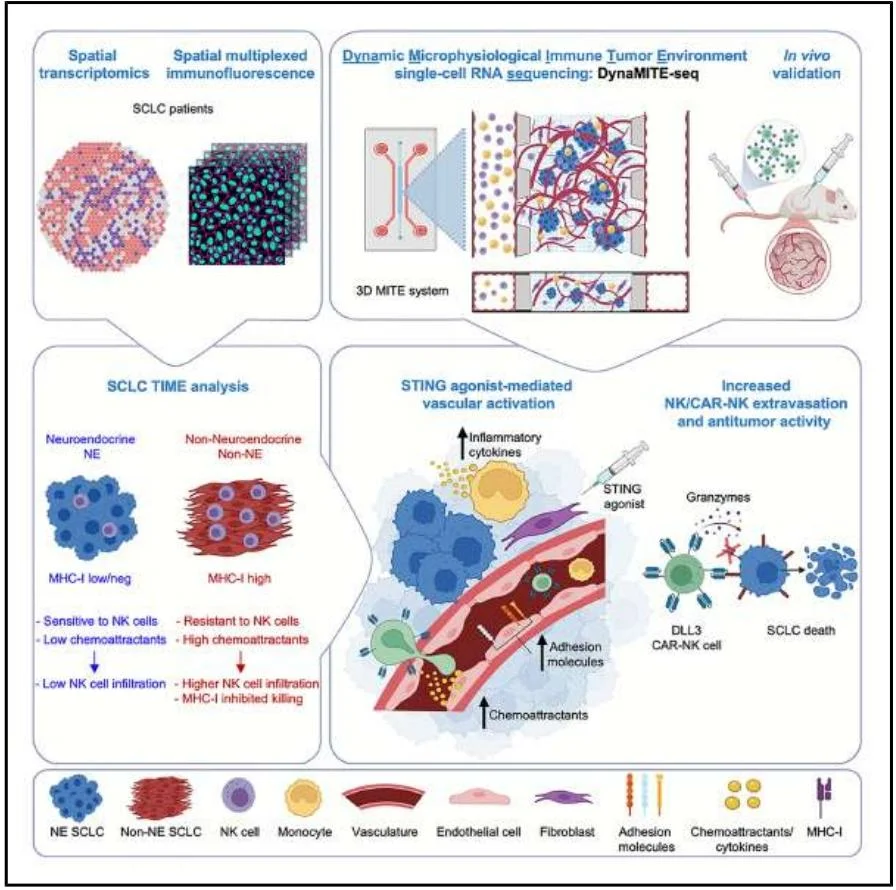
摘要图解
主要结果
1.MHC-Iˡᵒʷ/neg SCLC 体外对 NK 细胞敏感,体内浸润不足
MHC-Iˡᵒʷ/neg SCLC 细胞系对 NK 细胞杀伤高度敏感,而患者样本中该亚型瘤内 NK 细胞浸润稀少,且 NK 细胞更倾向定位于 MHC-Ihigh 区域;NK 细胞低浸润患者生存期更短。
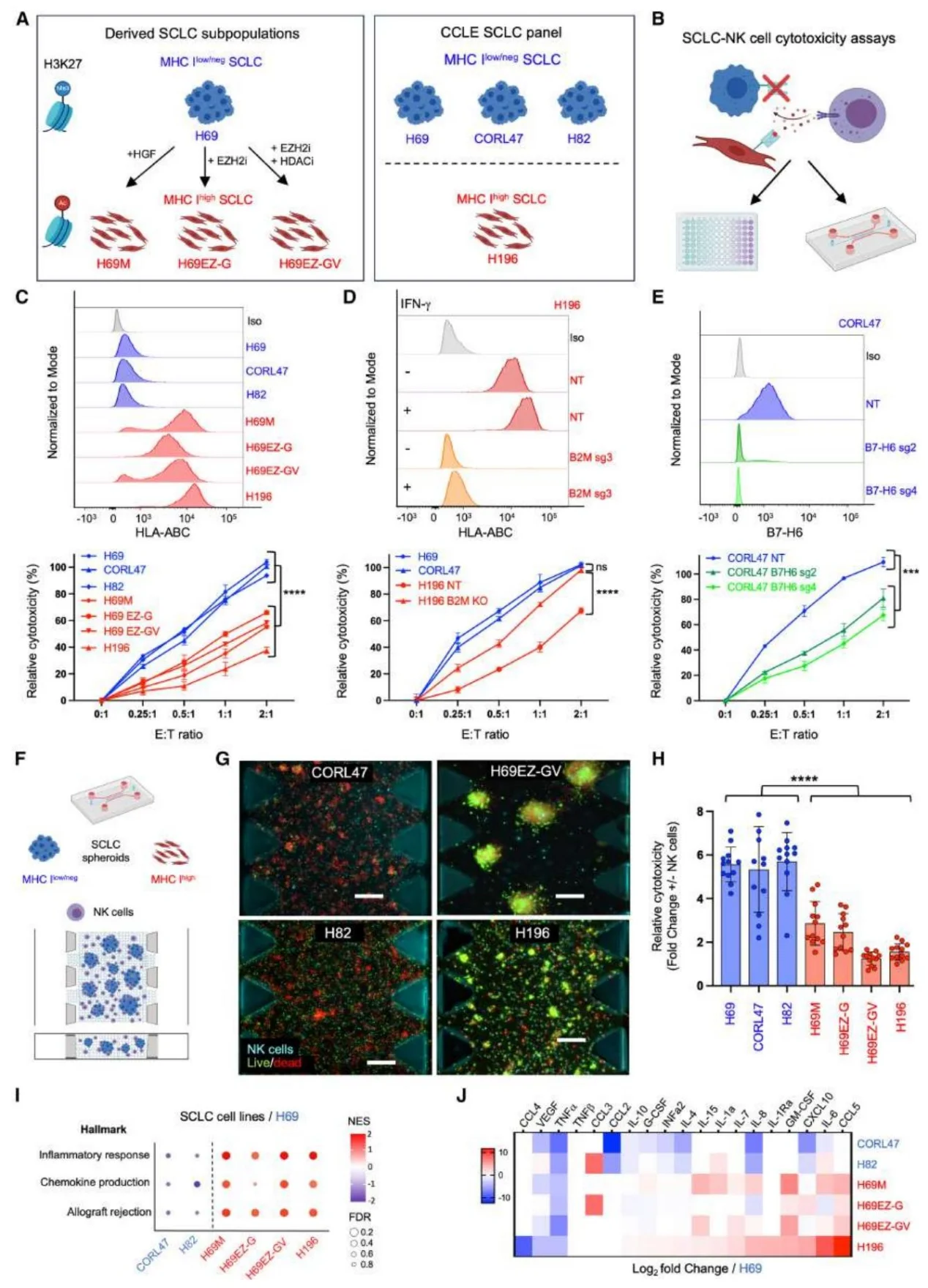
图1.MHC I类低表达/阴性小细胞肺癌(SCLC)对 NK 细胞介导的细胞毒性敏感
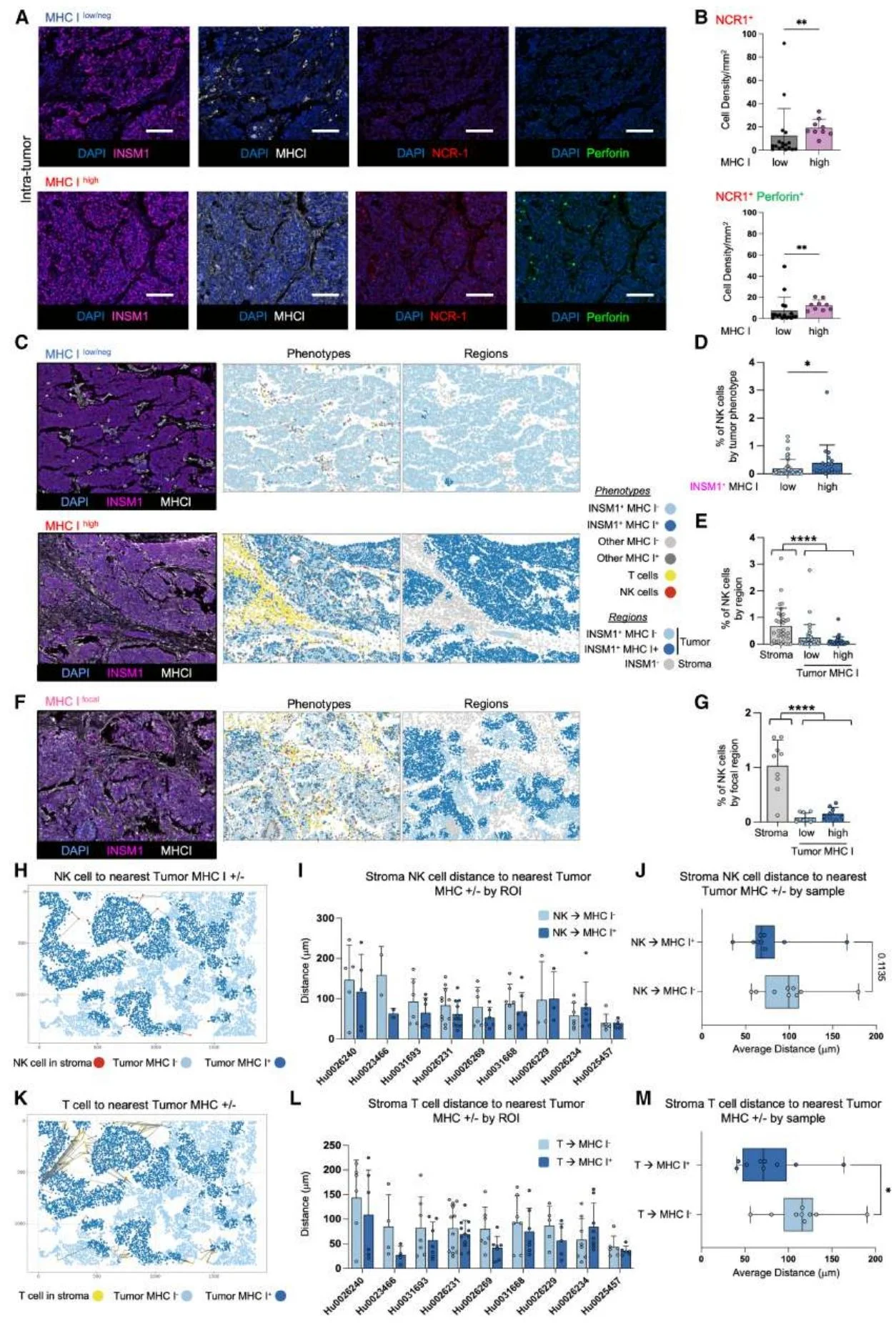
图2.MHC-Ilow/neg小细胞肺癌(SCLC)呈现稀疏的区域性 NK 细胞浸润
2. 肿瘤血管是 NK 细胞浸润的核心屏障
MHC-Iˡᵒʷ/neg SCLC 的趋化因子表达下调,STING 在肿瘤细胞中低表达但在血管基质细胞中高表达;STING 激动剂可诱导血管内皮细胞上调黏附分子(VCAM1、ICAM1)及趋化因子(CXCL10),MHC-Ihigh 区域血管具有更高活化特征并与 NK 细胞共定位。
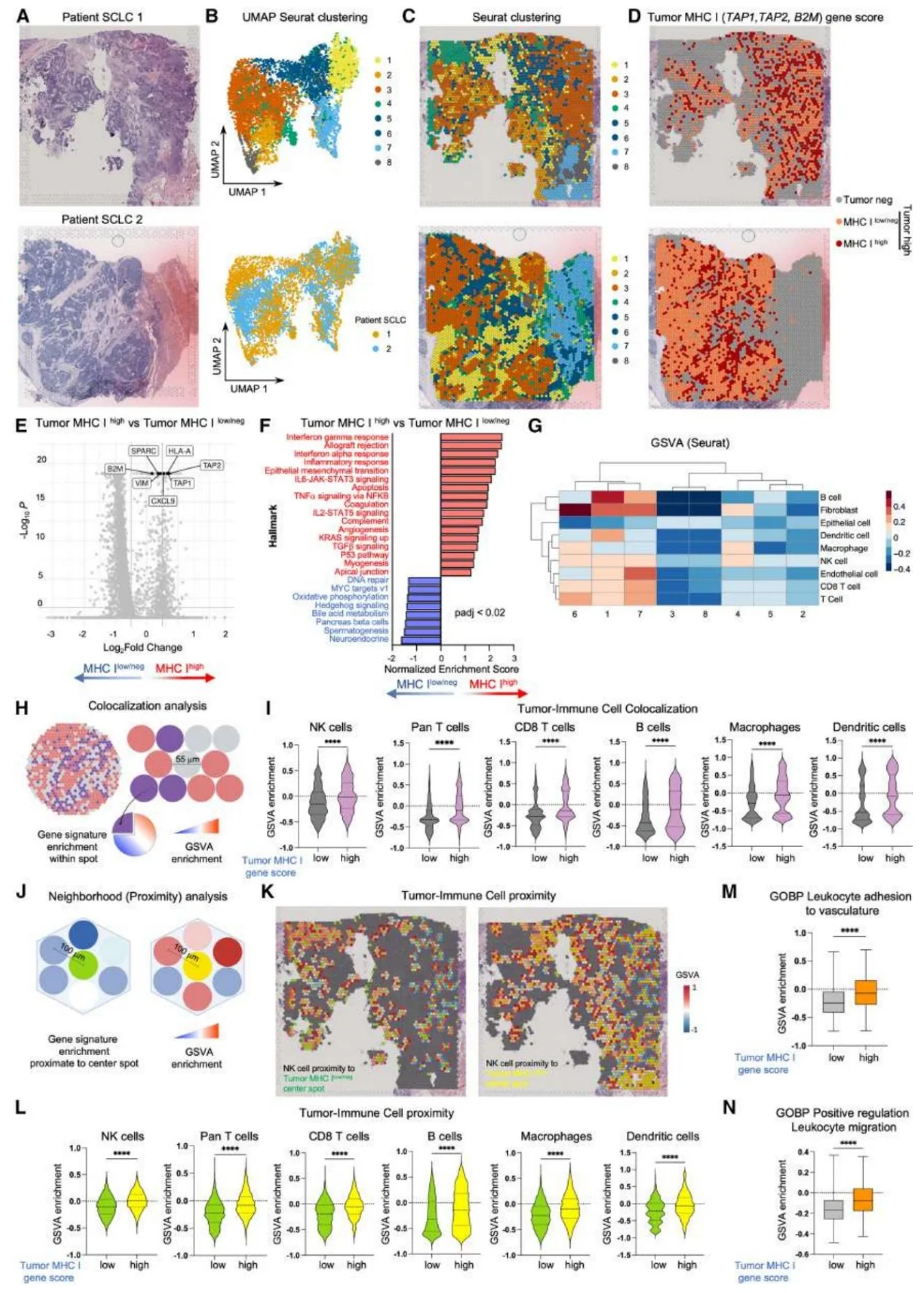
图3.MHC-Ilow/neg小细胞肺癌TIME检测显示免疫参与和血管激活不足
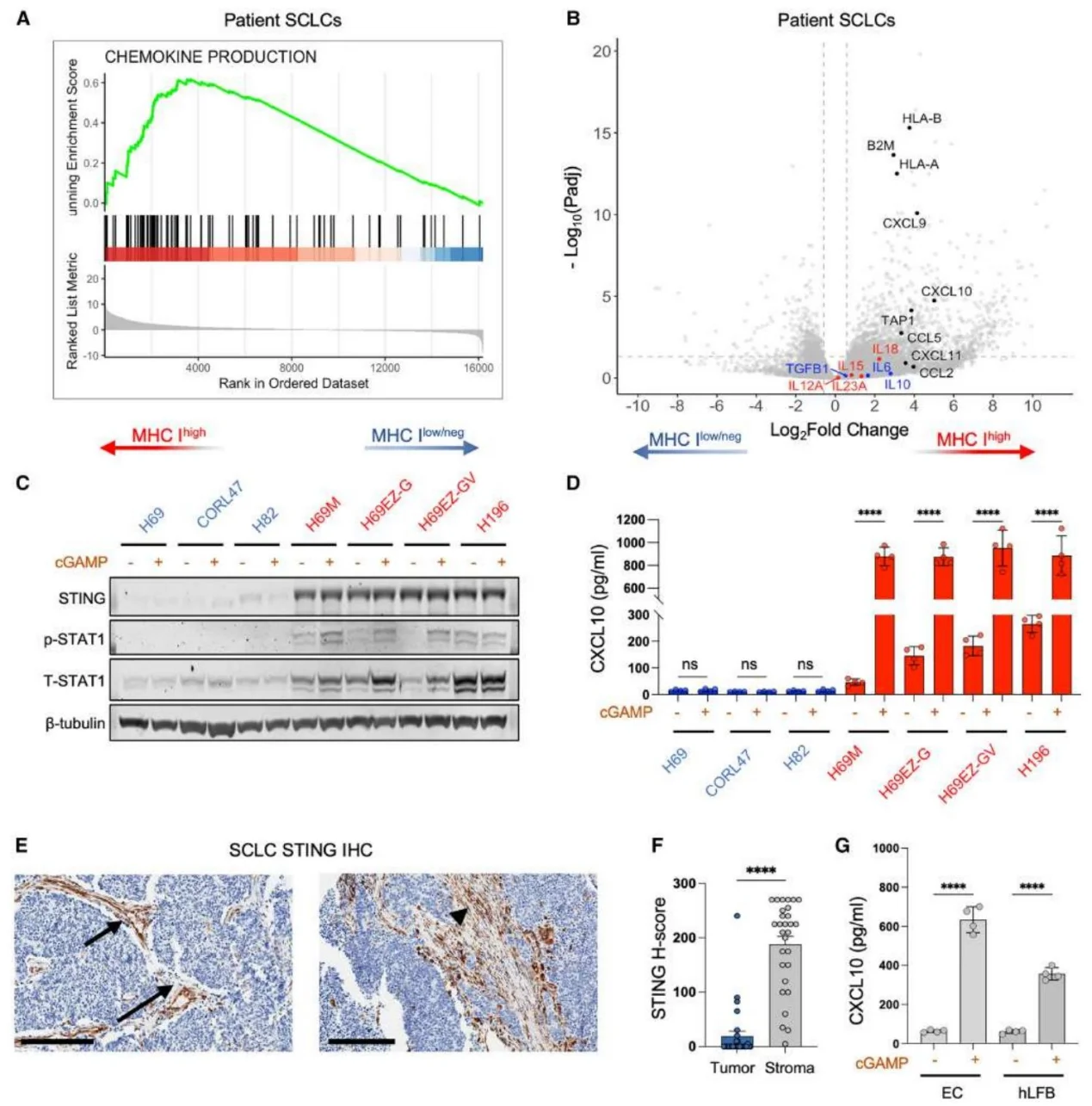
图4.MHC-Ilow/neg小细胞肺癌TIME分析显示肿瘤内在与外在免疫特征不匹配
3. 血管 STING 激活促进 NK 细胞迁移与活化
STING 激动剂联合单核细胞可激活血管内皮的炎症及白细胞外渗通路,增强内皮细胞与 NK 细胞间 VCAM1、SELE 介导的相互作用;NK 细胞在该环境中活化标志物上调、抑制性受体下调,细胞毒性增强。
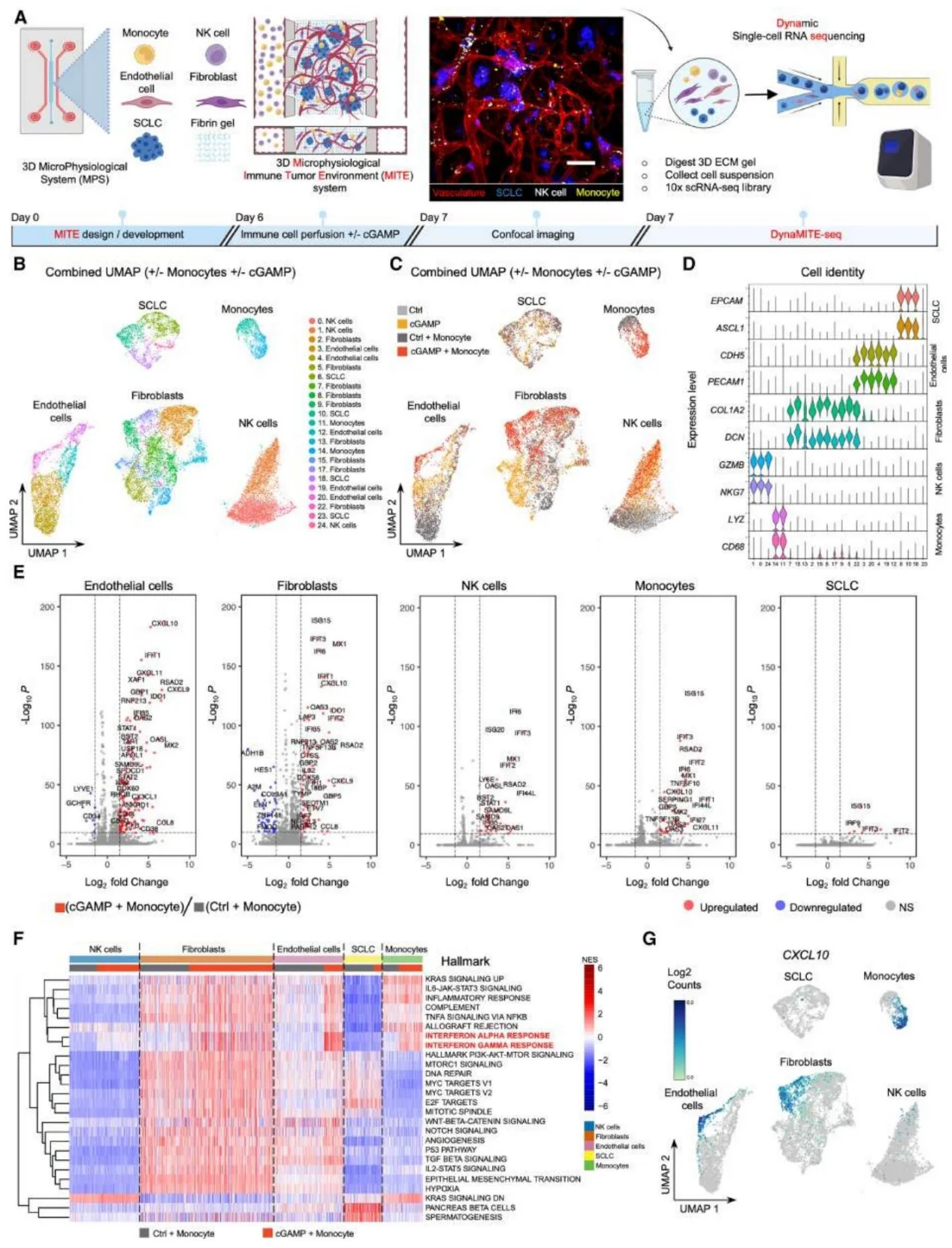
图5.可扰动微生理免疫肿瘤微环境(MITE)的高分辨率表征
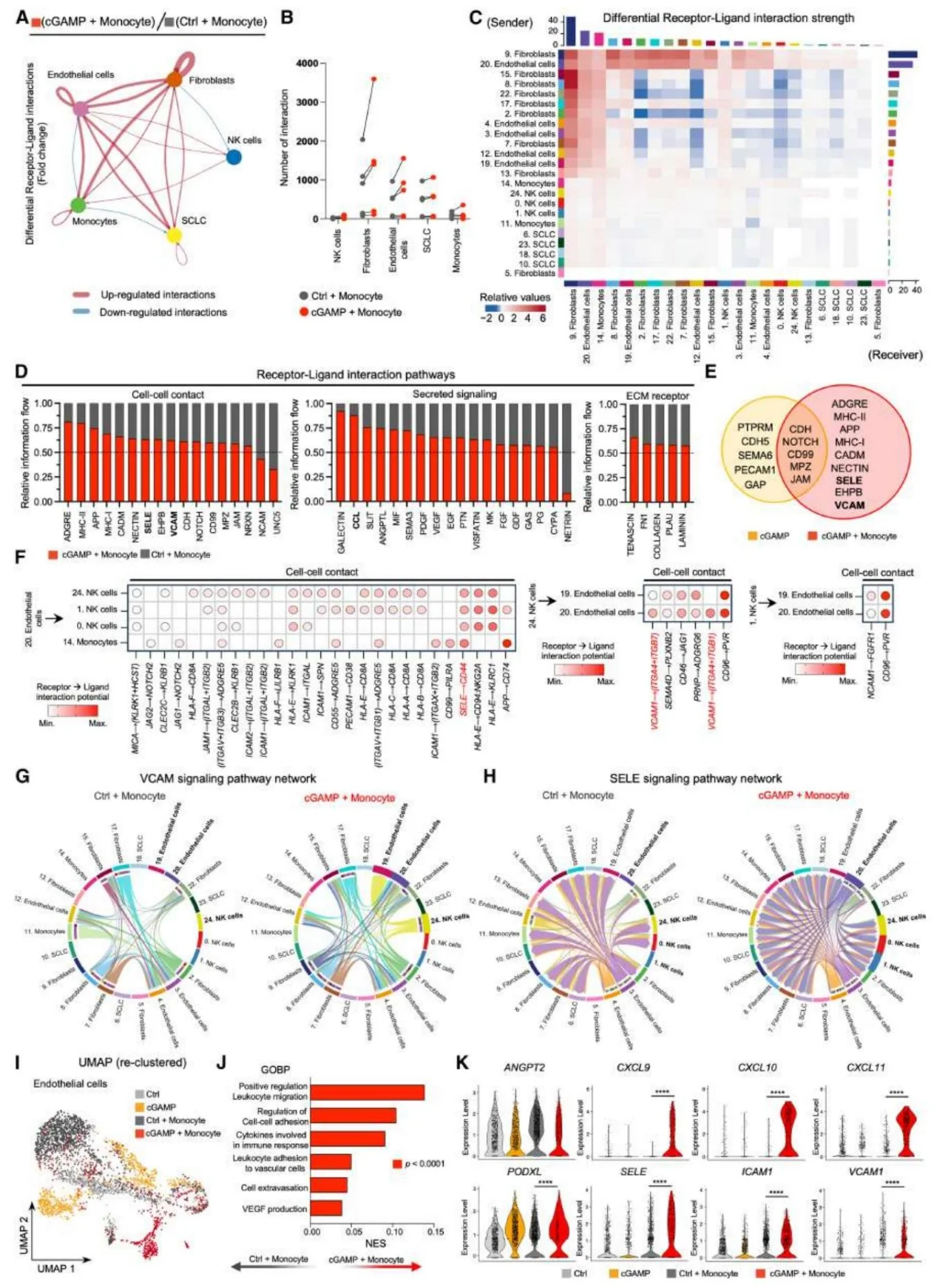
图6.DynaMITE-seq与受体-配体相互作用分析揭示刺痛激动剂介导的血管激活
4. STING 激动剂增强 DLL3 CAR-NK 疗法疗效
DLL3 CAR-NK 细胞杀伤 SCLC 能力优于未修饰 NK 细胞;STING 激动剂可增加 CAR-NK 细胞的血管黏附与肿瘤浸润。体内实验中,两者联合治疗显著抑制肿瘤生长,增加瘤内 CAR-NK 细胞浸润及炎症因子水平。
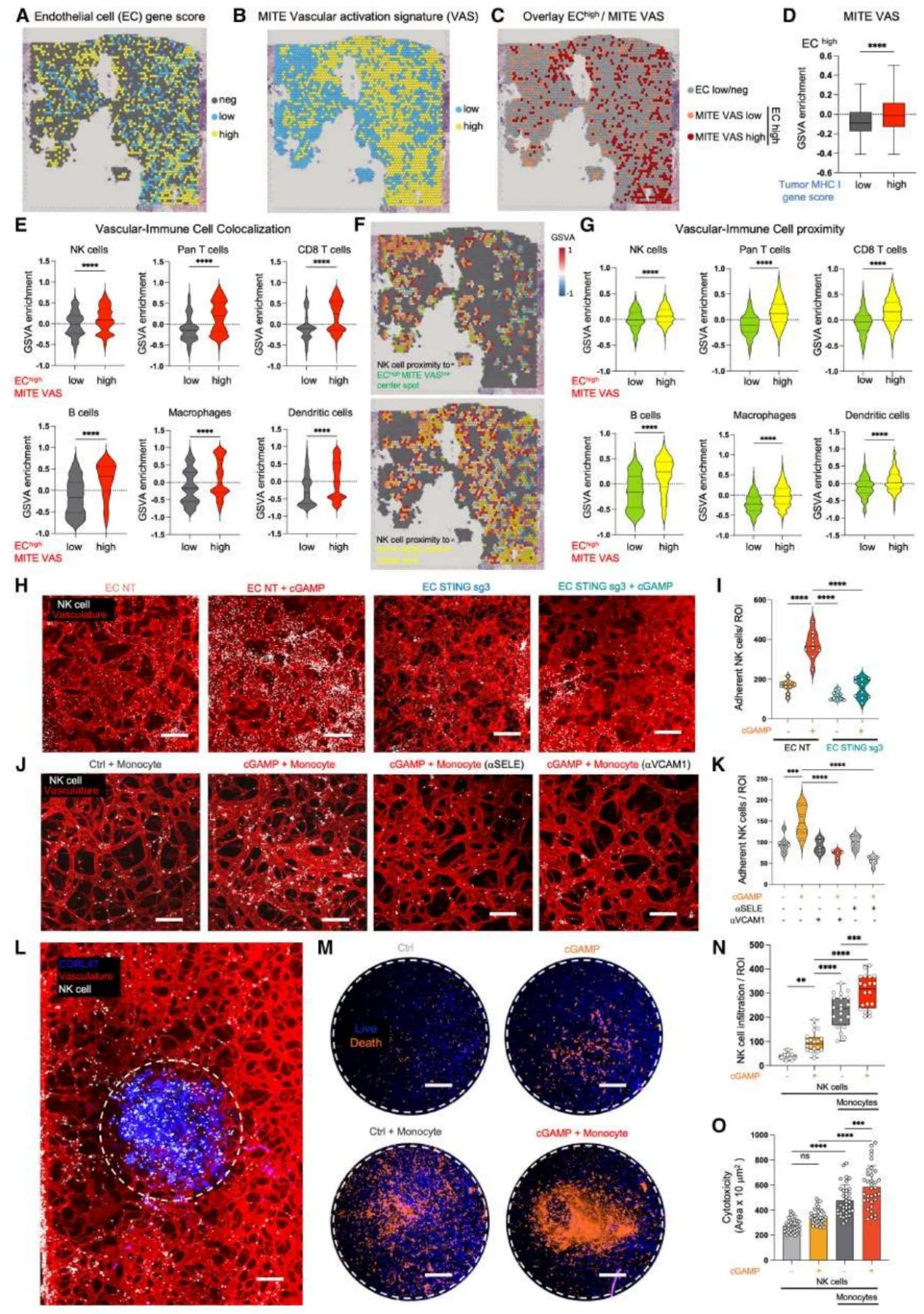
图7.整合空间与DynaMITE-seq分析表明,刺痛性激活性可促进 NK 细胞外渗并增强小细胞肺癌(SCLC)的抗肿瘤活性
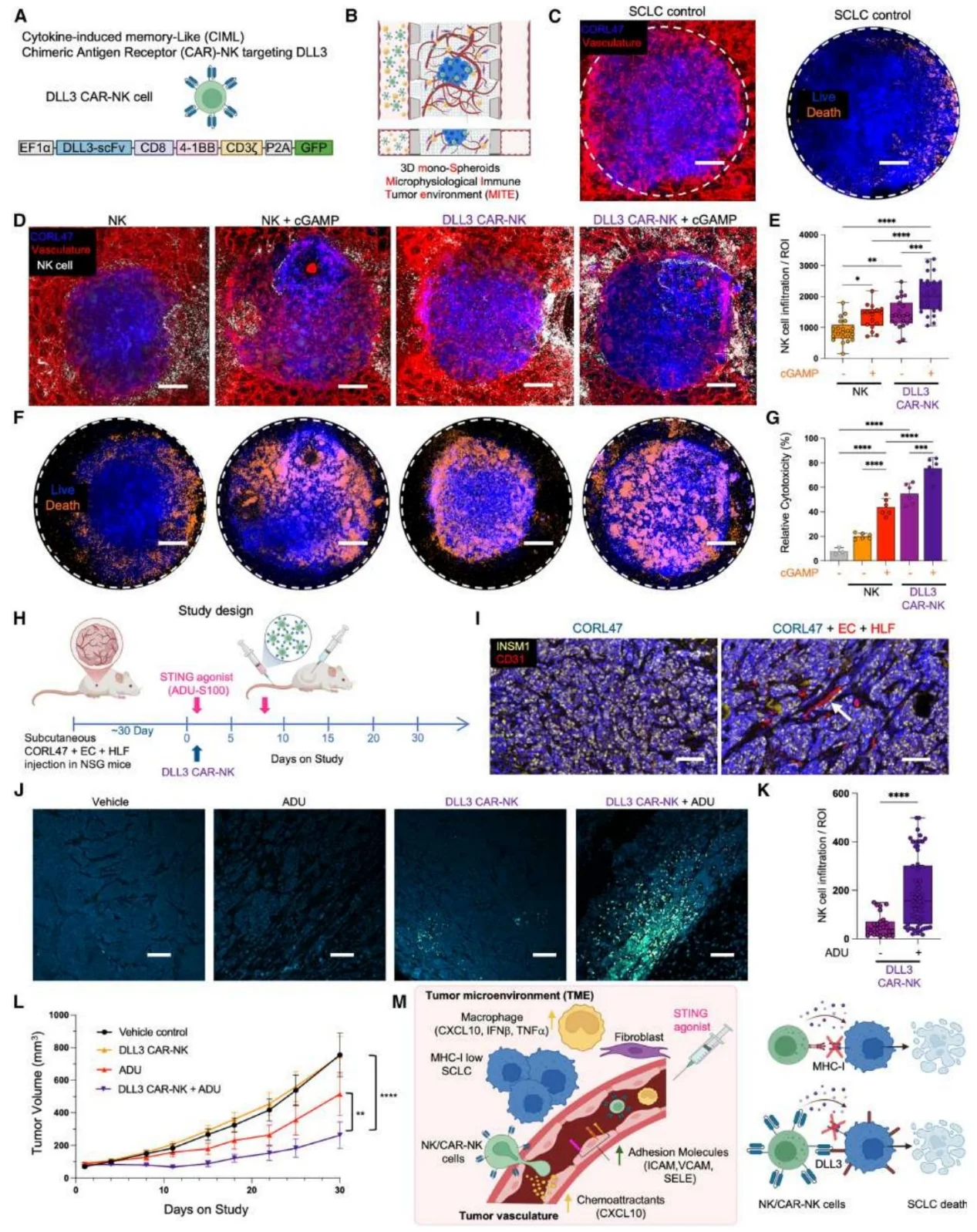
图8.在人MHC-Ilow/neg小细胞肺癌(SCLC)血管化异种移植模型中,刺痛激动作用促进DLL3 CAR- NK 细胞外渗并增强抗肿瘤活性
研究意义与创新点
- 机制创新: 揭示肿瘤血管是 SCLC NK 细胞浸润的关键屏障,阐明血管 STING 激活调控 NK 细胞功能的分子机制,破解 “敏感但浸润不足” 的核心悖论。
- 技术创新: 开发 DynaMITE-seq 结合 3D MITE 模型,实现肿瘤 - 血管 - 免疫细胞动态相互作用的高分辨率解析。
- 治疗创新: 提出 STING 激动剂与 DLL3 CAR-NK 联合方案,通过激活血管 STING 改善 CAR-NK 递送效率,为实体瘤 CAR-NK 疗法优化提供可转化策略。
文章小结
本研究明确肿瘤血管在 SCLC 免疫抑制中的核心作用, 阐明血管 STING 激活可打破免疫浸润屏障,增强 CAR-NK 细胞杀伤能力。 该发现填补了 SCLC 免疫微环境研究空白,STING 激动剂与 CAR-NK 的联合方案有望为 SCLC 患者带来新的治疗希望。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有13000+细胞产品(含10000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
STING是体内固有免疫反应的关键信号转导分子,被外源性DNA触发, 在调节体内自发性抗肿瘤免疫反应产生过程中发挥重要功能。 如果您也想针对STING展开研究,源井生物可为您提供STING基因敲除细胞,涵盖THP-1、Hela、A549等热门细胞系。如果您有个性化基因编辑的需要,欢迎咨询!
联系我们了解更多>>>










