体内 CRISPR 筛选锁定 OR7A10,CAR-NK 细胞疗法攻克实体瘤,实现 100% 完全缓解


引言
CAR-NK 细胞疗法在实体瘤治疗中前景广阔,但受肿瘤浸润弱、存续短、TME 耐药等问题限制。耶鲁大学团队在Nature发表最新研究, 通过体内 CRISPR 激活筛选与靶向 ORF 筛选,锁定 GPCR 家族的 OR7A10 为核心增强子。 经 OR7A10 cDNA 工程改造的 CAR-NK 细胞,无需 CRISPR 编辑,制备简便,可全面提升增殖、细胞毒性、代谢适应性等多项功能,降低细胞耗竭,在多种实体瘤模型中展现强效疗效(如原位乳腺癌模型 100% 完全缓解),为实体瘤提供高效可规模化的现成疗法。

研究背景
NK 细胞无需 MHC 限制和预先致敏,能靶向低突变负荷癌细胞,CAR-NK 疗法安全性高、GVHD 风险低,适合现成制造,目前全球超 1200 项相关临床试验,其中 CAR-NK 疗法超 160 项。但该疗法在实体瘤中面临肿瘤浸润不足、增殖弱、TME 中存续差等核心挑战。现有策略如细胞因子工程、抑制性基因敲除等依赖 CRISPR 编辑,增加制造复杂性。本研究通过 双重体内筛选, 鉴定可直接整合到 CAR 构建体的 “增强子” 基因,为 CAR-NK 细胞制造提供简单规模化方案。
研究目的
通过体内 CRISPR 激活筛选及靶向 ORF 筛选,系统性鉴定可增强 CAR-NK 细胞体内抗肿瘤功效的基因(称为 “超增强子” 或 “增强子”);明确 OR7A10 增强 CAR-NK 细胞多种功能的分子机制;验证 OR7A10 工程改造 CAR-NK 细胞在多种实体瘤模型中的体内疗效;评估 OR7A10 工程改造 CAR-NK 细胞的临床转化潜力(包括制造可行性、安全性等);探索 OR7A10 与其他激活信号的协同作用,为优化 CAR-NK 细胞疗法提供理论支撑。
研究方法
双重筛选策略
- 体内 CRISPRa 筛选:HT29 结直肠癌模型中,转染 SAM 文库的 HER2-CAR-NK92 细胞过继转移至荷瘤小鼠,NGS 分析 sgRNA 丰度差异;
- 体内条形码 ORF 迷你筛选:原代人 PBNK 细胞转染 HER2-CAR 及 ORF 文库,注射至荷瘤小鼠,3/6 天后收集肿瘤组织,NGS 量化 ORF 和 UMI 丰度。
功能验证与机制解析
构建 OR7A10 过表达(OR7A10 (OE))和终止突变(OR7A10 (STOP))细胞系;通过流式细胞术、共培养实验、Seahorse 代谢分析、TEM 等检测细胞功能;CRISPR-Cas9 敲除 GNAS 基因,结合小分子抑制剂,探索 GPCR 信号通路;批量 mRNA-seq 及单细胞转录组学分析基因表达谱。
体内疗效与安全性验证
在 HT29 结直肠癌、MCF7 乳腺癌、SKOV3 卵巢癌模型中,通过肿瘤体积测量、生物发光成像、生存曲线评估疗效;检测血清细胞因子水平、组织病理学分析、WGS 检测基因组完整性,评估安全性。
研究路线
全基因组 CRISPRa 筛选→靶向 ORF 筛选锁定 OR7A10→体外功能验证(增殖、细胞毒性等)→机制解析(信号通路、基因表达)→体内疗效与安全性验证→协同作用探索。
主要结果
1.体内双重筛选锁定 OR7A10
CRISPRa 筛选鉴定 66 个候选基因,ORF 迷你筛选验证 OR7A10 为唯一显著富集基因,其 UMI 在肿瘤样本中强烈富集。
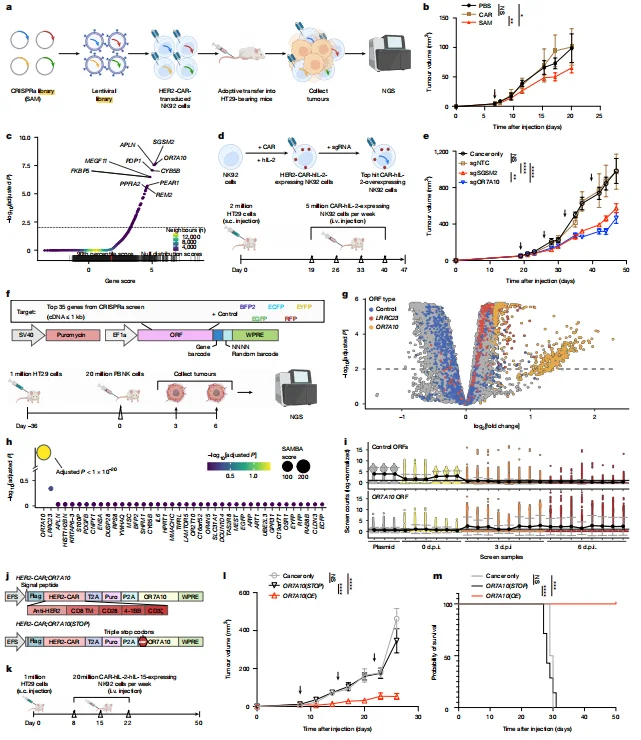
图1.体内CRISPRa与条形码ORF筛选鉴定OR7A10为CAR- NK 细胞抗肿瘤疗效的增强剂
2.OR7A10 增强 CAR-NK 细胞体内疗效
OR7A10 (OE) 转染的 CAR-NK 细胞在 HT29、MCF7、SKOV3 模型中显著抑制肿瘤生长,MCF7 模型实现 100% 完全缓解,且肿瘤浸润和体内存续能力增强。
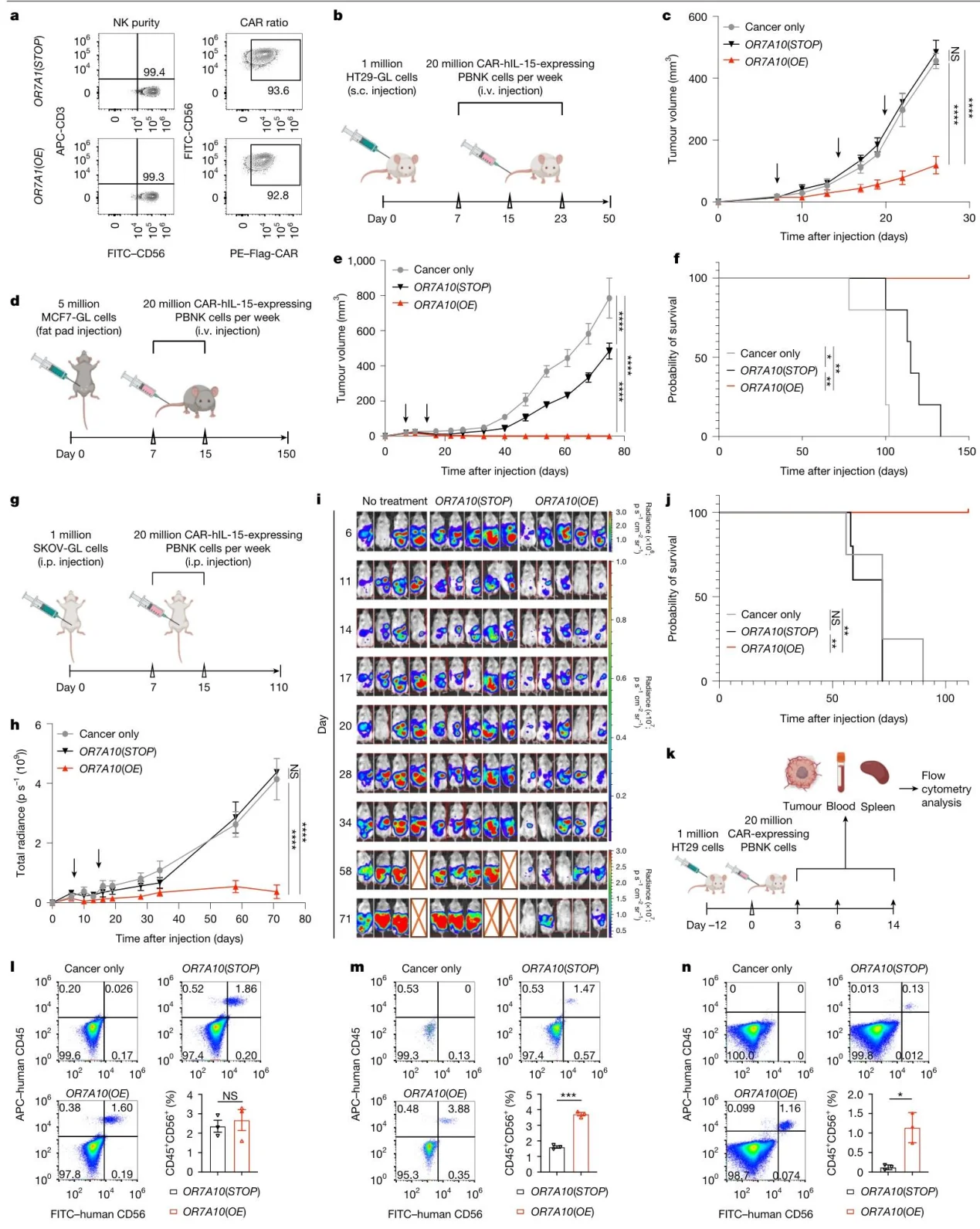
图2.经OR7A10开放阅读框(ORF)改造的CAR- PBNK 细胞在多种肿瘤模型中表现出显著的体内抗肿瘤活性及增强的肿瘤浸润能力
3.提升原代 CAR-NK 细胞多项效应功能
OR7A10 (OE) 转染的 PBNK 细胞对多种癌细胞的细胞毒性显著增强,脱颗粒、细胞因子(IFNγ、TNF)产生、死亡配体(FasL、TRAIL)表达均升高,增殖能力增强,耗竭标志物(TIM-3、LAG-3 等)表达降低。
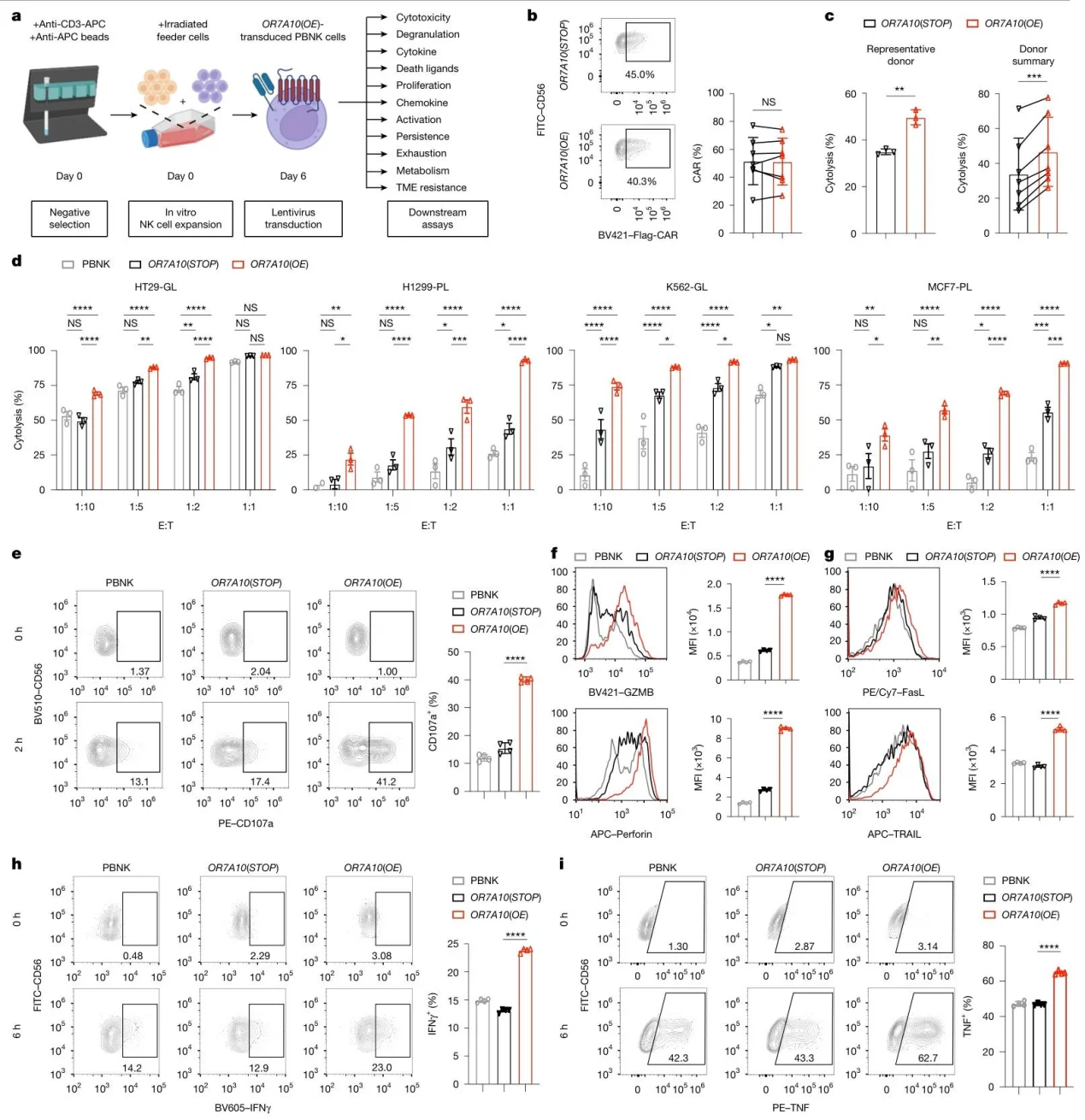
图3.OR7A10 ORF工程增强了CAR-PBNK细胞的抗肿瘤功能
4.增强代谢适应性与 TME 耐药性
OR7A10 (OE) 细胞基础 / 备用 / 最大氧消耗率升高,线粒体质量增加;在酸性环境、TGFβ、缺氧等免疫抑制条件下,细胞毒性仍显著高于对照组。
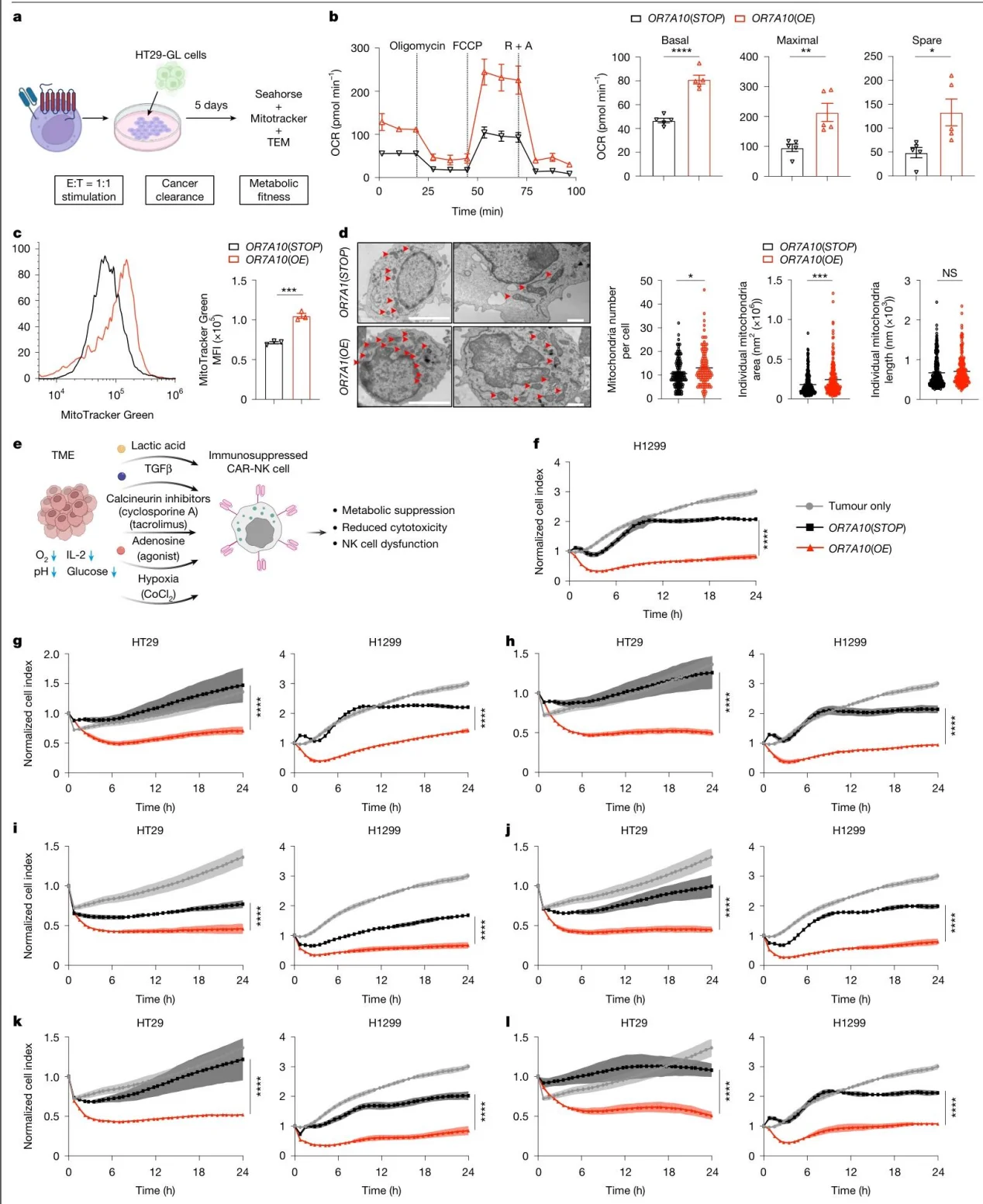
图4.OR7A10开放阅读框工程化可增强CAR- PBNK 细胞的代谢适应性及对 TME 相关免疫抑制的耐受性
5.单细胞转录组揭示调控特征
OR7A10 过表达对 8 个 NK 细胞亚群均有广泛影响,上调炎症细胞因子、细胞毒性基因,激活 NFAT、JNK 等通路。
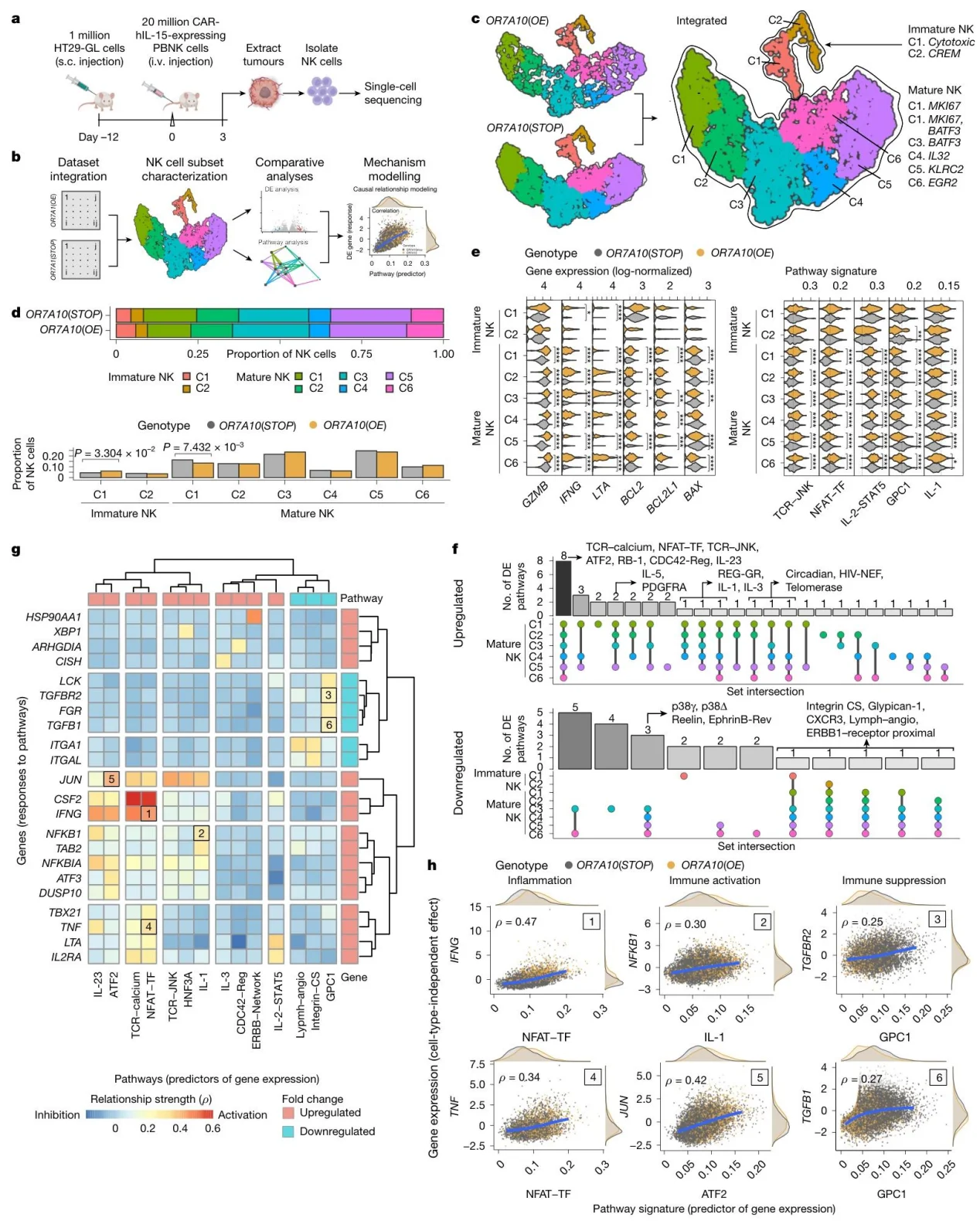
图5.SCT揭示了肿瘤浸润的人原代CAR- NK 细胞中OR7A10过表达所驱动的无偏倚体内基因表达改变
文章小结
本研究通过双重体内筛选鉴定出 GPCR 分子 OR7A10,其过表达可通过多种机制 全面提升 CAR-NK 细胞的增殖、细胞毒性、代谢适应性、肿瘤浸润能力及 TME 耐药性,降低细胞耗竭。 分子机制上,OR7A10 依赖 GPCR 相关信号通路调控基因表达谱。OR7A10 工程改造的 CAR-NK 细胞制造简便,在多种实体瘤模型中疗效显著且安全性良好,无 GVHD 风险,与 NKp46 信号具有协同作用。该研究深化了对 CAR-NK 细胞功能调控的理解,提供了高效、可规模化、安全的实体瘤 CAR-NK 细胞疗法,具有重要临床转化价值。
源井生物CRISPR-iScreen™文库
CRISPR-iScreen™是源井生物自主研发的一项创新技术,旨在实现高效的CRISPR筛选。目前,源井生物拥有超过40种的CRISPR文库现货供应,覆盖人类、小鼠、绿猴及猪等物种的全基因组基因敲除/抑制/激活文库;此外,还有针对激酶、细胞周期、膜蛋白、代谢等相关基因构建的CRISPR敲除/抑制/激活亚文库,助您轻松实现靶点筛选!目前源井拥有150+文库病毒现货,文库Cell Pool数量突破600,还提供一站式CRISPR文库(体内/体外)功能筛选服务,随时支持您的研究需求。
联系我们了解更多>>>










