GR-FAS轴成播散性肿瘤细胞(DTCs)免疫逃逸关键,靶向联合疗法破局TNBC转移


引言
三阴性乳腺癌(TNBC)等实体瘤患者的 主要死亡原因是转移, 肿瘤细胞从原发灶扩散后,需逃避全身免疫监视并在新器官定植形成转移灶。目前,关于初始播散性肿瘤细胞(DTCs)在新器官播种后如何克服抗肿瘤免疫的机制尚不清楚。近日,来自丹娜-法伯癌症研究所(Dana-Farber Cancer Institute) 的研究团队在 Nature 发表最新研究, 首次揭示糖皮质激素受体(GR)-FAS 轴是 DTCs 在转移性播种期实现免疫逃逸的关键调控机制, 证实 GR 激活可通过抑制 FAS 表达,帮助 DTCs 逃避 CD8⁺T 细胞和自然杀伤(NK)细胞的 FASL 介导杀伤;同时发现 GR 抑制剂与免疫治疗联合使用可显著减少转移负荷并延长小鼠生存期,为预防肿瘤转移提供了全新靶点和治疗策略。

研究背景
TNBC 具有早期复发特性,转移性 TNBC 被认为是不治之症。DTCs 通常对化疗等传统疗法具有抗性,免疫治疗成为清除 DTCs 的潜在方案,但 DTCs 在转移性播种早期的免疫逃逸机制尚未明确。此前研究多聚焦于肿瘤组织中的免疫逃逸,而 DTCs 脱离原发肿瘤微环境后,需进化出独特的免疫抵抗机制。 GR 在 TNBC 患者中与不良预后相关,且在临床前模型中与转移相关,但 GR 在 DTCs 免疫逃逸中的具体作用及分子机制仍需深入探究。
研究目的
鉴定 DTCs 在转移性播种期逃避抗肿瘤免疫的关键分子机制,明确 GR 在该过程中的功能及调控路径,验证 GR 作为治疗靶点的有效性,开发针对 DTCs 的联合治疗策略,为预防 TNBC 转移提供理论依据和实验支持。
研究方法
临床样本与数据库分析
整合 AURORA US 数据集、TBCRC-030 临床试验数据等公共数据库,分析 GR、FAS 表达与 TNBC 患者转移复发及生存期的相关性,验证 GR 活性特征在原发肿瘤与转移灶中的差异。
动物模型构建:
构建 BALB/c、C57BL/6J、NSG(免疫缺陷)、Jedi(表达 GFP 特异性 CD8⁺T 细胞)等小鼠模型,建立 4T1、E0771 等 TNBC 皮下肿瘤模型、肺转移模型,通过 GR 敲低(shGR)、诱导性敲低(Dox-shGR)、Fas 敲低(shFas)等基因工程手段,评估 GR 对 DTCs 存活、转移及小鼠生存期的影响;利用抗体耗竭 CD8⁺T 细胞、NK 细胞,验证免疫细胞在 GR 调控转移中的作用。
细胞实验
通过慢病毒转染构建 shGR、shFas、Rela 敲除等细胞系,利用地塞米松(Dex)激活 GR;分离小鼠脾脏 CD8⁺T 细胞、骨髓来源 NK 细胞,人外周血单核细胞来源 CD8⁺T 细胞、NK-92 细胞,通过共培养实验验证 GR 激活对肿瘤细胞抵抗免疫细胞杀伤的影响;采用体外 FASL 处理实验检测 FAS 介导的凋亡。
分子机制验证
采用 bulk RNA-seq、单细胞 RNA-seq(scRNA-seq)分析基因表达差异;通过染色质免疫沉淀(CUT&RUN)验证 GR 与 Fas 启动子的结合;利用 CellChat 分析细胞间信号通路;通过免疫荧光(IF)、流式细胞术检测蛋白表达及细胞表型;采用 BH3 分析评估凋亡敏感性。
治疗验证
使用 GR 抑制剂米非司酮(mifepristone,RU486)与抗 PD-1 抗体联合治疗,在小鼠转移模型中评估治疗效果,检测转移负荷、免疫细胞浸润及相关分子表达变化。
研究路线
- DTCs 免疫逃逸关键分子筛选 利用 GFP 可视抗原系统分离逃避 T 细胞杀伤的 DTCs,通过转录组分析鉴定核心调控因子 GR;
- GR 功能验证 在细胞和动物模型中,证实 GR 激活可促进 DTCs 存活和转移,且依赖于 CD8⁺T 细胞和 NK 细胞;
- 分子机制解析 阐明 GR 通过抑制 FAS 表达,阻断 FAS-FASL 介导的细胞凋亡,进而逃避免疫杀伤的调控路径,明确 GR 通过 NF-κB 通路调控 FAS 表达;
- 联合治疗策略验证 在小鼠模型中验证 GR 抑制剂与抗 PD-1 抗体联合使用的抗转移效果及安全性。
主要结果
1. GR 激活是 DTCs 逃避免疫杀伤的关键驱动因素
转录组分析显示,逃避 T 细胞杀伤的 DTCs 中 GR 编码基因 Nr3c1 表达显著升高,GR 活性特征增强;免疫荧光证实,肺 DTCs 中 GR 呈核定位(转录激活状态),而原发肿瘤中 GR 呈胞质弥散分布。
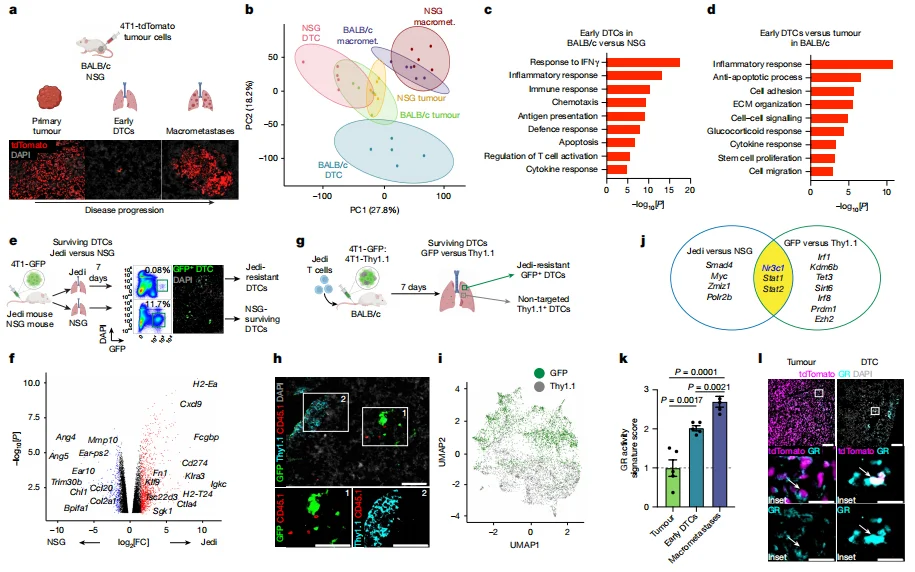
图1.逃逸T细胞杀伤的DTCs表达Nr3c1激活程序
2. GR 激活以免疫依赖方式促进 DTCs 转移和存活
GR 敲低不影响原发肿瘤生长,但显著减少 BALB/c 小鼠肺微转移灶数量,且在免疫缺陷 NSG 小鼠中无此效应;GR 激活可保护 DTCs 免受 CD8⁺T 细胞和 NK 细胞的联合杀伤,延长小鼠生存期。
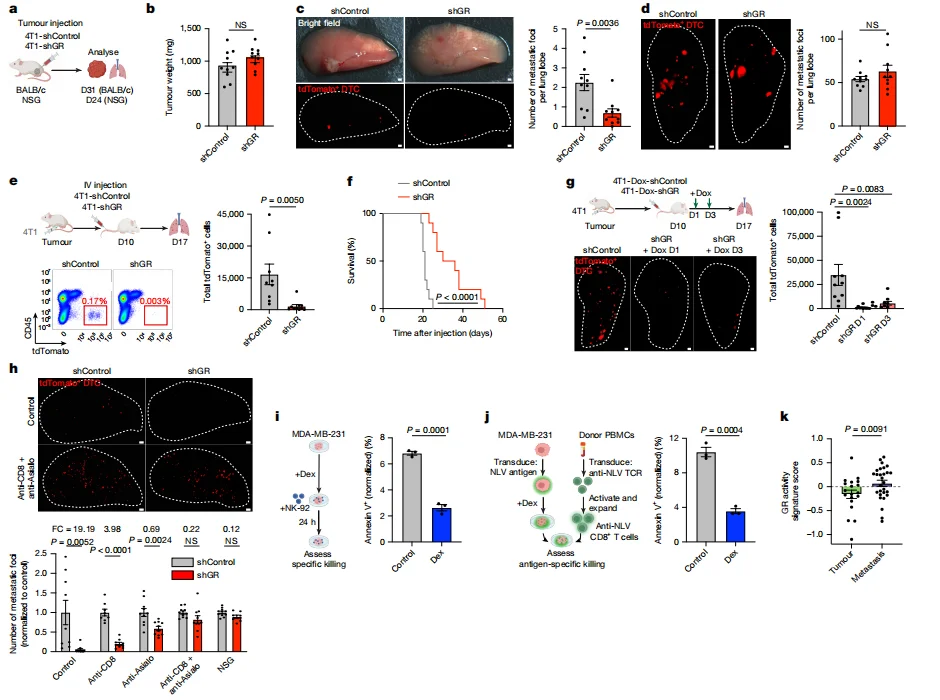
图2.肿瘤细胞中的糖皮质激素受体(GR)通过增强细胞毒性淋巴细胞耐药性促进肺转移
3.GR 通过抑制 FAS 表达阻断凋亡性
GR 敲低的 DTCs 中 FAS 表达升高,GR 激活(地塞米松处理)可降低人、鼠肿瘤细胞的 FAS 表达;临床样本分析显示,转移性 TNBC 中 FAS 活性低于原发肿瘤,FAS 低表达与复发风险增加相关。
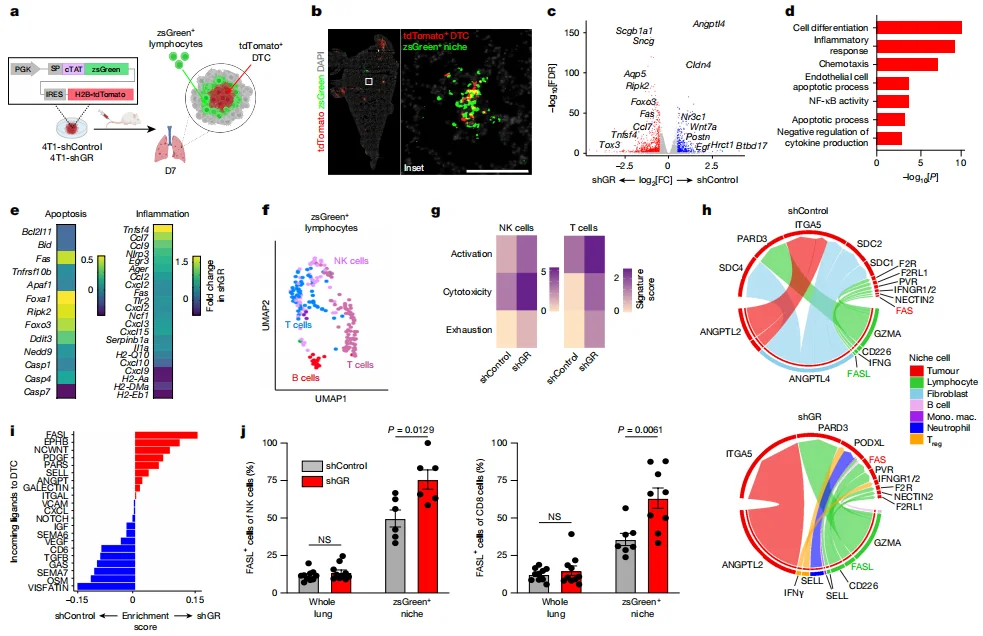
图3.DTCs中的GR激活可调节相互作用淋巴细胞的细胞毒性
4. GR 通过阻断 NF-κB 通路抑制 FAS 表达
CUT&RUN 实验证实,GR 结合 Fas 启动子的 NF-κB 结合位点,阻断 NF-κB 的转录激活作用,从而抑制 FAS 表达;GR-FAS 轴通过抑制 BID 介导的内在凋亡通路,保护 DTCs 免受 FASL 诱导的杀伤。
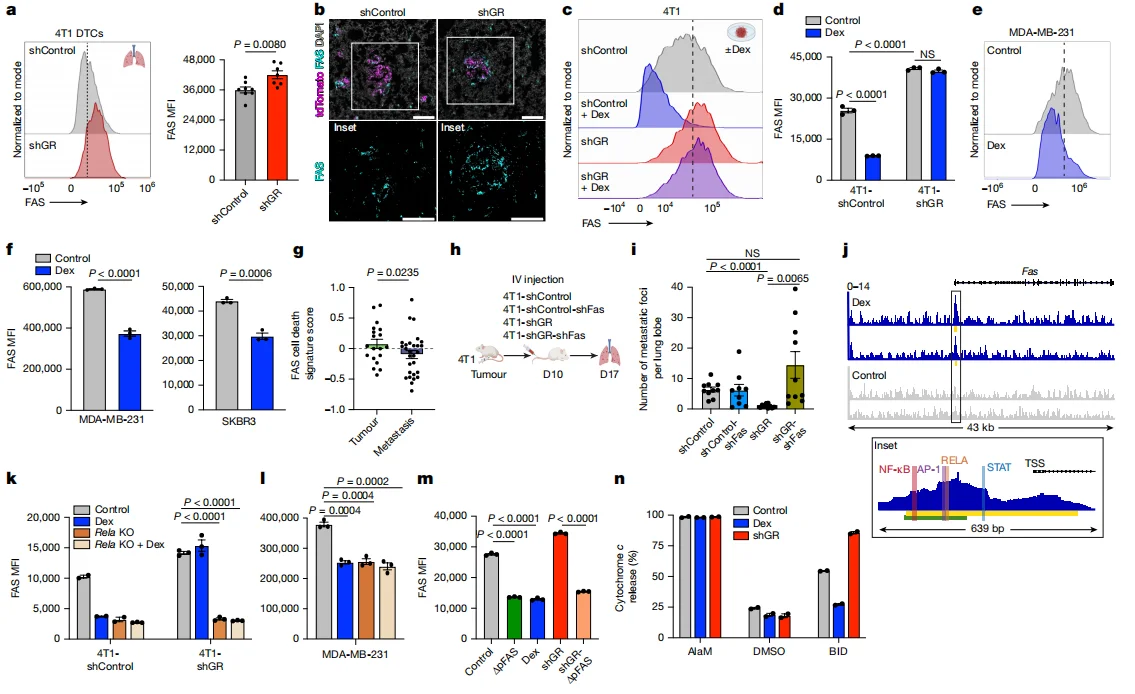
图4.GR激活直接抑制FAS以保护DTC免受免疫介导的杀伤
5. GR 抑制剂与抗 PD-1 联合治疗有效抑制转移
GR 敲低可增强 DTCs 对 PD-1 抑制剂的敏感性;米非司酮(GR 抑制剂)与抗 PD-1 联合治疗,能显著减少肺转移负荷,增加 FAS⁺DTCs 及 FASL⁺免疫细胞比例,延长小鼠生存期。
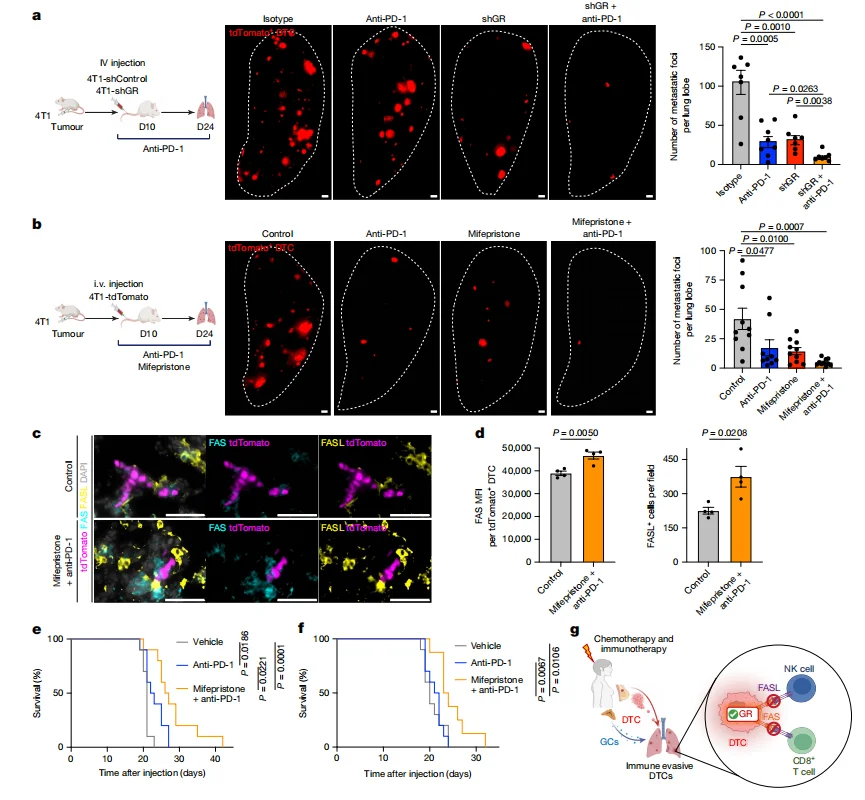
图5.阻断GR活性可增强抗PD-1免疫疗法对DTCs的清除作用
研究意义与创新点
- 概念突破: 首次揭示 GR-FAS 轴是 DTCs 转移播种期免疫逃逸的核心机制,填补了相关研究空白。
- 靶点鉴定: 证实 GR 是 DTCs 特异性免疫逃逸的关键调控因子,为精准治疗提供全新靶点。
- 治疗策略: 开发 GR 抑制剂与免疫治疗的联合方案,米非司酮的临床应用基础为该策略的转化提供了便利。
文章小结
本研究通过多种基因工程小鼠模型和高通量测序技术,系统阐明了 GR-FAS 轴在 DTCs 转移性播种期免疫逃逸中的核心作用,揭示了 GR 通过阻断 NF-κB 介导的 FAS 表达,抑制免疫细胞介导的凋亡,最终促进转移的分子路径。研究不仅鉴定了 DTCs 特有的免疫逃逸机制,还验证了 GR 抑制剂与免疫治疗联合使用的抗转移效果,为克服 TNBC 转移难题提供了重要的理论支撑和潜在的临床治疗方案。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有11000+细胞产品(含8000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
Rela 结合序列是连接 NF-κB 通路与 GR 通路的关键分子节点,通过调控 Fas 基因表达,成为肿瘤细胞免疫逃逸的 “分子开关”。 如果您也想针对RELA展开研究,源井生物可为您提供RELA基因敲除细胞,涵盖THP-1、A549等细胞系。如果您有个性化基因编辑的需要,欢迎咨询!
联系我们了解更多>>>










