化疗药多柔比星伤心脏?CRISPR筛选锁定RARA/SPNS1双靶点,破解毒性困局!


化疗药多柔比星伤心脏?CRISPR筛选锁定RARA/SPNS1双靶点,破解毒性困局!
标题:CRISPR/Cas9 Screens Implicate RARA and SPNS1 in Doxorubicin Cardiotoxicity
期刊:JACC: CardioOncology IF=12.8
研究单位:宾夕法尼亚大学 。
研究工具:Cas9 稳定表达的心肌细胞系(小鼠永生心肌细胞 HL-1、人心肌细胞系 AC16)及诱导多能干细胞衍生心肌细胞(iCMs) 。
文库类型:全基因组 CRISPR/Cas9 敲除文库(GeCKOv2、Brunello)和靶向 CRISPR 敲除文库(覆盖初筛高置信度靶点,含 7820 条 sgRNA,靶向 952 个基因) 。
筛选策略:研究采用 细胞死亡筛选+DOX 蓄积筛选的双重筛选策略 ,分别通过下一代测序分析 sgRNA 丰度变化,鉴定调控 DOX 诱导细胞死亡的基因,以及流式细胞术分选 DOX 高蓄积(Top15%)和低蓄积(Bottom15%)细胞群,结合测序分析鉴定调控 DOX 摄取、转运或外排的基因。
引言
多柔比星(DOX)作为蒽环类化疗药物的核心成员,在儿童癌症、乳腺癌等多种肿瘤治疗中不可或缺,相关患者 5 年生存率已达 85% 以上。然而,其严重的心脏毒性副作用常导致心力衰竭,极大地限制了临床应用,而背后的分子机制尚未完全明确。近日,宾夕法尼亚大学研究团队在 JACC: CardioOncology 发表重磅研究,他们采用 全基因组及靶向 CRISPR筛选技术 ,以无偏倚的功能基因组学方法系统性挖掘 DOX 诱导心脏毒性的遗传调控因子,首次鉴定出视黄酸受体 α(RARA)和溶血脂转运蛋白 1(SPNS1)为关键调控分子。研究阐明了 RARA 激活可通过保护线粒体功能减轻 DOX 毒性,而 SPNS1 缺失会导致 DOX 在溶酶体异常蓄积并加剧损伤的双重机制,为开发 DOX 心脏毒性防护策略提供了全新靶点和技术框架。

研究背景
DOX 心脏毒性的临床管理一直面临巨大挑战,现有研究对其分子病因和遗传风险因素的理解仍较为有限。尽管已有研究发现部分相关基因和通路,但缺乏大规模、系统性的机制解析。CRISPR筛选技术凭借高特异性和全基因组覆盖能力,成为挖掘疾病关键调控基因的理想工具。本研究聚焦 DOX 诱导的心肌细胞损伤,通过双重筛选策略(细胞死亡调控因子筛选 + DOX 蓄积调控因子筛选),旨在全面鉴定影响 DOX 心脏毒性的遗传修饰因子,解析其调控机制,为临床防护提供理论依据和潜在靶点。
研究目的
采用功能基因组学方法,系统性鉴定 DOX 诱导心脏毒性的遗传修饰因子;明确 RARA 和 SPNS1 调控 DOX 心脏毒性的分子机制;验证 RARA 激活剂及靶向 SPNS1 相关通路对 DOX 心脏毒性的防护效果;建立 DOX 心脏毒性遗传调控的技术框架,为后续治疗靶点发现和遗传生物标志物鉴定提供支撑。
研究方法
细胞模型与筛选体系
构建 Cas9 稳定表达的心肌细胞系(小鼠永生心肌细胞 HL-1、人心肌细胞系 AC16)及诱导多能干细胞衍生心肌细胞(iCMs),作为筛选和验证的核心细胞模型;分别采用全基因组 CRISPR 敲除文库(GeCKOv2、Brunello)和靶向 CRISPR 敲除文库(覆盖初筛高置信度靶点,含 7820 条 sgRNA,靶向 952 个基因)进行筛选。
双重筛选策略
- 细胞死亡筛选 :将转染文库的心肌细胞分为 DOX 处理组(1 μmol/L,72 小时,LD90 剂量)和 DMSO 对照组,通过下一代测序分析 sgRNA 丰度变化,鉴定调控 DOX 诱导细胞死亡的基因;
- DOX 蓄积筛选 :AC16 细胞转染文库后经 DOX 处理(1 μmol/L,24 小时),通过流式细胞术分选 DOX 高蓄积(Top15%)和低蓄积(Bottom15%)细胞群,结合测序分析鉴定调控 DOX 摄取、转运或外排的基因。
功能验证与机制解析
通过 CRISPR-Cas9 技术构建 RARA、SPNS1 敲除细胞系(HL-1、AC16、iPSCs);采用 alamarBlue 法检测细胞活力,流式细胞术、荧光显微镜量化 DOX 蓄积;借助 RNA-Seq 分析基因表达谱变化,聚焦线粒体相关通路;利用 LysoTracker 染色、免疫荧光、Western blot 验证溶酶体功能、自噬 flux 及 DNA 损伤标志物(γ-H2AX);通过时间分辨共聚焦显微镜观察 DOX 蓄积的时空动态。
药理学验证
在 iCMs 中评估 RARA 激动剂他米巴罗汀(TBT)对 DOX 毒性的防护作用;采用雷帕霉素、Torin1 激活自噬,验证自噬通路对 SPNS1 缺失细胞中 DOX 蓄积的影响;在营养剥夺条件下(HBSS 培养基),检测 DOX 蓄积和毒性变化。
研究路线
- 全基因组筛选 :在 HL-1、AC16 细胞中开展 DOX 诱导细胞死亡和 DOX 蓄积的全基因组 CRISPR 筛选,初步鉴定候选调控基因;
- 靶向验证筛选 :在 iCMs 中进行靶向 CRISPR 筛选,聚焦高置信度靶点,明确 RARA 和 SPNS1 的核心调控作用;
- 机制解析 :分别阐明 RARA 调控线粒体功能、SPNS1 调控溶酶体稳态与 DOX 处理的分子机制;
- 药理学验证 :验证 RARA 激动剂、营养剥夺等策略对 DOX 心脏毒性的防护效果。
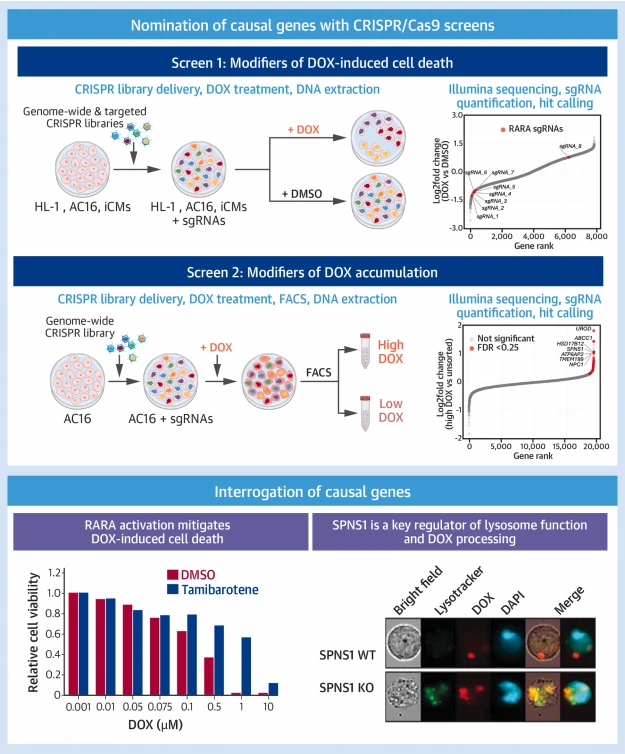
图1. 研究的筛选机制
主要结果
1. 全基因组 CRISPR 筛选鉴定 DOX 细胞死亡调控因子
在 HL-1 细胞中筛选得到 36 个脱敏基因(sgRNA 富集)和 87 个致敏基因(sgRNA 耗竭),其中 DOX 主要靶点 Top2A 缺失是最强脱敏因素(log₂FC=2.1,FDR<0.001),而 DOX 外排转运体 Abcb1b 缺失是最强致敏因素(log₂FC=-1.9,FDR<0.001)。在 AC16 细胞中鉴定出 69 个脱敏基因和 25 个致敏基因,GO 分析显示, 这些基因显著富集于 DNA 损伤应答、凋亡等与 DOX 心脏毒性相关的通路 。通过 MCF7 细胞平行筛选,排除了部分肿瘤细胞特异性调控因子,确保候选基因与心肌细胞 DOX 毒性的相关性。
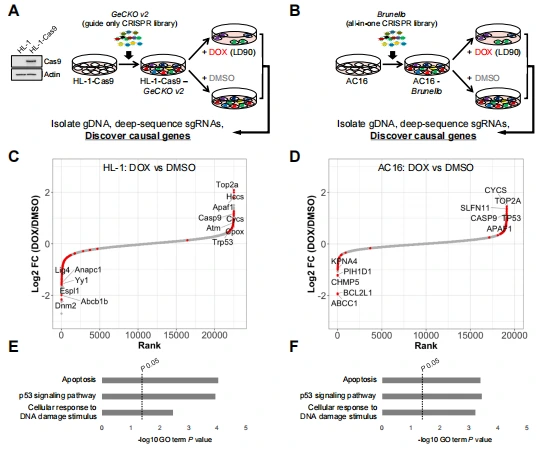
图2.通过全基因组 CRISPR /Cas9基因敲除筛选确定DOX细胞毒性的修饰因子
2. 靶向 CRISPR 筛选验证 RARA 为 DOX 毒性关键调控因子
在 iCMs 中进行靶向筛选,发现 RARA 是最显著的致敏基因 ,其靶向 sgRNA 在 DOX 处理组中显著耗竭。CRISPR 介导的 RARA 敲除(RARA-KO)iCMs 对 DOX 敏感性显著增加,相同剂量下细胞活力显著低于野生型(WT)iCMs。RARA 激动剂他米巴罗汀(TBT)预处理可显著降低 DOX 诱导的 iCMs 死亡,且不影响 DOX 对 MCF7 肿瘤细胞的细胞毒性;TBT 还可减轻 DOX 诱导的 iCMs 肌原纤维紊乱,证实 RARA 激活对心肌细胞的特异性保护作用。
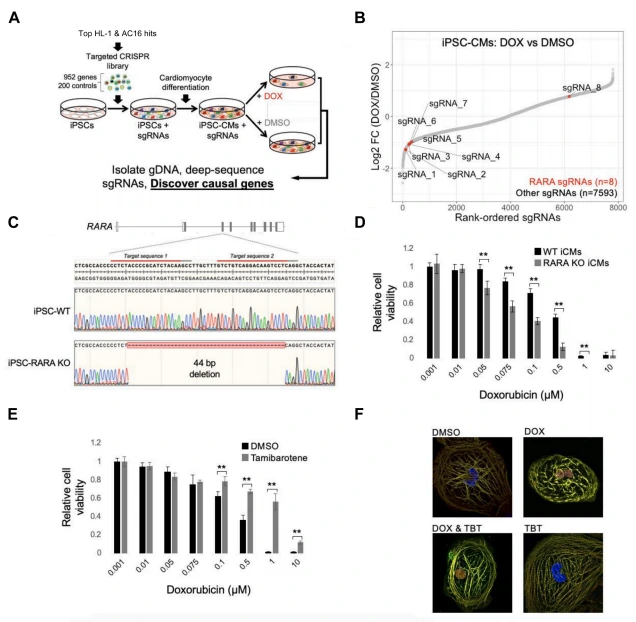
图3.RARA状态作为DOX心脏毒性决定因素的验证
3. RARA 激活通过保护线粒体基因表达减轻 DOX 毒性
RNA-Seq 分析显示,DOX 处理显著下调 iCMs 中线粒体定位蛋白编码基因的表达,而 TBT 与 DOX 联合处理可逆转该抑制效应。主成分分析和火山图显示,TBT 处理可特异性调控 DOX 诱导的转录组变化,尤其是线粒体相关通路,提示 RARA 激活通过缓冲 DOX 介导的线粒体基因表达抑制,改善心肌细胞代谢功能,从而减轻毒性。
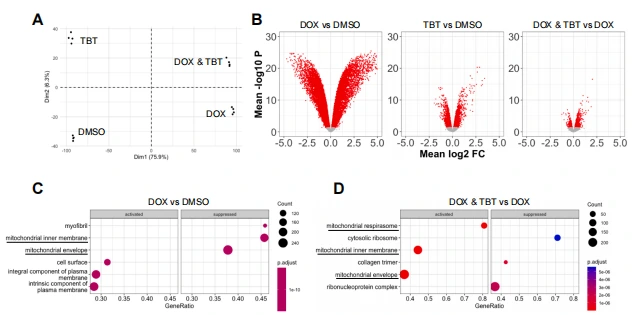
图4.TBT 减轻DOX介导的线粒体基因表达抑制
4. 全基因组筛选鉴定 DOX 蓄积调控因子,聚焦溶酶体功能
DOX 蓄积筛选显示,AC16 细胞中 DOX 荧光强度呈剂量依赖性增加,ABCC1(已知 DOX 外排泵)敲除细胞的 DOX 蓄积显著高于 WT 细胞,验证了筛选体系的可靠性。筛选鉴定出 32 个低 DOX 蓄积相关基因和 23 个高 DOX 蓄积相关基因,GO 分析显示高 DOX 蓄积相关基因主要定位于或调控内体 / 溶酶体功能。SPNS1 作为高 DOX 蓄积组的核心靶点(log₂FC=1.1,FDR<0.001),其功能尚未被报道与 DOX 处理相关。
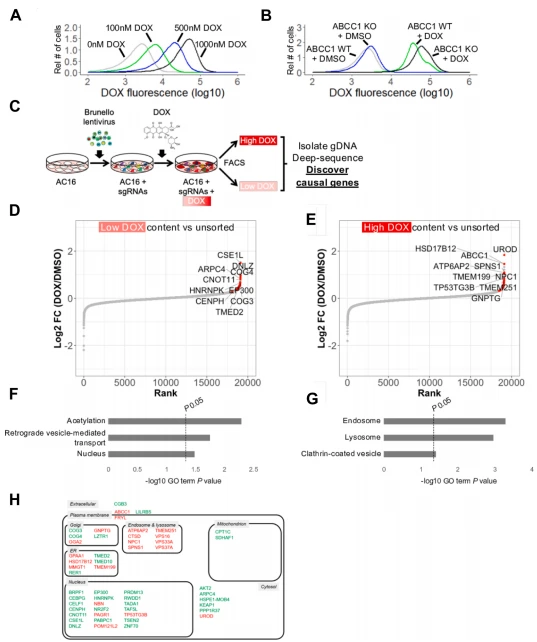
图5.通过全基因组 CRISPR /Cas9敲除筛选发现调控AC16人源心肌细胞中DOX蓄积的因素
5. SPNS1 缺失导致 DOX 异常蓄积并加剧心肌细胞损伤
SPNS1-KO 的 AC16 细胞和 iCMs 中,DOX 蓄积量显著高于 WT 细胞,且蓄积速度更快,大量 DOX 定位于核周体(溶酶体)。LysoTracker 染色证实,SPNS1-KO 细胞中溶酶体数量增加,且与 DOX 显著共定位;SPNS1 缺失还导致自噬 flux 异常(LC3 puncta 增加、LC3-II 积累)和 DNA 损伤加剧(γ-H2AX 表达升高)。在 SPNS1-KO 细胞中,雷帕霉素或 Torin1 激活自噬可进一步增加 DOX 蓄积,而 SPNS1-KO iCMs 对 DOX 毒性的敏感性显著高于 WT 细胞, 证实 SPNS1 介导的溶酶体稳态与自噬耦合是调控 DOX 蓄积和毒性的关键 。
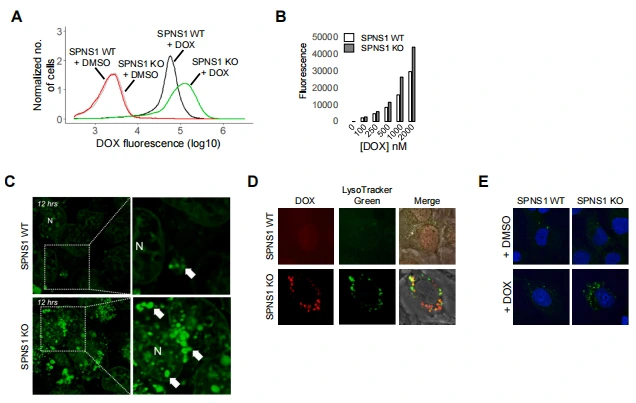
图6.SPNS1作为DOX蓄积调节因子的验证
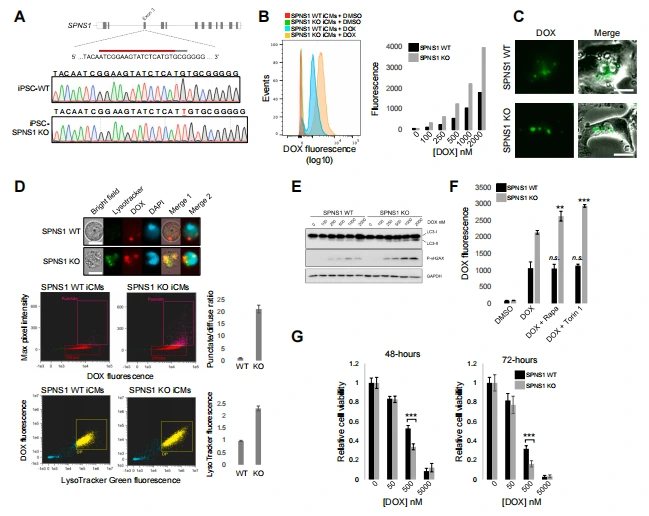
图7.SPNS1缺陷加剧iPSC来源心肌细胞中DOX的蓄积与毒性
6. 核糖体功能缺失与营养剥夺降低 DOX 蓄积和毒性
筛选数据二次分析显示,核糖体生物发生和功能相关基因缺失与 DOX 蓄积减少、细胞存活增加显著相关。营养剥夺条件(HBSS 培养基)下,iCMs 的 DOX 蓄积显著降低,且 DOX 诱导的细胞死亡减少,该效应可通过补充营养逆转,提示营养可用性通过非 mTORC 依赖途径调控 DOX 蓄积和毒性。
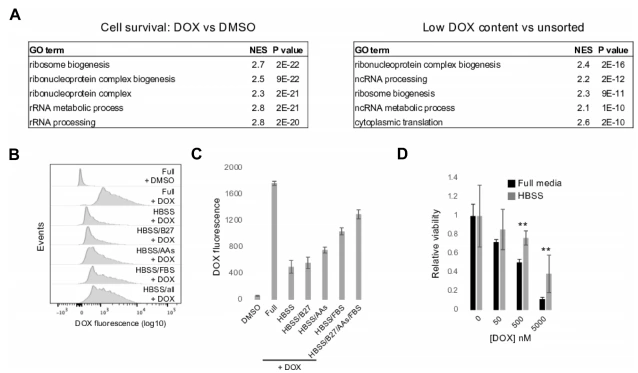
图8.核糖体基因缺失与营养剥夺降低多柔比星(DOX)蓄积及毒性
研究意义与创新点
机制创新
首次通过双重 CRISPR 筛选体系,系统鉴定出 DOX 心脏毒性的两类核心调控因子 ,阐明了 “RARA - 线粒体功能” 和 “SPNS1 - 溶酶体稳态 - 自噬” 两条独立且关键的调控通路,突破了对 DOX 心脏毒性单一机制的认知,揭示了遗传背景对 DOX 响应的重要影响。
靶点与策略创新
鉴定 RARA 为 DOX 心脏毒性的保护性靶点 ,其激动剂他米巴罗汀可特异性保护心肌细胞;明确 SPNS1 作为溶酶体功能调控因子,为开发靶向溶酶体通路的防护策略提供依据;发现 营养剥夺可降低 DOX 蓄积 ,为临床优化给药方案提供新思路。
技术框架创新
建立了 “全基因组筛选 - 靶向验证 - 机制解析 - 药理学验证” 的完整功能基因组学研究框架,为其他化疗药物毒性的遗传调控机制研究提供了可复用的技术范式。
文章小结
本研究通过CRISPR全基因组和靶向筛选,系统性鉴定出RARA和SPNS1为 DOX心脏毒性的关键调控分子,阐明了双重调控机制:RARA 缺失会增强心肌细胞对 DOX 的敏感性,而 RARA 激活可通过保护线粒体基因表达减轻毒性;SPNS1 缺失导致溶酶体稳态失衡,DOX 异常蓄积并抑制自噬,加剧 DNA 损伤和细胞死亡。此外,核糖体功能缺失和营养剥夺可降低 DOX 蓄积,为防护策略提供了补充方向。 研究不仅深化了对 DOX 心脏毒性分子机制的理解,还鉴定了潜在治疗靶点(RARA、SPNS1)和可行防护策略(RARA 激动剂、营养调控),为临床改善 DOX 治疗的安全性提供了重要理论和实验依据。
源井生物CRISPR-iScreen™文库
CRISPR-iScreen™是源井生物自主研发的一项创新技术,旨在实现高效的CRISPR筛选。目前,源井生物拥有 超过40种 的 CRISPR文库现货供应 ,覆盖人类、小鼠、绿猴及猪等物种的全基因组基因敲除/抑制/激活文库;此外,还有针对激酶、细胞周期、膜蛋白、代谢等相关基因构建的CRISPR敲除/抑制/激活亚文库,助您轻松实现靶点筛选!目前源井拥有 150+文库病毒现货 , 文库Cell Pool数量突破600, 还提供 一站式CRISPR文库(体内/体外)功能筛选服务,随时支持您的研究需求。
源井开年特惠,CRISPR文库NGS测序(含分析)低至 ¥1600 ,文库数据分析低至 ¥500 , iScreenAnlys™ 文库分析平台免费使用, Drug-Z/MAGeCK-MLE/MAGeCK-RRA三大算法自由选,筛选数据一键分析,欢迎咨询加速您的研究进程!
引用文献
McDermott-Roe C, Lv W, Shao Y, Hoshino A, Arany Z, Musunuru K. CRISPR/Cas9 Screens Implicate RARA and SPNS1 in Doxorubicin Cardiotoxicity. JACC CardioOncol. 2026 Feb;8(1):48-61. doi: 10.1016/j.jaccao.2026.01.003. PMID: 41705753; PMCID: PMC12922622.











