研究前沿 | 聚焦 LRRC15⁺CAFs!最新研究解析肺癌免疫抑制机制,开发全新靶向疗法


研究前沿 | 聚焦 LRRC15⁺CAFs!最新研究解析肺癌免疫抑制机制,开发全新靶向疗法
引言
肺癌是全球发病率和癌症相关死亡率最高的恶性肿瘤,非小细胞肺癌(NSCLC)占其 85% 左右。免疫检查点阻断(ICB)疗法为耐药和转移性肺癌患者带来获益,但仅适用于小部分患者,开发新型免疫治疗策略迫在眉睫。肿瘤相关成纤维细胞(CAFs)作为肿瘤微环境(TME)核心基质成分,通过细胞外基质(ECM)重塑、生长因子分泌等调控肿瘤进展和免疫逃逸,且具有高度异质性。近日,北京大学朱琳楠研究团队在 Cancer Research 发表最新研究,首次鉴定出 LRRC15⁺ CAFs 为肺癌中肿瘤特异性 CAFs 亚群,揭示 LRRC15 通过调控 CAFs 的 ECM 产生,诱导 M2 型巨噬细胞极化并抑制 CD8⁺T 细胞杀伤功能,最终促进肺癌进展的关键机制;同时开发出靶向 LRRC15 和 TGF-β 的双特异性抗体,可有效下调 CAFs 中 LRRC15 表达并限制肿瘤进展,为肺癌的 CAFs 靶向免疫治疗提供了全新靶点和策略。

研究背景
CAFs 可分为肌成纤维细胞样 CAFs(myCAFs)、炎性 CAFs(iCAFs)等亚型,其中 LRRC15⁺ CAFs 是终末分化的 myCAFs,在胰腺癌、肺癌中均被发现与肿瘤进展、ICB 耐药相关,但其调控肺癌进展的具体分子机制尚未明确,也缺乏针对性的有效治疗手段。LRRC15 属于亮氨酸重复序列超家族,在健康组织中低表达,可能参与 ECM 重塑,但其在 CAFs 中的功能及调控肿瘤免疫微环境的作用亟待阐明。本研究聚焦 LRRC15⁺ CAFs,旨在明确 LRRC15 作为肺癌治疗靶点的潜力,并解析其调控肿瘤免疫的分子机制,开发靶向性治疗策略。
研究目的
鉴定肺癌中具有促肿瘤功能的 CAFs 亚群及关键调控分子,阐明 LRRC15 调控肺癌肿瘤微环境和免疫应答的分子机制,验证 LRRC15 作为肺癌治疗靶点的有效性,并开发基于 LRRC15 的靶向治疗策略,为肺癌免疫治疗提供新方向。
研究方法
临床样本与数据库分析
纳入 14 例经病理确诊的肺癌患者临床样本,整合 12 个肺腺癌相关单细胞 RNA 测序(scRNA-seq)数据集(11 个公共数据集 + 1 个自建数据集)、TCGA、GTEx、GEPIA 等公共数据库,分析 LRRC15⁺ CAFs 的分布、LRRC15 表达与肺癌患者预后的相关性。
动物模型
构建 C57BL/6J、Lrrc15 敲除、成纤维细胞特异性 Lrrc15 条件性敲除(Col1a2-CreER; Lrrc15fl/fl)、M-NSG 等基因工程小鼠,建立 TC1-GFP、LLC、KPS 皮下肿瘤模型及 LLC-Luc 肺转移模型,评估 LRRC15 缺失及靶向抗体治疗对肿瘤生长的影响;利用氯膦酸脂质体耗竭巨噬细胞,验证巨噬细胞在 LRRC15 调控肿瘤进展中的作用。
细胞实验
通过 TGF-β 诱导小鼠肺成纤维细胞、人肺癌患者来源成纤维细胞向 LRRC15⁺ CAFs 分化;利用 CRISPR-Cas9 技术构建 LRRC15-KO 的人 / 鼠 CAFs 细胞系;分离小鼠骨髓来源巨噬细胞(BMDMs)、人外周血单核细胞来源巨噬细胞(mo-MΦs)、小鼠脾脏 CD8⁺T 细胞、人外周血 CD8⁺T 细胞,通过共培养、Transwell、ECM 共培养等实验,验证 LRRC15 对巨噬细胞极化、CD8⁺T 细胞活化的调控作用。
分子机制验证
采用 scRNA-seq、bulk RNA-seq、qPCR、Western blot 检测基因和蛋白表达;通过多重免疫组化(mIHC)、流式细胞术分析肿瘤组织中免疫细胞浸润及表型;利用天狼星红染色、胶原浓度检测实验评估 ECM(胶原)产生;通过免疫荧光验证双特异性抗体的体内靶向性。
治疗验证
设计并制备靶向 LRRC15 和 TGF-β 的双特异性抗体,在 KPS 肺癌小鼠模型中评估该抗体单药治疗的疗效,检测其对肿瘤生长、LRRC15 表达、ECM 沉积及免疫微环境的影响。
研究路线
- 肺癌 CAFs 亚群鉴定:构建人肺基质细胞 scRNA-seq 图谱,鉴定肿瘤富集且与不良预后相关的 CAFs 亚群,筛选其特异性表面分子;
- LRRC15 功能验证:在细胞和动物模型中,证实 LRRC15 缺失可抑制肺癌进展,且该效应依赖于宿主免疫系统;
- 免疫调控机制解析:阐明 LRRC15 通过促进 CAFs 的 ECM 产生,诱导 CD206⁺M2 型巨噬细胞极化,进而抑制 CD8⁺T 细胞的浸润和杀伤功能的分子路径;
- 靶向治疗策略开发:设计靶向 LRRC15 和 TGF-β 的双特异性抗体,验证其在肺癌模型中的治疗效果及安全性。
主要结果
1. LRRC15⁺ CAFs 在肺癌组织中富集,且与患者不良预后相关
通过整合 12 个肺基质细胞 scRNA-seq 数据集,构建包含 26091 个高质量基质细胞的 scRNA-seq 图谱,将成纤维细胞分为 9 个亚群,其中 LRRC15⁺ CAFs(c03)在肺癌组织中显著富集,占肺癌样本中成纤维细胞的约 40%,而在癌旁正常组织中罕见。mIHC 结果显示,肺癌患者肿瘤巢中存在大量 LRRC15⁺α-SMA⁺ CAFs,癌旁组织中几乎无表达。Scissor 分析发现,LRRC15⁺ CAFs 是与肺癌不良预后关联最显著的成纤维细胞亚群,TCGA 数据库分析显示,LRRC15⁺ CAFs 特征基因高表达的肺癌、结直肠癌、胃癌患者总生存期更短,且 LRRC15 基因高表达与肺癌患者不良预后显著相关。此外,LRRC15 在健康组织中低表达,且特异性表达于肺癌 CAFs,在免疫细胞、上皮细胞、内皮细胞中几乎无表达,提示其作为治疗靶点具有良好的特异性和安全性。
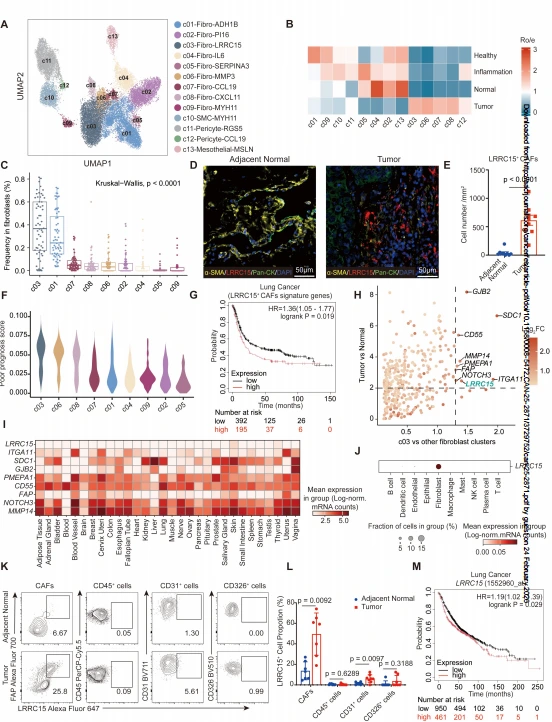
图1. LRRC15+ 间质细胞在肺肿瘤中富集,并与患者预后不良相关
2. LRRC15 缺失以免疫系统依赖的方式抑制肺癌进展
TGF-β 可诱导小鼠肺成纤维细胞上调 LRRC15 表达,分化为 LRRC15⁺ CAF 样细胞。将 TGF-β 诱导的 WT/Lrrc15-KO CAFs 与肺癌细胞共注射至 C57BL/6J 小鼠,结果显示 Lrrc15-KO CAFs 可显著抑制 TC1-GFP、LLC 皮下肿瘤生长,博来霉素联合 TGF-β 处理进一步增强该效应。在 Lrrc15-KO 小鼠及成纤维细胞特异性 Lrrc15 条件性敲除小鼠中,KPS 皮下肿瘤生长显著受抑,LLC-Luc 肺转移灶形成减少,小鼠生存期延长。而在免疫缺陷的 NSG 小鼠中,WT/Lrrc15-KO CAFs 对肿瘤生长的影响无差异,且体外共培养实验中 LRRC15 缺失不影响 CAFs 对肺癌细胞增殖的直接作用,表明 LRRC15 缺失的抑瘤效应依赖于宿主免疫系统。
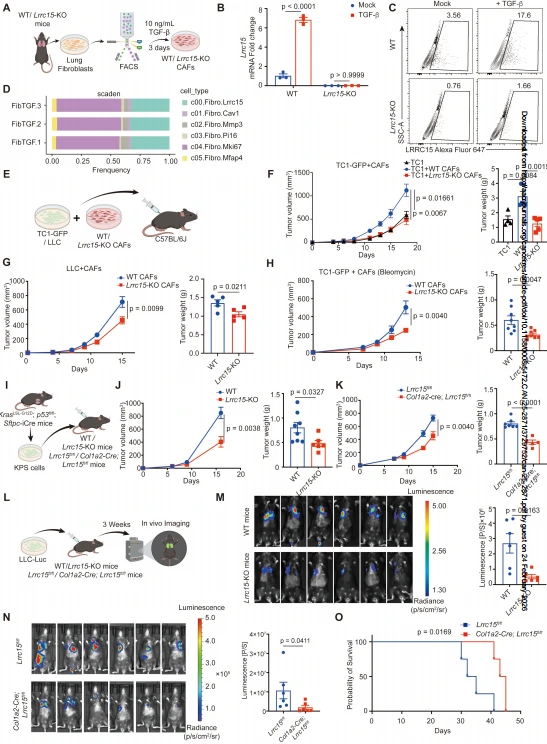
图2. CAF中LRRC15缺失可抑制肿瘤进展
3. LRRC15 缺失重塑肿瘤免疫微环境:促进 CD8⁺T 细胞活化,抑制巨噬细胞 M2 极化
流式细胞术分析显示,Lrrc15-KO CAFs 共注射的肿瘤中 CD45⁺免疫细胞、淋巴细胞浸润增加,其中 CD8⁺T 细胞比例显著升高,且其穿孔素、颗粒酶 B、IFN-γ 的表达水平上调,杀伤功能增强。髓系细胞中,巨噬细胞浸润比例降低,且 CD206⁺M2 型巨噬细胞 / CD206⁻巨噬细胞的比值显著下降。mIHC 验证结果显示,Lrrc15-KO CAFs 组肿瘤中 CD8⁺T 细胞浸润增加,F4/80⁺巨噬细胞浸润减少。TCGA 数据库分析显示,肺癌患者中 LRRC15⁺ CAFs 特征基因表达与 M2 型巨噬细胞特征基因表达呈正相关,且肿瘤组织中 LRRC15⁺ CAFs 密度与 CD68⁺巨噬细胞密度显著正相关,提示 LRRC15 调控肺癌中巨噬细胞与 CD8⁺T 细胞的功能平衡。
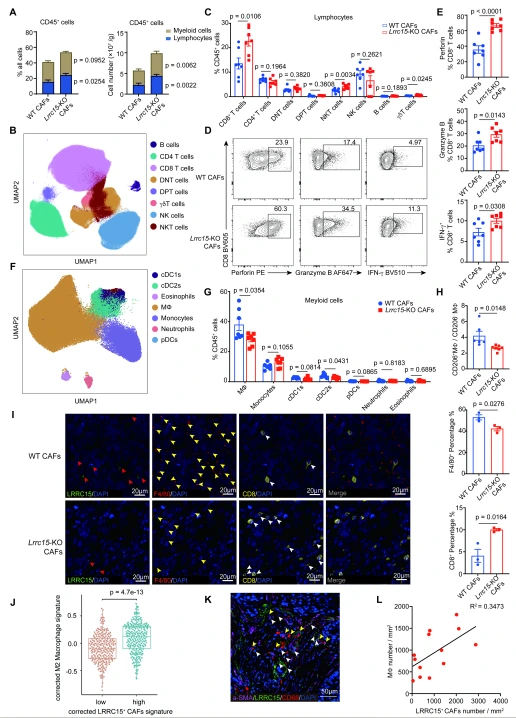
图3. CAFs中LRRC15缺失可诱导CD8+ T细胞数量增加及活化增强,并减少巨噬细胞浸润
4. LRRC15 在 CAFs 中驱动 M2 型巨噬细胞极化,间接抑制 CD8⁺T 细胞活化
体外共培养实验显示,WT CAFs 可显著增加 BMDMs、mo-MΦs 中 CD206⁺细胞的数量和比例,而 Lrrc15/LRRC15-KO CAFs 则几乎完全消除该效应;肿瘤来源的 Lrrc15-KO LRRC15⁺ CAFs 也可显著抑制 BMDMs 向 M2 型极化。巨噬细胞耗竭实验显示,氯膦酸脂质体耗竭巨噬细胞后,Lrrc15 条件性敲除的抑瘤效应被完全逆转,证实巨噬细胞是 LRRC15 调控肺癌进展的关键介质。此外,CAFs 与 CD8⁺T 细胞直接共培养时,LRRC15 缺失不直接影响 CD8⁺T 细胞活化,但与 Lrrc15-KO CAFs 预培养的巨噬细胞可显著促进 CD8⁺T 细胞增殖及颗粒酶 B、IFN-γ 的表达,表明 LRRC15 通过调控巨噬细胞极化间接抑制 CD8⁺T 细胞功能。
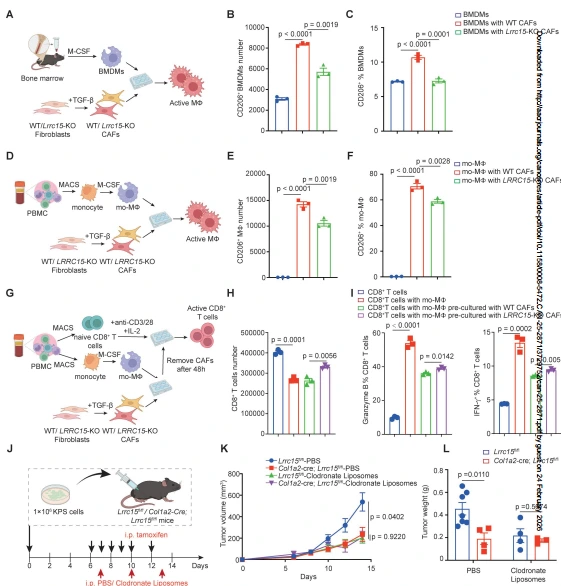
图4. LRRC15在成纤维细胞中驱动M2巨噬细胞极化以抑制CD8+T细胞活化
5. LRRC15 通过促进 CAFs 的 ECM 产生调控 M2 型巨噬细胞极化
Bulk RNA-seq 及 GO 分析显示,与 LRRC15-KO CAFs 相比,WT CAFs 中 ECM 相关通路显著富集,且肺癌患者中 LRRC15 表达与 ECM 相关基因表达呈正相关,人、鼠 LRRC15⁺ CAFs 均高富集 ECM 组织化通路。天狼星红染色、胶原浓度检测、Western blot 结果显示,LRRC15 缺失可显著降低人、鼠 CAFs 的胶原(COL1A1)产生,且 Lrrc15 条件性敲除小鼠的 KPS 肿瘤中 ECM 密度显著降低。将巨噬细胞接种于 CAFs 脱细胞 ECM 上,结果显示 Lrrc15/LRRC15-KO CAFs 的 ECM 可显著减少 CD206⁺巨噬细胞的数量和比例。Transwell 实验及细胞因子中和实验证实,LRRC15 调控巨噬细胞极化不依赖可溶性细胞因子,而依赖 CAFs 与巨噬细胞的直接接触;外源性补充胶原 I 可显著增加 CD206⁺巨噬细胞比例,证实 LRRC15 通过促进 CAFs 的 ECM(胶原 I)产生诱导 M2 型巨噬细胞极化。
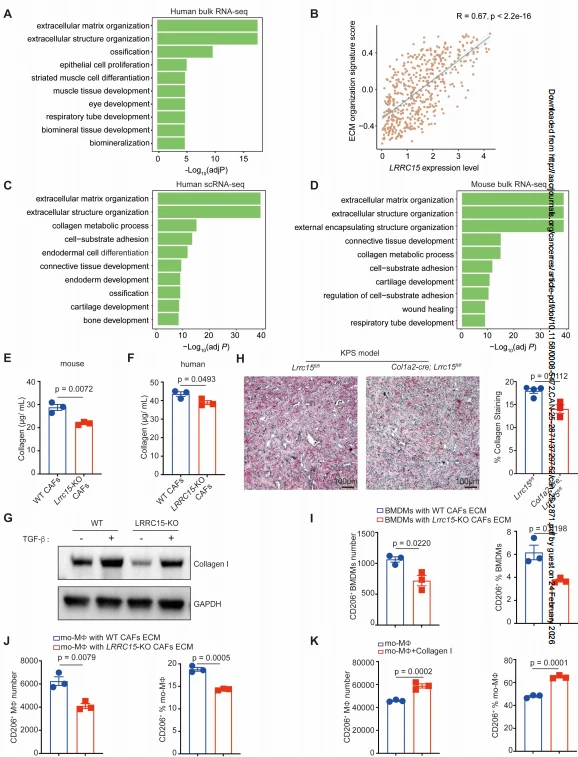
图5. LRRC15通过调节细胞外基质的产生促进M2型巨噬细胞极化
6. 靶向 LRRC15 和 TGF-β 的双特异性抗体有效抑制肺癌进展,且安全性更佳
制备的抗 LRRC15 抗体(Abio-1)对人、鼠 LRRC15 均具有高亲和力,基于 TGF-β 调控 LRRC15⁺ CAFs 分化的机制,设计靶向 LRRC15 和 TGF-β 的双特异性抗体,体内示踪显示该抗体可特异性富集于肿瘤组织中的 LRRC15⁺ CAFs,在免疫细胞、肿瘤细胞中几乎无结合。KPS 肺癌模型中,该双特异性抗体可显著抑制肿瘤生长,疗效与 TGF-βRII 抗体相当,而单独抗 LRRC15 抗体无明显抑瘤效应。与 TGF-βRII 抗体导致小鼠脾肿大(全身 TGF-β 阻断副作用)不同,双特异性抗体无此现象,提示其可通过 LRRC15 靶向性阻断肿瘤局部 TGF-β 信号,安全性更高。此外,双特异性抗体治疗可显著降低肿瘤中 LRRC15⁺ CAFs 的 LRRC15 表达水平(无 CAFs 消除),并减少肿瘤 ECM 沉积;在免疫缺陷 NSG 小鼠中,该抗体无抑瘤效应,证实其疗效依赖于免疫系统。
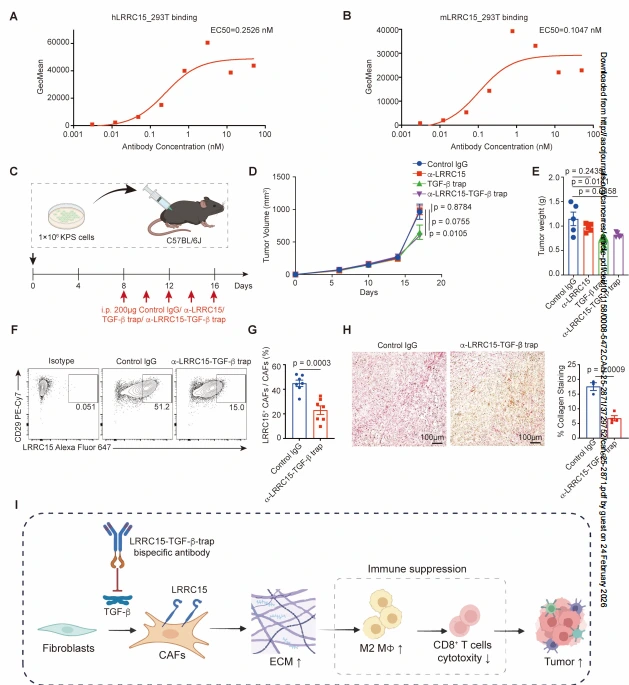
图6. 靶向LRRC15阳性癌相关成纤维细胞可抑制肿瘤进展
研究意义与创新点
机制创新
首次系统解析了 LRRC15⁺ CAFs 调控肺癌肿瘤免疫微环境的分子机制,明确 LRRC15 通过促进 CAFs 的 ECM 产生,诱导 M2 型巨噬细胞极化,进而抑制 CD8⁺T 细胞的浸润和杀伤功能,揭示了 CAFs-ECM - 巨噬细胞 - CD8⁺T 细胞的调控轴在肺癌进展中的核心作用,拓展了对 CAFs 异质性及功能调控的认知。
靶点鉴定
首次证实 LRRC15 是肺癌中肿瘤特异性 CAFs 的功能驱动分子,其在健康组织中低表达、特异性表达于 LRRC15⁺ CAFs 的特征,使其成为肺癌治疗的理想靶点,为肺癌的精准靶向治疗提供了新的分子靶点。
治疗策略
开发出靶向 LRRC15 和 TGF-β 的双特异性抗体,该抗体可特异性靶向肿瘤组织中的 LRRC15⁺ CAFs,下调 LRRC15 表达并减少 ECM 沉积,有效抑制肺癌进展,且避免了全身 TGF-β 阻断的副作用,为肺癌的 CAFs 靶向免疫治疗提供了全新的可行策略,也为其他实体瘤的 CAFs 靶向治疗提供了参考。
文章小结
本研究通过构建人肺基质细胞 scRNA-seq 图谱,鉴定出 LRRC15⁺ CAFs 为肺癌中肿瘤富集、与不良预后相关的特异性 CAFs 亚群,并证实 LRRC15 是该亚群的功能核心分子。本研究不仅揭示了 CAFs 调控肺癌免疫的新机制,更鉴定了一个极具潜力的肺癌治疗靶点,并开发出针对性的靶向治疗策略,为克服肺癌免疫治疗耐药、提升治疗效果提供了重要的理论和实验依据。
源井生物基因编辑服务
源井生物一直秉持“让基因编辑更简单”的核心理念,持续迭代产品与服务,已累计实现 13000+ 基因编辑成功案例,拥有 11000+ 细胞产品(含 8000+ KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升 10-20 倍。目前源井生物已为超 10000 个生命科学实验室、药企和 CRO 公司提供优质的基因编辑服务与产品。
LRRC15 是一种参与细胞-细胞和细胞-基质相互作用的 I 型跨膜蛋白,被发现与肿瘤细胞的增殖、迁移和侵袭密切相关。如果您也想针对 LRRC15 展开研究,源井生物可为您提供 LRRC15 基因敲除细胞,涵盖 U-87 MG、Ishikawa 等肿瘤细胞系。如果您有个性化基因编辑的需要, 欢迎咨询!
引用文献
Qi L, Dang G, Ling X, Miao Y, Bo Y, Zhai Y, Chen X, Zhai Q, Zheng L, Zhang Y, Li Y, Liu C, Fan H, Si W, Tong D, Yang Z, Hu X, Wang D, Cheng S, Zhang Z, Zhu L. Targeting LRRC15 in Cancer-Associated Fibroblasts Modifies the Extracellular Matrix and Enhances Tumor Immune Responses to Suppress Lung Cancer Progression. Cancer Res. 2026 Jan 27. doi: 10.1158/0008-5472.CAN-25-2871. Epub ahead of print. PMID: 41591362.











