破解免疫 “线粒体密码”!OPA1-NRF1 轴掌控树突状细胞抗肿瘤免疫力


引言
I 型常规树突状细胞(cDC1s)是调控 CD8+T 细胞抗肿瘤免疫的关键细胞,但其在肿瘤微环境中易发生代谢应激与功能损伤,线粒体代谢对其功能的调控机制尚不明确。 美国圣犹大儿童研究医院 Hongbo Chi 团队 在 Science 发表研究,首次发现肿瘤内 cDC1s 存在两种线粒体状态, OPA1-NRF1 信号轴 通过维持线粒体氧化磷酸化、能量代谢与氧化还原平衡,决定 cDC1s 抗原呈递与抗肿瘤免疫功能,且高线粒体极化 cDC1s 联合免疫检查点阻断可显著增强抗肿瘤效果。

研究背景
cDC1s 是驱动 CD8+T 细胞活化、决定免疫检查点阻断治疗效果的核心抗原呈递细胞,但在肿瘤微环境中常出现代谢紊乱与功能下降。既往研究认为线粒体氧化磷酸化对树突状细胞成熟非必需,甚至与免疫耐受相关, 线粒体代谢如何调控肿瘤微环境中 cDC1s 的抗肿瘤功能, 仍是待解决的关键科学问题。
研究方法
- 动物模型与基因编辑: 构建 DC 特异性 OPA1/DRP1 敲除、cDC1 特异性 OPA1 敲除等小鼠模型,建立多种小鼠肿瘤模型。
- 细胞分析: 流式分选 cDC1s,检测线粒体膜电位与质量,划分功能亚群。
- 功能实验: 抗原呈递实验、Seahorse 线粒体呼吸检测、免疫印迹等。
- 多组学分析: 蛋白质组学、代谢组学、ATAC-seq、转录组测序。
- 治疗验证: 回输高 / 低线粒体极化 cDC1s,联合免疫检查点抑制剂评估抗肿瘤效果。
研究路线
- 临床 / 体内发现: 人 / 小鼠肿瘤 cDC1s 存在两种线粒体状态,高极化亚群功能更强。
- 关键因子鉴定: OPA1 调控 cDC1s 线粒体形态与抗肿瘤功能。
- 机制解析: OPA1 通过 NRF1 维持氧化磷酸化,抑制自噬并平衡氧化还原状态。
- 动态变化: 肿瘤进展导致 cDC1s 进行性线粒体功能障碍。
- 逆转验证: 敲除 DRP1 可恢复 OPA1 缺失导致的功能缺陷。
- 转化应用: 高极化 cDC1s 联合免疫检查点阻断实现强效抗肿瘤免疫。
主要结果
1.OPA1 调控 cDC1 线粒体状态与抗肿瘤 CD8+T 细胞应答
肿瘤内 cDC1 存在 [TMRM/MG]hi(高线粒体极化)与[TMRM/MG]ˡᵒ(低极化)两个亚群,前者激活 CD8+T 细胞能力更强。蛋白质组显示肿瘤 cDC1 线粒体嵴形成通路显著上调,OPA1特异性高表达。DC 特异性敲除 OPA1 后,cDC1 线粒体碎片化、膜电位下降,多种肿瘤生长加快。OPA1 缺失导致肿瘤浸润 CD8+T 细胞数量与效应功能显著降低,且该作用具有肿瘤特异性,不影响抗病毒免疫。cDC1 特异性敲除 OPA1 即可重现表型,证实OPA1 在 cDC1 中发挥必需作用。
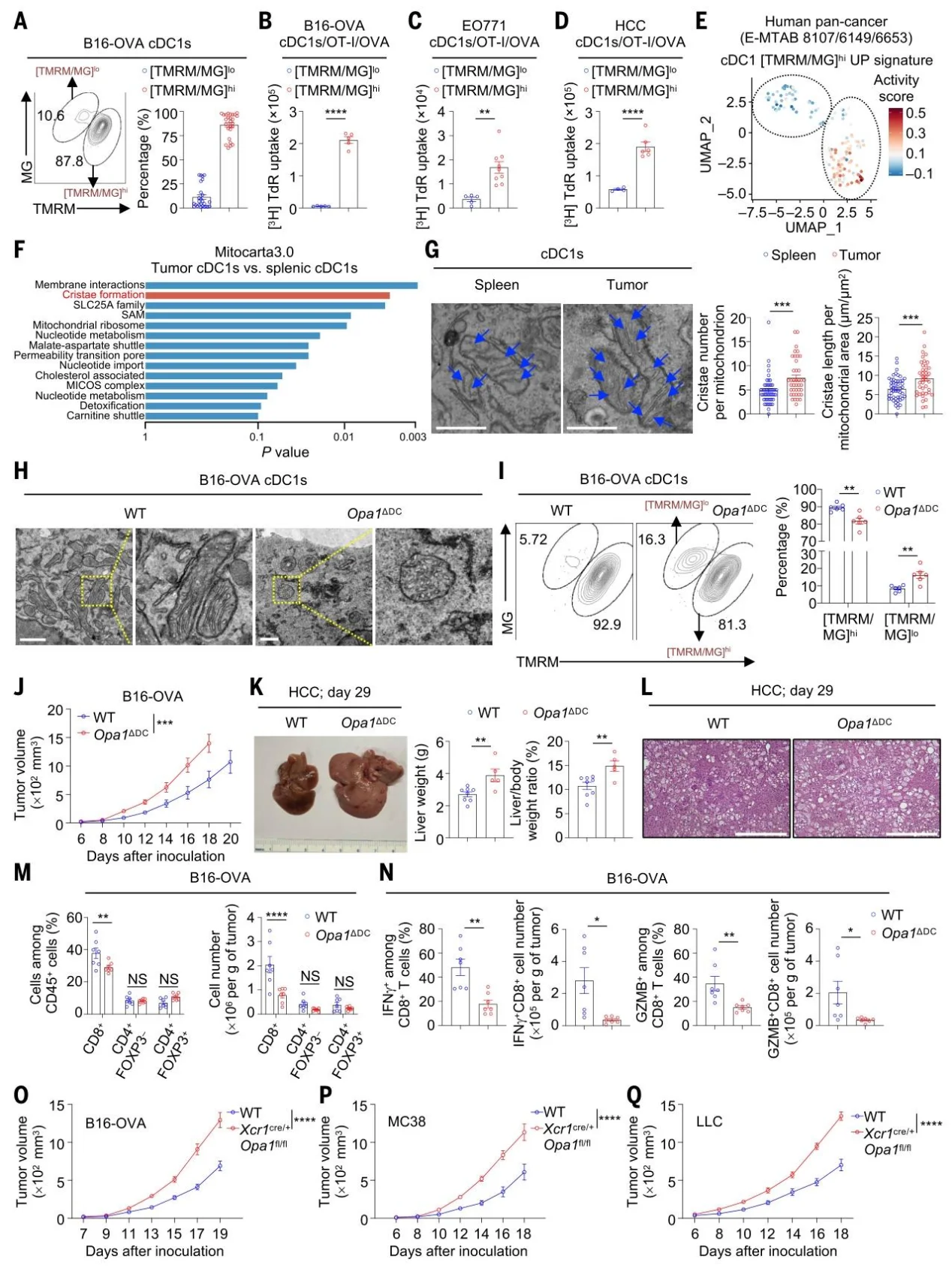
图1.OPA1调控cDC1s的离散线粒体状态及其在激活抗肿瘤CD8+ T细胞应答中的功能。
2.OPA1-NRF1 轴介导的 OXPHOS 促进 cDC1 抗原呈递
OPA1 缺失特异性降低 cDC1 表面 MHC-I - 抗原复合物水平,不影响共刺激分子与细胞因子。ATAC-seq 与转录组显示,OPA1 缺失导致NRF1转录活性与表达显著下降。NRF1 敲除降低线粒体 OXPHOS,并损伤 cDC1 抗原呈递功能;过表达 NRF1 可部分挽救 OPA1 缺失表型。OPA1-NRF1 通路调控线粒体呼吸链复合物 I-V 表达,ETC 完整性是 cDC1 功能必需。抑制 ETC 复合物可消除 OPA1/NRF1 对 cDC1 功能的影响,证实 OXPHOS 为核心下游环节。
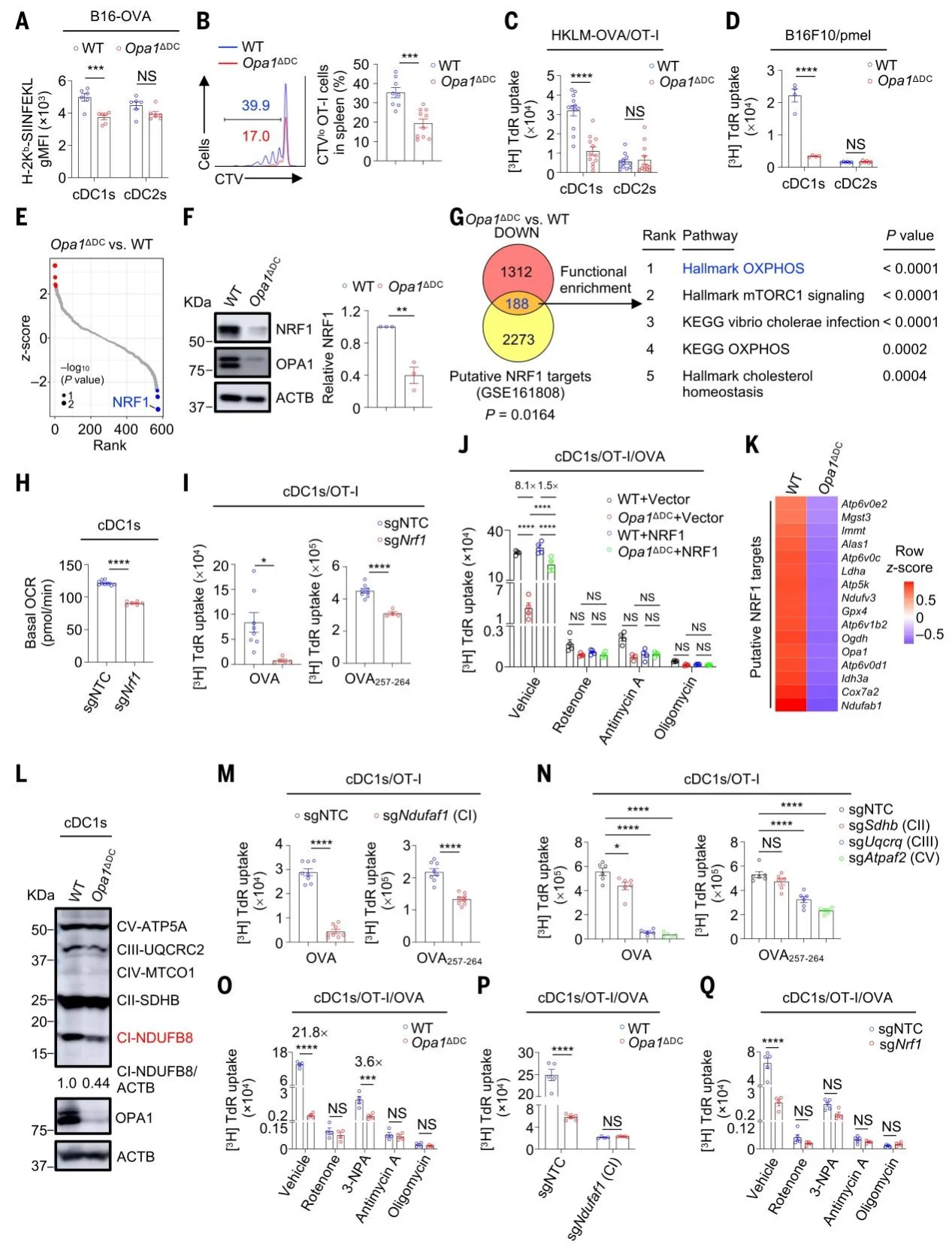
图2.OPA1-NRF1轴介导的 OXPHOS 促进cDC1抗原呈递。
3.线粒体 OXPHOS 抑制自噬及 NAD⁺平衡维持 cDC1 功能
OPA1/NRF1 缺失导致 ATP 下降、AMPK 激活,自噬通路显著上调。自噬增强导致 MHC-I 与抗原被溶酶体降解,抑制自噬可恢复抗原呈递。OPA1 缺失破坏 ETC 导致NAD⁺/NADH 失衡,恢复 NAD⁺可部分挽救 cDC1 功能。敲除线粒体分裂蛋白 DRP1,可逆转 OPA1 缺失导致的线粒体损伤、自噬升高与肿瘤进展。线粒体融合 - 分裂平衡是 cDC1 代谢与免疫功能的关键调控点。
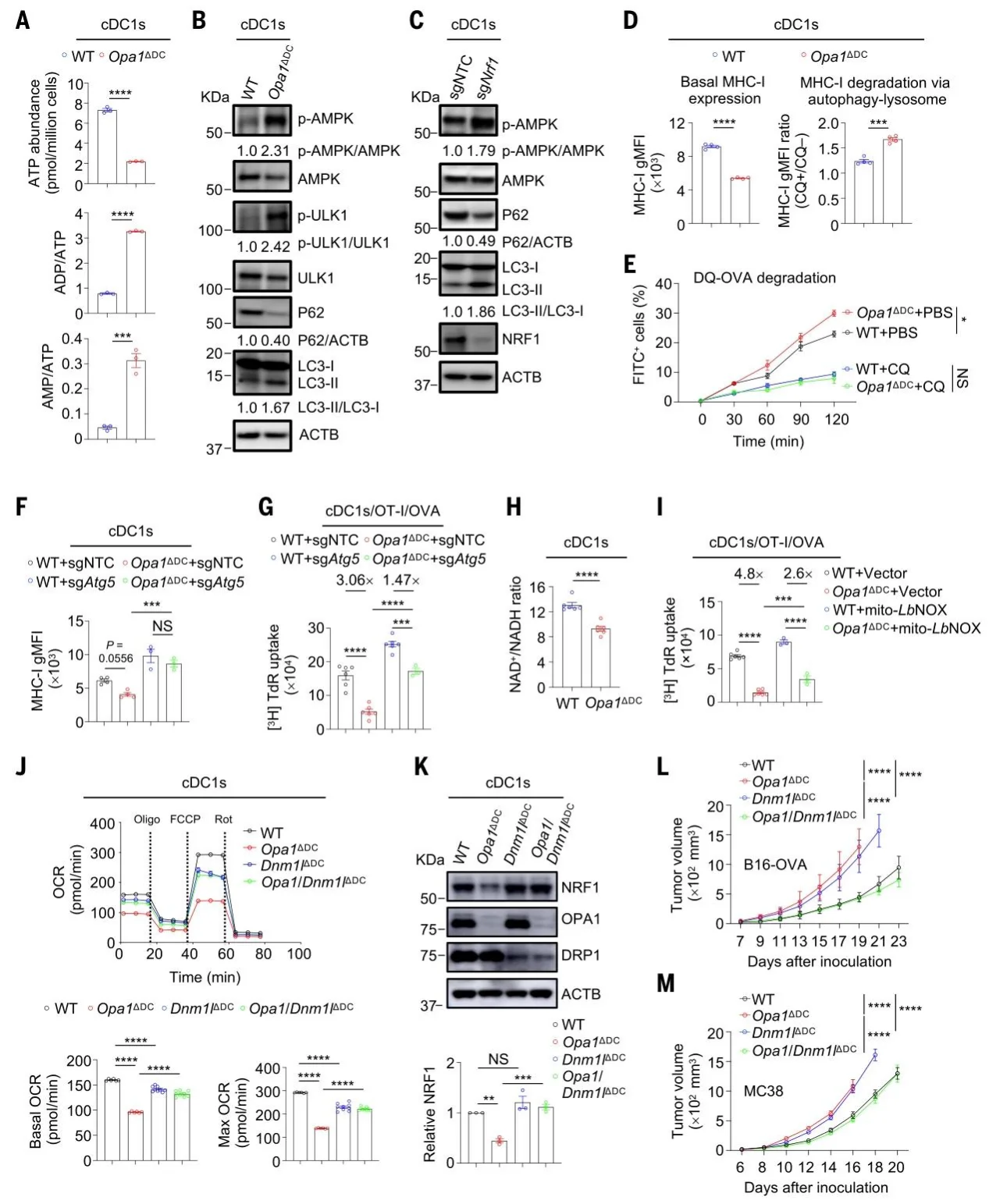
图3.线粒体 OXPHOS 驱动的自噬抑制与NAD+再生共同促进OPA1介导的cDC1功能适应性。
4.肿瘤进展导致 cDC1 线粒体进行性功能障碍
随肿瘤进展,cDC1 的 [TMRM/MG]hi亚群比例、线粒体膜电位与体积持续下降。OPA1、NRF1 蛋白水平与信号活性随肿瘤进展显著下调。肿瘤微环境直接导致 cDC1 线粒体功能受损,与肿瘤细胞线粒体转移无关。过继回[TMRM/MG]hi cDC1 可显著抑制肿瘤,联合 ICB(抗 PD-L1/PD-1/CTLA-4)可完全清除肿瘤并建立长期免疫记忆。
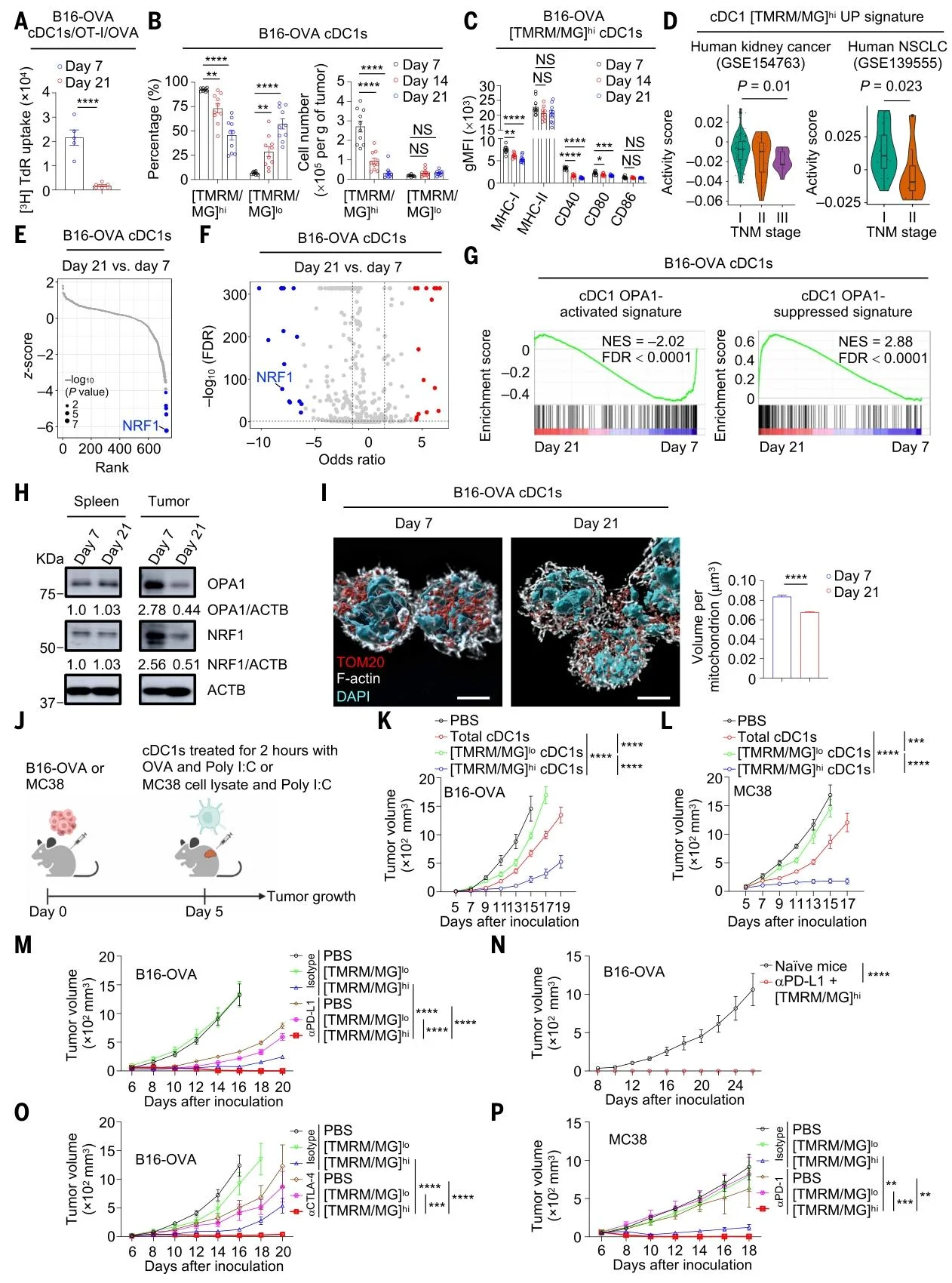
图4.肿瘤内cDC1细胞在肿瘤进展过程中经历线粒体膜电位和体积的进行性下降,这一现象与OPA1和NRF1水平的下调相关。
研究意义与创新点
- 理论创新: 首次揭示肿瘤微环境中 cDC1s 线粒体状态异质性,阐明 OPA1-NRF1 - 氧化磷酸化轴的核心调控作用。
- 机制突破: 发现线粒体代谢通过抑制自噬维持 MHC-I 稳定、调控氧化还原平衡的双重机制。
- 转化价值: 提出高线粒体极化 cDC1s 联合免疫检查点阻断的治疗新策略。
- 靶点明确: 锁定 OPA1、NRF1、DRP1 为 cDC1s 代谢改造核心靶点。
文章小结
本研究发现 OPA1-NRF1 信号轴通过维持线粒体氧化磷酸化、能量代谢与氧化还原平衡,抑制自噬介导的 MHC-I 降解,保障 cDC1s 抗原呈递与抗肿瘤免疫功能;肿瘤进展会引发 cDC1s 进行性线粒体功能障碍,而回输高线粒体极化 cDC1s 可协同免疫检查点阻断,触发强效持久的抗肿瘤免疫,为代谢工程化改造树突状细胞、优化肿瘤免疫治疗提供全新理论与策略。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有10000+KO细胞产品,自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
OPA1 的主要功能是调控线粒体的融合过程,这对于维持线粒体的正常形态和功能至关重要 线粒体不仅是细胞的能量工厂,还参与多种细胞过程,如 apoptosis(细胞凋亡)和 calcium homeostasis(钙稳态)。如果您也想针对 OPA1 展开研究,源井生物可为您提供 OPA1基因敲除 服务,欢迎咨询!
联系我们了解更多>>>










