膜蛋白CRISPR文库筛选:高效挖掘疾病潜在靶点的核心策略


一、膜蛋白CRISPR文库是什么?
膜蛋白广泛分布于细胞膜与细胞器膜,约占人类蛋白质组的25%,在细胞感知外界信号、胞间通讯与信号转导中发挥关键作用。其表达异常与肿瘤发生、发展、增殖及转移密切相关,是当前药物研发与基础科研的核心靶点。 CRISPR文库凭借低成本、高通量、高重复性等优势,已成为靶点筛选的主流工具。基于膜蛋白我们可以构建敲除、激活或抑制文库,通过膜蛋白CRISPR文库筛选,能高效挖掘疾病治疗的潜在靶点。 那么,膜蛋白CRISPR文库究竟如何筛选出潜在靶点?小源用真实案例为你揭秘膜蛋白文库是如何适配多种应用场景,让你轻松读懂这一科研核心技术。
二、膜蛋白CRISPR文库筛选逻辑
膜蛋白CRISPR文库筛选的核心逻辑就是:通过CRISPR技术调控膜蛋白基因的表达(敲除、激活或抑制),观察细胞表型的变化,进而锁定与疾病相关的关键膜蛋白靶点——直白讲,就是“逐个调控膜蛋白,看哪个膜蛋白的变化会影响疾病进程”。
具体流程主要分为4个关键步骤,每一步都环环相扣,确保筛选的准确性和高效性。
第一步,文库导入与细胞感染
将构建好的膜蛋白CRISPR文库,通过病毒载体(如慢病毒)感染目标细胞(通常为疾病相关细胞,如肿瘤细胞),确保每个细胞都只被一个gRNA感染,即每个细胞只针对一个膜蛋白基因进行调控。这个过程就像给每个细胞分配一个“专属工具”,让它们各自负责调控一个膜蛋白。
第二步,筛选压力施加与细胞培养
根据研究目的施加筛选压力,模拟疾病相关的生理或病理环境,让被调控膜蛋白基因的细胞出现差异化存活或表型变化。比如,筛选肿瘤治疗靶点时,可施加化疗药物压力,此时若某个膜蛋白被敲除/激活后,肿瘤细胞出现凋亡、增殖受阻,说明该膜蛋白可能与肿瘤耐药或增殖相关,是潜在靶点。随后,将感染后的细胞进行长时间培养,让表型差异充分显现。
第三步,阳性细胞富集与测序分析
通过流式细胞术、筛选标记等方式,将表现出目标表型(如存活、凋亡、迁移能力变化)的“阳性细胞”分离出来,这些细胞中含有的gRNA,对应的膜蛋白基因就是潜在靶点。之后,对这些阳性细胞中的gRNA进行高通量测序,统计每个gRNA的富集程度——富集程度越高,说明该gRNA靶向的膜蛋白基因,与筛选表型的关联性越强,成为核心靶点的可能性越大。
第四步,靶点验证与确认
这是筛选的关键收尾步骤,也是确保靶点可靠性的核心。针对测序筛选出的高关联膜蛋白靶点,通过单独构建该基因的CRISPR调控体系,在不同细胞系或动物模型中重复验证,确认该膜蛋白的表达变化确实能调控疾病相关表型(如肿瘤细胞增殖、信号通路激活等)。
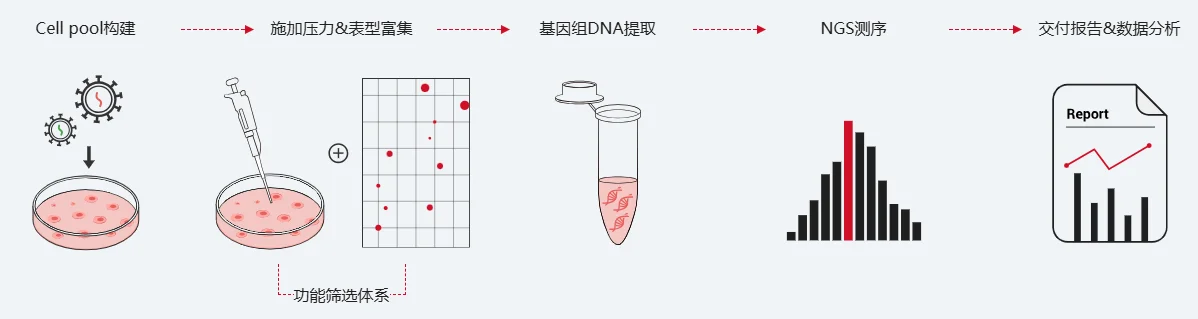
CRISPR文库筛选流程
三、鼠膜蛋白激活文库筛选发现促肿瘤细胞转移靶点Lrrn4cl
黑色素瘤在所有皮肤恶性肿瘤中占比约5%,但是由于其易转移的特点,致死率高达70%以上。为了寻找出黑色素瘤转移相关基因,Adams等人使用小鼠膜蛋白激活文库构建B16-F0文库细胞,并通过尾静脉注射入裸鼠后,于第19天收集肺转移肿瘤细胞(图1)。经NGS测序分析肺转移肿瘤组织与对照组sgRNA差异,研究者发现Lrrn4cl基因被显著富集(表1)。
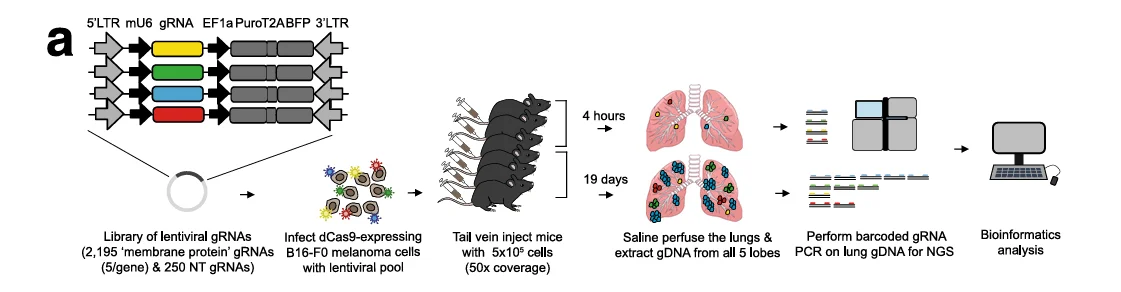
图1 小鼠膜蛋白激活文库筛选促进肿瘤细胞肺转移基因
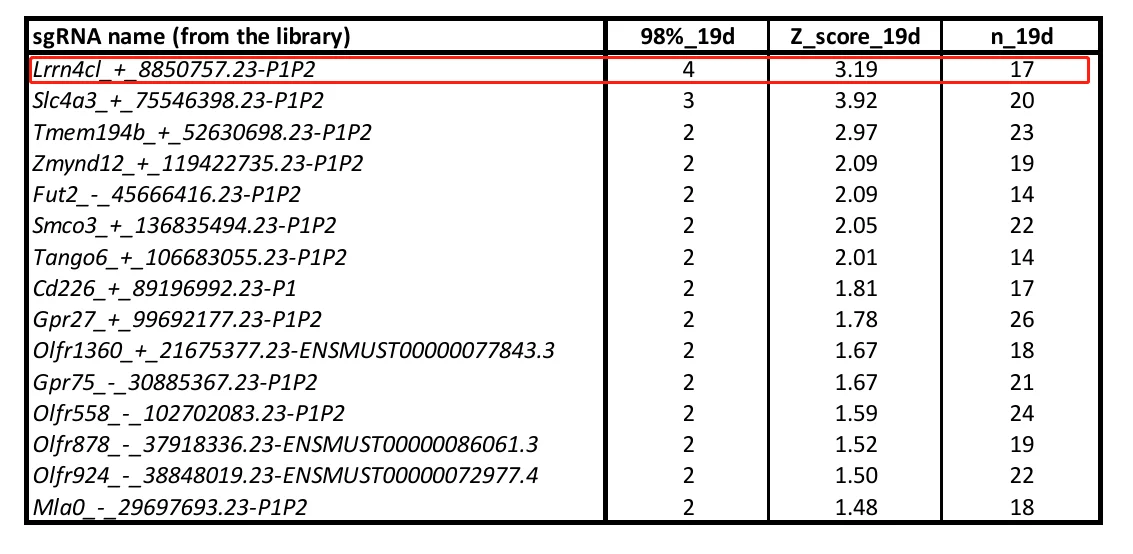
表1 肺肿瘤组织中sgRNA富集分析
为了确认Lrrn4cl基因促进肿瘤转移的作用,研究者们在三种不同的小鼠黑色素瘤细胞系(图2 a)以及另外三种不同肿瘤细胞系(图2 b)中分别过表达该基因后,发现这些细胞的肺转移定植能力均显著上调。除此之外,使用膜蛋白激活文库对E0771-dCas9细胞进行筛选后,富集程度最高的同样是Lrrn4cl基因(数据未展示),进一步说明该基因对肿瘤细胞肺转移定植的重要性。
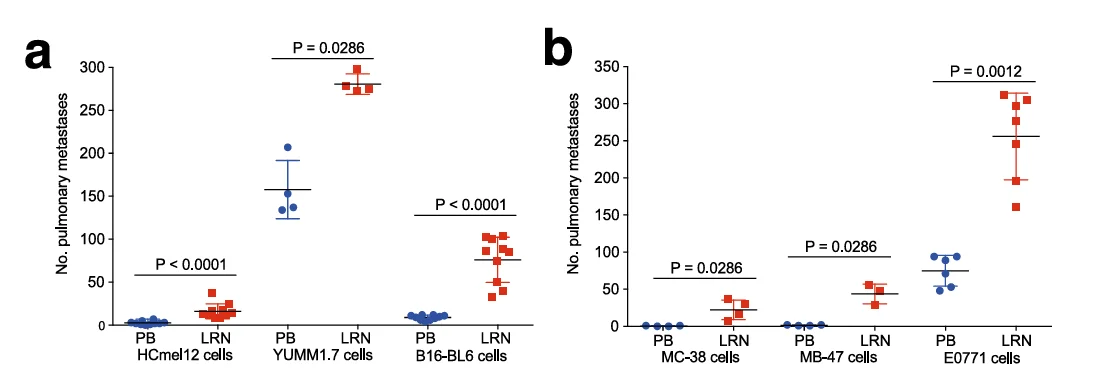
图2 不同细胞系中过表达Lrrn4cl基因均能促进其肺转移定植能力
四、人膜蛋白激活文库筛选发现TMX2促进HCC细胞增殖
原发性肝癌是第六大常见癌症类型,也是导致癌症相关死亡的第三大原因。作为原发性肝癌的主要组织学类型,肝细胞癌(HCC)占肝癌诊断和死亡的绝大多数。Zhang等人使用人膜蛋白激活文库感染HCC细胞后,持续对其进行传代培养,并比较D1和D14天文库细胞中sgRNA差异(图3)。
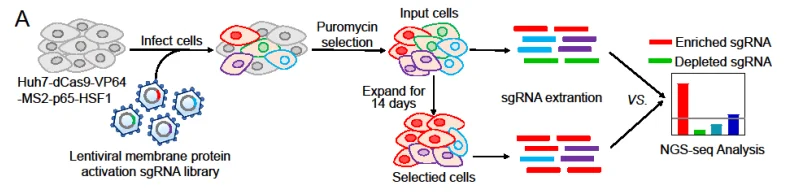
图3 人膜蛋白激活文库筛选促HCC细胞增殖基因
分析发现TMX2基因在正向筛选中显著富集;同时,一项使用全基因组敲除文库筛选HCC细胞的研究中,TMX2基因在负向筛选中也被显著富集(图4)。这些结果说明TMX2可能在HCC细胞活力中发挥关键作用。
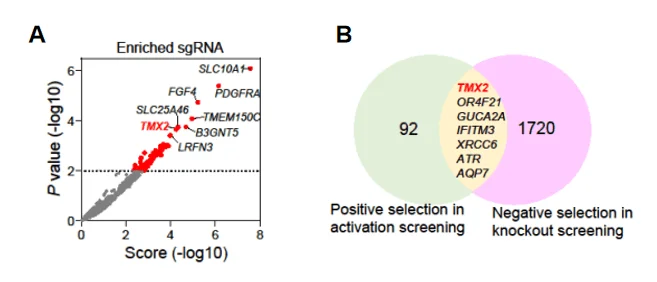
图4 TMX2基因被显著富集
为了确认TMX2基因对HCC细胞活力的影响,研究者在不同的HCC细胞系中进行了基因敲低和过表达实验,发现TMX2基因敲低后HCC细胞的克隆形成能力显著降低,而过表达则会显著增加HCC细胞的增殖能力(图5)。
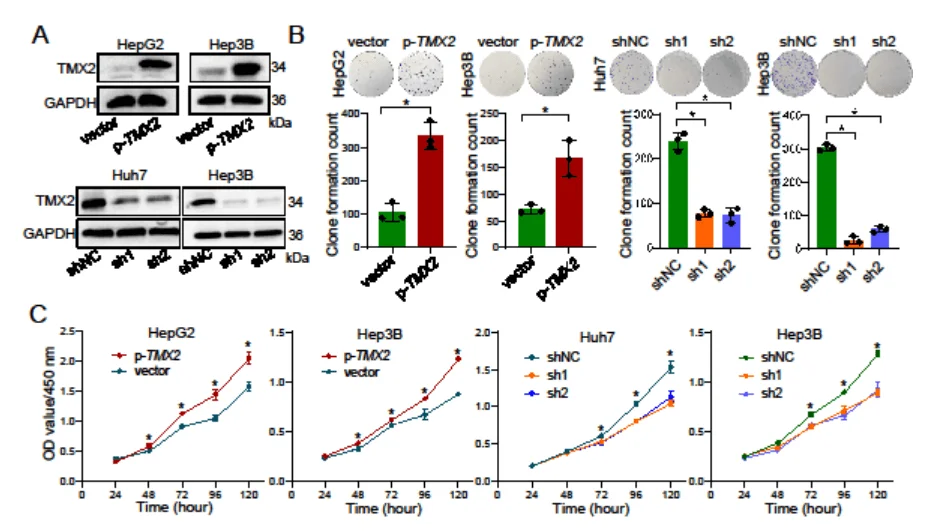
图5 不同HCC细胞中敲低或过表达TMX2基因
进一步探究TMX2基因促进HCC细胞增殖的机制,研究者们通过比较TCGA(The Cancer Genome Altas Program)数据库中TMX2高表达和低表达样本间差异,发现TMX2高表达样本中,与自噬相关基因明显富集。通过RT-qPCR检测也发现,敲低TMX2基因后,自噬相关基因表达量均显著下调(图6)。
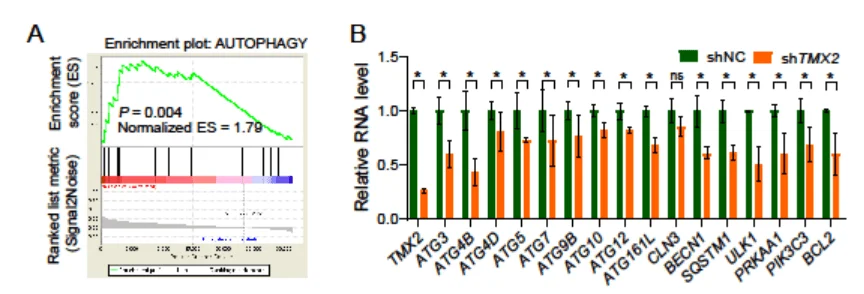
图6 TMX2基因调控细胞自噬水平
通过co-IP,免疫荧光等实验深入研究TMX2调控自噬的机制,发现TMX2通过调控KPNB1蛋白的核质比来调节细胞自噬(图7)。
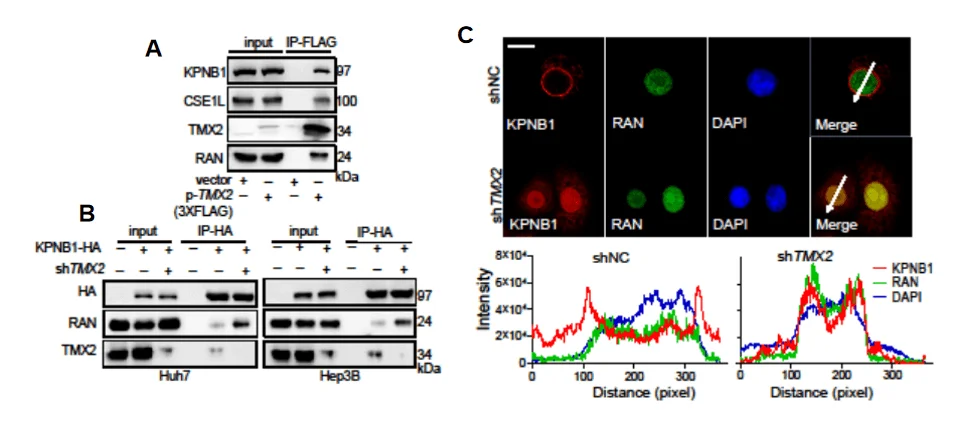
图7 TMX2通过调控KPNB1蛋白的核质比来调节细胞自噬
五、源井生物CRISPR文库定制化服务
源井生物为您提供一站式
CRISPR 文库定制服务
,覆盖 sgRNA 设计、载体构建到文库质粒 NGS
测序全流程,全方位助力药物抑制靶点、肿瘤转移靶点、细胞增殖相关靶点等研究与探索。
✔拥有自主开发的sgRNA批量设计平台,全面打靶所有转录本,确保高编辑效率与低脱靶率,为下游实验提供强有力保障。
✔支持多类型文库载体定制,提供多种抗性标记与荧光标签选项,灵活匹配不同实验体系和筛选策略自主研发高性能电转感受态细胞,有效提升文库扩增效率,显著减少CRISPR质粒文库扩增过程中的重组和条带异常。
✔采用高通量NGS测序,确保sgRNA覆盖率>99%、均一性<10%;结合一代测序与酶切鉴定,全面排查载体污染,确保文库质粒纯净稳定。
✔超40种现货 CRISPR文库质粒,品类齐全、覆盖广泛,支持即买即用,缩短实验准备周期。
✔更提供150余种现货CRISPR文库病毒,600余种文库Cell
Pool,文库构建不费心,到手即开筛。
六、总结
总的来说,作为细胞信号调控的核心载体,膜蛋白凭借其关键的生理功能与疾病关联特性,始终是科研与药物研发的核心方向,而膜蛋白 CRISPR 文库则为解锁膜蛋白的靶点价值提供了高效工具。敲除、激活、抑制三类定制化文库的构建,结合高通量、高精准的筛选流程,既能精准解析膜蛋白的功能机制,又能高效挖掘疾病相关的潜在靶点,适配基础科研、靶点发现、药物研发等多种应用场景。这一技术将膜蛋白的功能研究与临床转化紧密衔接,为肿瘤、病毒感染等多种疾病的机制探索和治疗方案开发提供了核心技术支撑,也为后续精准靶向研究开辟了更高效的路径,让膜蛋白这一重要靶点的研究与应用更具针对性和实用性。
参考文献
[1]van der Weyden L, Harle V, Turner G, Offord V, Iyer V, Droop A,
Swiatkowska A, Rabbie R, Campbell AD, Sansom OJ, Pardo M, Choudhary JS,
Ferreira I, Tullett M, Arends MJ, Speak AO, Adams DJ. CRISPR activation
screen in mice identifies novel membrane proteins enhancing pulmonary
metastatic colonisation. Commun Biol. 2021 Mar 23;4(1):395.
[2]Zhang W, Tang Y, Yang P, Chen Y, Xu Z, Qi C, Huang H, Liu R, Qin H, Ke H,
Huang C, Xu F, Pang P, Zhao Z, Shan H, Xiao F. TMX2 potentiates cell
viability of hepatocellular carcinoma by promoting autophagy and mitophagy.
Autophagy. 2024 Oct;20(10):2146-2163.
[3]Meyers RM, Bryan JG, McFarland JM, Weir BA, Sizemore AE, Xu H, Dharia NV,
Montgomery PG, Cowley GS, Pantel S, Goodale A, Lee Y, Ali LD, Jiang G,
Lubonja R, Harrington WF, Strickland M, Wu T, Hawes DC, Zhivich VA, Wyatt
MR, Kalani Z, Chang JJ, Okamoto M, Stegmaier K, Golub TR, Boehm JS, Vazquez
F, Root DE, Hahn WC, Tsherniak A. Computational correction of copy number
effect improves specificity of CRISPR-Cas9 essentiality screens in cancer
cells. Nat Genet. 2017 Dec;49(12):1779-1784.











