IF=26.6 | 源井Luc细胞助力脑肿瘤活体成像与放疗免疫治疗机制研究


引言
放疗用于超半数癌症患者治疗,但传统放疗增敏剂多通过提升活性氧(ROS)增强细胞毒性,在缺氧肿瘤中效果有限且易损伤健康组织。中国科学技术大学闵元增教授团队在 Nature Biomedical Engineering (IF=26.6)发表题为“X-ray activated platinum complex induces DNA damage and enhances cancer immunotherapy through abscopal effect”的研究论文,该研究开发一种 叠氮铂 (II) 配合物(Complex 1) ,其在 X 射线照射下释放铂氮烯,以非 ROS 依赖方式与 DNA 碱基亲核位点共价结合引发双链断裂,联合低剂量放疗与 PD-1 抑制剂可实现 40% 双侧肿瘤小鼠完全消退,展现强效远隔效应,为精准放疗提供全新金属氮烯介导策略。源井生物为该研究提供 Gl261-Luc细胞 ,助力高效实现原位脑肿瘤模型的疗效评估。

研究背景
放疗主要通过 DNA 损伤杀伤肿瘤细胞,但对转移性肿瘤疗效有限;免疫检查点抑制剂(ICIs)可与放疗协同放大远隔效应,却受限于放疗剂量与肿瘤放射敏感性差异。金属氮烯作为高活性催化中间体,具备与 DNA 碱基反应增强放疗敏感性的潜力,但现有研究仅聚焦紫外激活,无法用于体内。同时,传统铂类药物通过 Pt-N 配位结合 DNA,存在毒性与耐药问题,亟需开发作用机制全新的铂基放疗增敏剂。
研究目的
- 构建 X 射线激活的铂基配合物,验证其体内外放疗增敏活性。
- 阐明铂氮烯介导的 DNA 损伤全新分子机制。
- 评估该配合物联合放疗与免疫治疗的抗肿瘤效果、远隔效应及生物安全性。
- 验证其在原位胶质母细胞瘤等模型中的治疗潜力。
研究路线
- 分子验证: 证实 Complex 1 经 X 射线照射生成铂氮烯,通过 N-N 耦合与 DNA 结合(非传统 Pt-N 配位)。
- 体外验证: 明确 1+RT 以非 ROS 依赖方式诱导 DNA 双链断裂与免疫原性细胞死亡(ICD)。
- 体内单瘤验证: 3.证实 1+RT 抑制肿瘤生长、激活抗肿瘤免疫、选择性降低 Treg 浸润。
- 远隔效应验证: 1+RT+αPD-1 协同抑制双侧肿瘤,实现高比例完全消退。
- 安全性与记忆验证: 评估系统毒性,确认长效免疫记忆与脑肿瘤治疗潜力。
主要结果
1. Complex 1 经放疗生成铂氮烯并与 DNA 共价结合
X 射线照射下,Complex 1 释放 N₂生成铂氮烯,质谱捕获该中间体与 DMS、胞嘧啶的反应产物。DFT 计算显示铂氮烯与 DNA 通过 N-N 耦合(Pt-N-N-DNA) 结合,区别于传统铂药配位结构,结合位点为 DNA 大沟 GC 步骤胞嘧啶胺基。天然键轨道分析证实 Pt (II)-N 的铂氮烯特征,Pt-N 键级为 1.15,结构稳定。
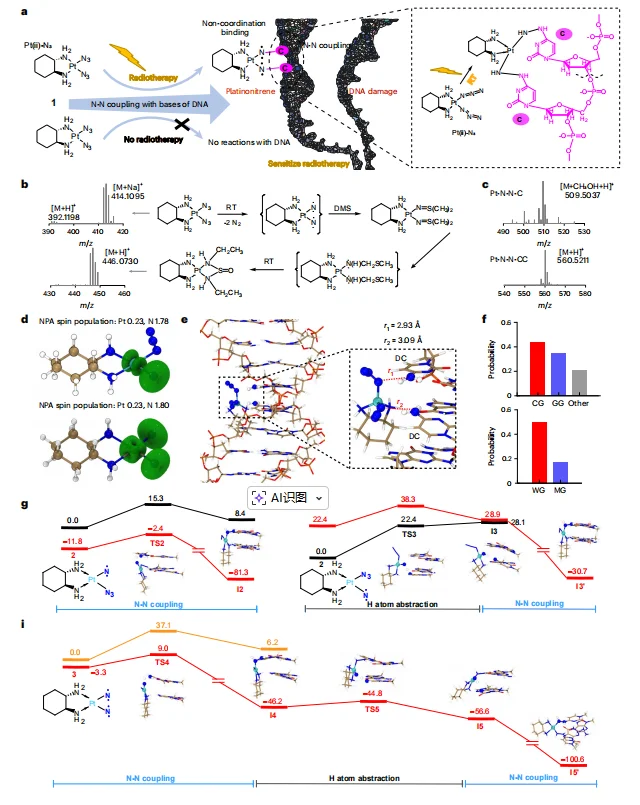
图1.在放疗条件下与Complex 1生成铂氮三烯及其通过N-N偶联进行DNA铂化
2. Complex 1 增敏放疗诱导增强 ICD 与 DNA 损伤
通过凋亡检测发现1+RT 组晚期凋亡细胞比例是单纯放疗组的 2.4 倍,显著降低线粒体膜电位。1+RT 可清除肿瘤细胞 ROS 与超氧阴离子,证实 不依赖 ROS 的增敏通路。肿瘤组织 CRT、HMGB1 表达提升 2-3 倍,ATP 分泌增加 1.5 倍。γH2AX 表达显著升高,彗星实验显示 Tail DNA% 最高,双链断裂效应最强;克隆形成实验证实放疗杀伤效果显著增强。
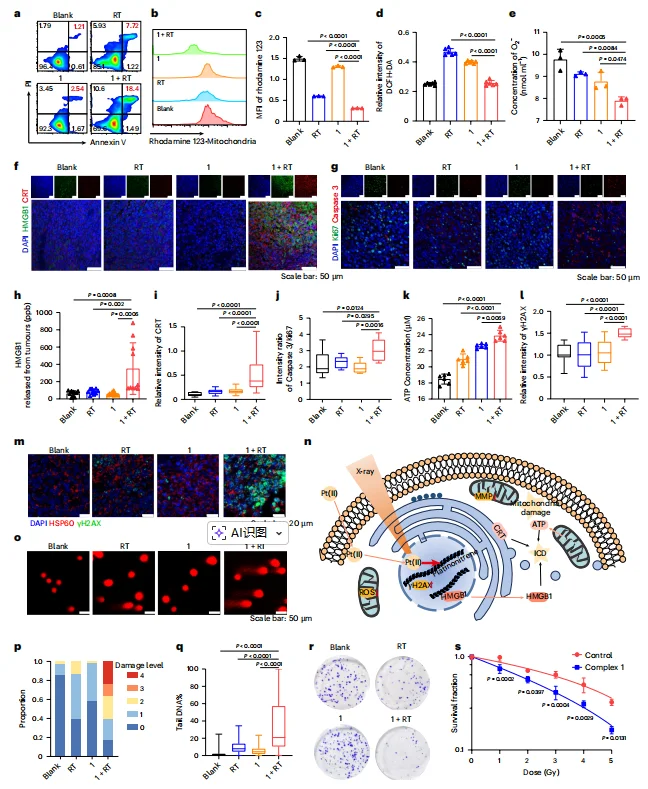
图2.Complex 1增敏的放射治疗可增强细胞毒性,表现出更强的DNA损伤能力,并在CT26细胞中诱导更显著的免疫原性细胞死亡。
3. Complex 1 增敏放疗在体内发挥强效抗肿瘤应答
体外实验发现,CT26 与 4T1 肿瘤中,1+RT 组肿瘤生长显著慢于其他组,约 1/3 小鼠完全治愈,生存期显著延长。4T1 模型中,1+RT 组肺部转移结节数量显著少于其他组。肿瘤引流淋巴结中 CD80⁺CD86⁺成熟 DCs 比例提升 2-3 倍;肿瘤浸润 CD45⁺CD3⁺T 细胞、CD8⁺T 细胞翻倍,Treg 比例仅为对照组的 16%。CD8⁺IFNγ⁺、CD8⁺CD107a⁺细胞比例升高,肿瘤组织 IFNγ、Granzyme B 分泌显著增加;GSEA 显示 PD-1/PD-L1 通路响应增强。
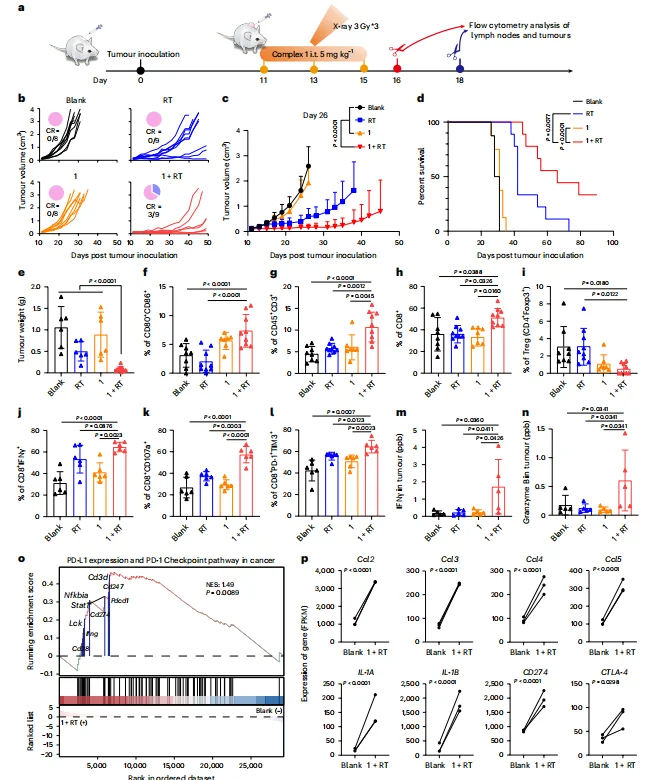
图3.Complex 1增敏的放射治疗可有效抑制已建立的CT26肿瘤生长。
4. RNA-seq 证实 Complex 1增敏放疗重塑肿瘤免疫微环境
PCA 分析显示各组基因表达存在显著差异,1+RT 组基因表达谱独特1+RT 组基质评分、免疫评分、ESTIMATE 评分显著升高,肿瘤纯度降低。差异基因富集于先天免疫、炎症反应、T 细胞活化等通路,激活多维度免疫应答。活化 CD8⁺T 细胞比例上升,Treg 比例下降,与流式结果一致。
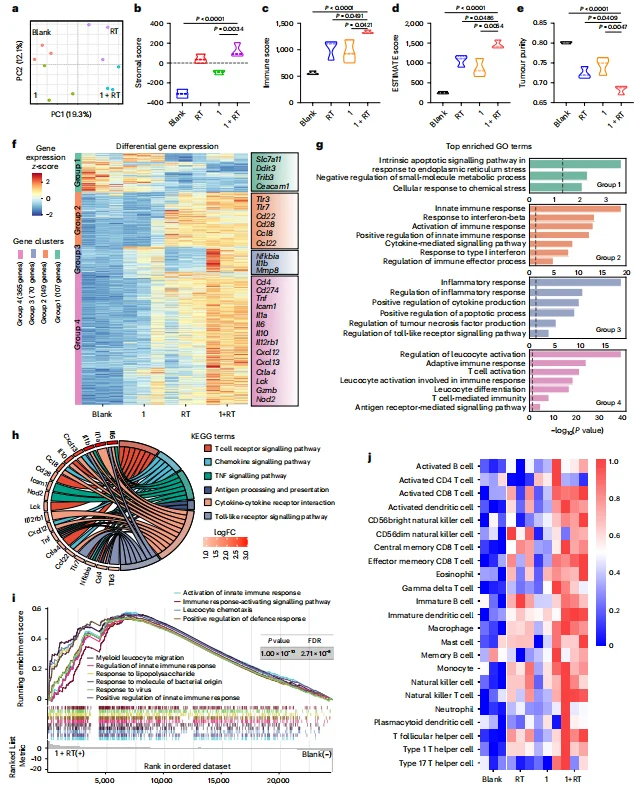
图4.CT26肿瘤组织的RNA测序分析表明,Complex 1增敏的放射治疗可诱导免疫细胞浸润至TME。
5. Complex 1 选择性抑制 Treg 细胞增殖
Complex 1 浓度≥2.0 μg/ml 时, 选择性抑制 Treg 增殖, 对 CD4⁺、CD8⁺T 细胞增殖无影响。通过抑制增殖而非诱导凋亡降低 Treg 比例,低浓度下无明显细胞毒性。
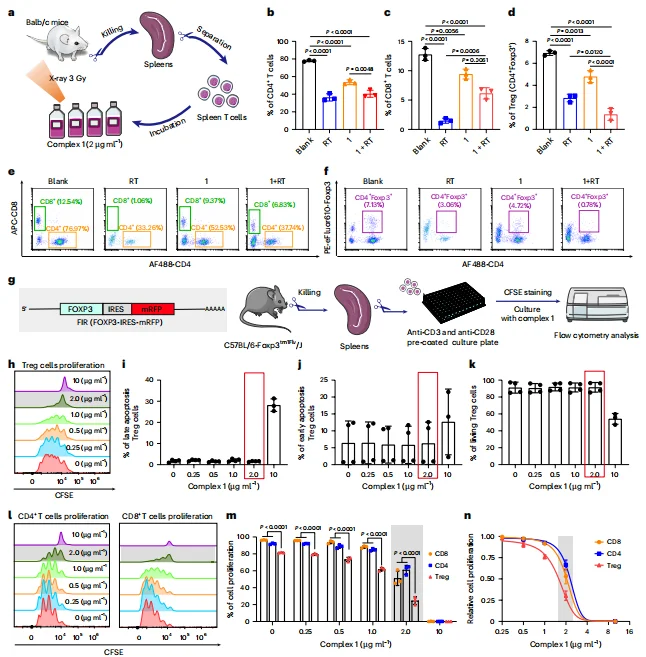
图5.Complex 1本身可抑制调节性T细胞(Treg细胞)增殖。
6. 低剂量放疗增敏增强远隔效应
1+RT+αPD-1 组 αPD-1 疗效显著提升,20% 小鼠完全治愈。仅对原发灶给药 + 放疗,1+RT+αPD-1 组 原发与继发肿瘤均显著消退, 40% 小鼠双侧肿瘤完全消失。原发与继发肿瘤中 CD45⁺CD3⁺、CD8⁺T 细胞升高,Treg 降低,CD8⁺/Treg、CD4⁺/Treg 比值显著提升;引流淋巴结 DC 成熟度升高。
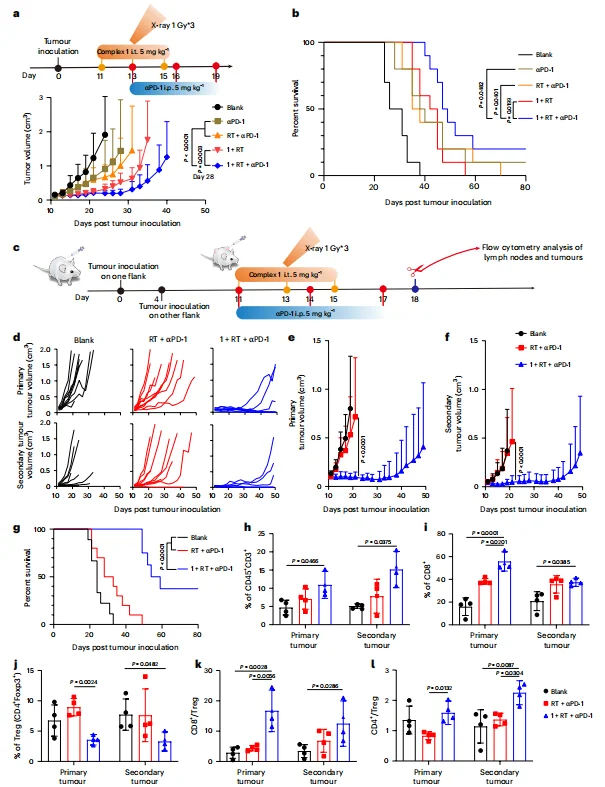
图6.在同基因CT26肿瘤模型中,Complex 1增敏放疗可增强免疫治疗效果及远隔效应。
7. 可靠生物安全性与长效免疫记忆效应
Complex 1 对心、肝、脾、肺、肾无明显损伤,无显著肾毒性;对比奥沙利铂,无肝肾损伤。治愈小鼠外周血效应记忆 T 细胞(CD44⁺CD62L⁻)比例显著升高;肿瘤再挑战可完全抵抗,形成长效保护。Complex 1 可进入脑部,1+RT 显著抑制原位胶质母细胞瘤生长,延长小鼠生存期。
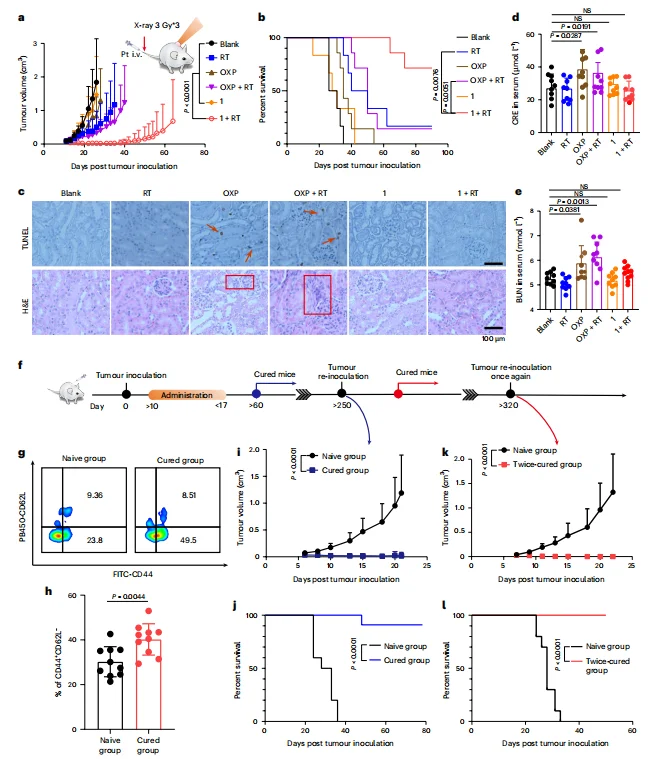
图7.Complex 1增明放疗具有可靠的生物安全性,并在同基因CT26肿瘤模型中产生持久的免疫记忆效应。
研究意义与创新点
首次开发 X 射线激活、非 ROS 依赖 的铂氮烯放疗增敏剂,颠覆传统铂药与增敏剂作用机制,突破缺氧肿瘤放疗抵抗瓶颈。兼具放疗增敏与选择性抑制 Treg 双重功能,联合免疫治疗强效放大远隔效应,为转移性肿瘤治疗提供新方案。可用于原位胶质母细胞瘤等难治疗实体瘤,覆盖多癌种、多场景放疗 - 免疫联合治疗。
文章小结
本研究成功研发 X 射线激活的叠氮铂配合物,在放疗下生成铂氮烯,通过 N-N 耦合共价损伤 DNA,以非 ROS 依赖方式增敏放疗;同时选择性抑制 Treg 增殖,重塑肿瘤免疫微环境,联合 PD-1 抑制剂实现强效远隔效应与长效免疫记忆。该策略安全高效,为精准放疗与肿瘤免疫联合治疗提供全新范式,具备极高临床转化价值。
在本研究中,源井生物提供的 Gl261-Luc细胞 作为原位胶质母细胞瘤活体示踪模型,通过生物发光信号与野生型 GL261 细胞的定量对比,直观精准地验证了 X 射线激活叠氮铂配合物抑制脑肿瘤、增强免疫治疗的分子机制与体内疗效。
>>>研究同款细胞现在仅需¥1599,立即咨询!源井Luc细胞
源井生物提供超 300种 Luc细胞,经多篇 客户高分文献 引用验证,可稳定表达萤火虫(Firefly)的Luciferase荧光素酶, 特异性强且高度灵敏, 成像质量高,发光强度可精确定量,细胞株代次低、活性高、状态好,能够很好地帮助您进行转录因子调控机制研究、活体成像、细胞示踪等实验。











