研究前沿|癌症 “以毒攻毒”?胱抑素 C 激活 TREM2 通路为阿尔茨海默病治疗开辟新赛道


引言
阿尔茨海默病(AD)与癌症作为全球最具破坏性的疾病,流行病学数据显示癌症病史患者的 AD 发病率显著降低,但两者间的相互作用机制长期不明。华中科技大学团队发表于Cell的研究首次揭示: 外周癌症可通过分泌胱抑素 C(Cyst-C),结合淀粉样蛋白寡聚体并激活小胶质细胞表面的髓系细胞触发受体 2(TREM2),进而降解已形成的淀粉样斑块,最终改善 AD 模型小鼠的病理损伤和认知功能。 这一发现不仅为癌症神经科学提供了全新视角,更突破了传统淀粉样蛋白降低策略的局限,为 AD 精准靶向治疗提供了创新性思路。

研究背景
AD 是一种以认知功能进行性下降为特征的神经退行性疾病,β- 淀粉样蛋白(Aβ)沉积形成的老年斑是其核心病理标志。尽管目前已有部分抗 Aβ 抗体获批用于临床,但长期疗效和安全性仍存争议,且缺乏能降解已形成斑块的疾病修饰疗法。癌症与 AD 共享吸烟、细胞周期调控异常等多种风险因素,且流行病学研究一致提示两者发病率存在负相关,但由于患者存活时间差异、诊断偏倚等干扰因素,外周癌症对 AD 病理进程的直接影响及分子机制始终未被阐明。
研究目的
明确外周癌症对 AD 淀粉样病理的调控作用,鉴定癌症分泌的关键效应分子,揭示其介导 AD 病理改善的核心信号通路,为开发新型 AD 治疗策略提供实验依据。
研究方法
- 动物模型构建: 向 3 月龄 5×FAD 小鼠(AD 淀粉样病理模型)和 5 月龄 rTg4510 小鼠(tau 病理模型)尾静脉注射 Lewis 肺癌(LLC)、前列腺癌(RM1)、结肠腺癌(MC38)细胞,构建荷瘤 AD 小鼠模型。构建小胶质细胞特异性 TREM2 敲除(Cx3cr1TREM2-/-)、TREM2R47H 突变及 Cyst-CL68Q 突变小鼠模型,验证通路特异性。
- 敲除细胞系构建: 通过 CRISPR-Cas9 技术构建 CLS1、CPE、Cst3(编码 Cyst-C)、GSN 等基因敲除的 LLC 细胞系,验证关键效应分子。
- 干预与检测手段: 癌症细胞分泌蛋白(CSPs)提取与尾静脉注射,连续干预 30-60 天。
- 行为学测试: Morris 水迷宫、新臂 Y 迷宫评估小鼠认知功能。
- 病理检测: 免疫荧光染色(Aβ1-16、硫代黄素 S 标记)、Western blot 量化淀粉样斑块负荷及相关蛋白表达。
- 分子机制验证: RNA-seq、蛋白质组学筛选差异分子;ELISA 检测血浆 / 脑脊液中 Cyst-C 水平;FRET assay 验证 TREM2 与 DAP12 相互作用;流式细胞术分析免疫细胞亚群;125I 标记检测 Cyst-C 血脑屏障穿透能力。
- 临床样本验证: 检测非小细胞肺癌、前列腺癌、结肠癌等多种癌症患者血浆中 Cyst-C 及候选蛋白水平。
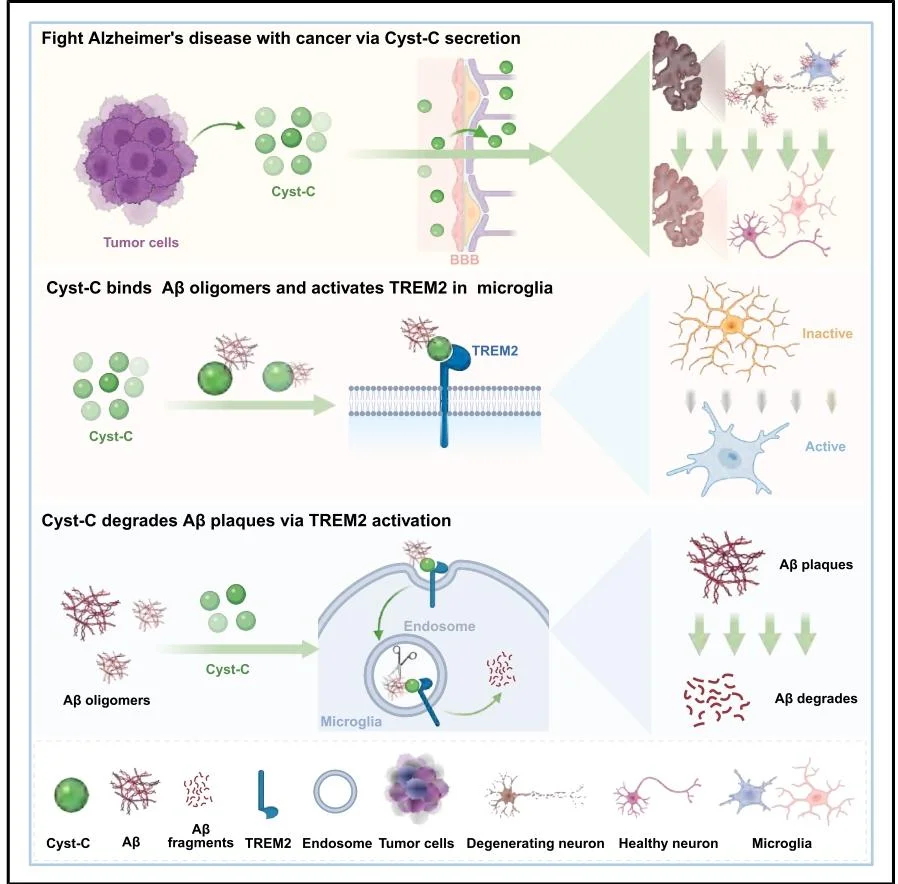
图1.利用外周癌分泌Cyst-C对抗阿尔兹海默症的机制图
研究路线
- 现象发现: 荷瘤 AD 小鼠模型中,多种外周癌症显著降低大脑 Aβ 沉积和斑块负荷,但不影响 tau 蛋白错误折叠,证实癌症对 AD 淀粉样病理的选择性抑制作用。
- 效应分子定位: 通过 CSPs 干预实验排除肿瘤物理负荷的影响,结合转录组与蛋白质组学筛选,鉴定出 Cyst-C 为介导淀粉样病理抑制的核心分泌蛋白。
- 作用途径验证: 125I 标记实验证实肿瘤来源的 Cyst-C 可穿透 AD 模型小鼠受损的血脑屏障,且其作用不依赖于外周免疫细胞。
- 分子机制解析: 明确 Cyst-C 作为 TREM2 配体,直接结合 Aβ1-42 寡聚体并激活 TREM2,促进小胶质细胞吞噬和降解淀粉样斑块,该效应可被 TREM2 或 Cyst-C 突变完全阻断。
- 治疗潜力验证: 重组人 Cyst-C 干预可剂量依赖性改善年轻及老年 AD 模型小鼠的病理和认知功能,证实其治疗潜力。
主要结果
1. 外周癌症选择性抑制 AD 淀粉样病理
LLC、RM1、MC38 三种癌症均能显著降低 5×FAD 小鼠大脑可溶性与不可溶性 Aβ1-42、Aβ1-40 水平及斑块面积,但对 rTg4510 小鼠的 tau 磷酸化无影响。
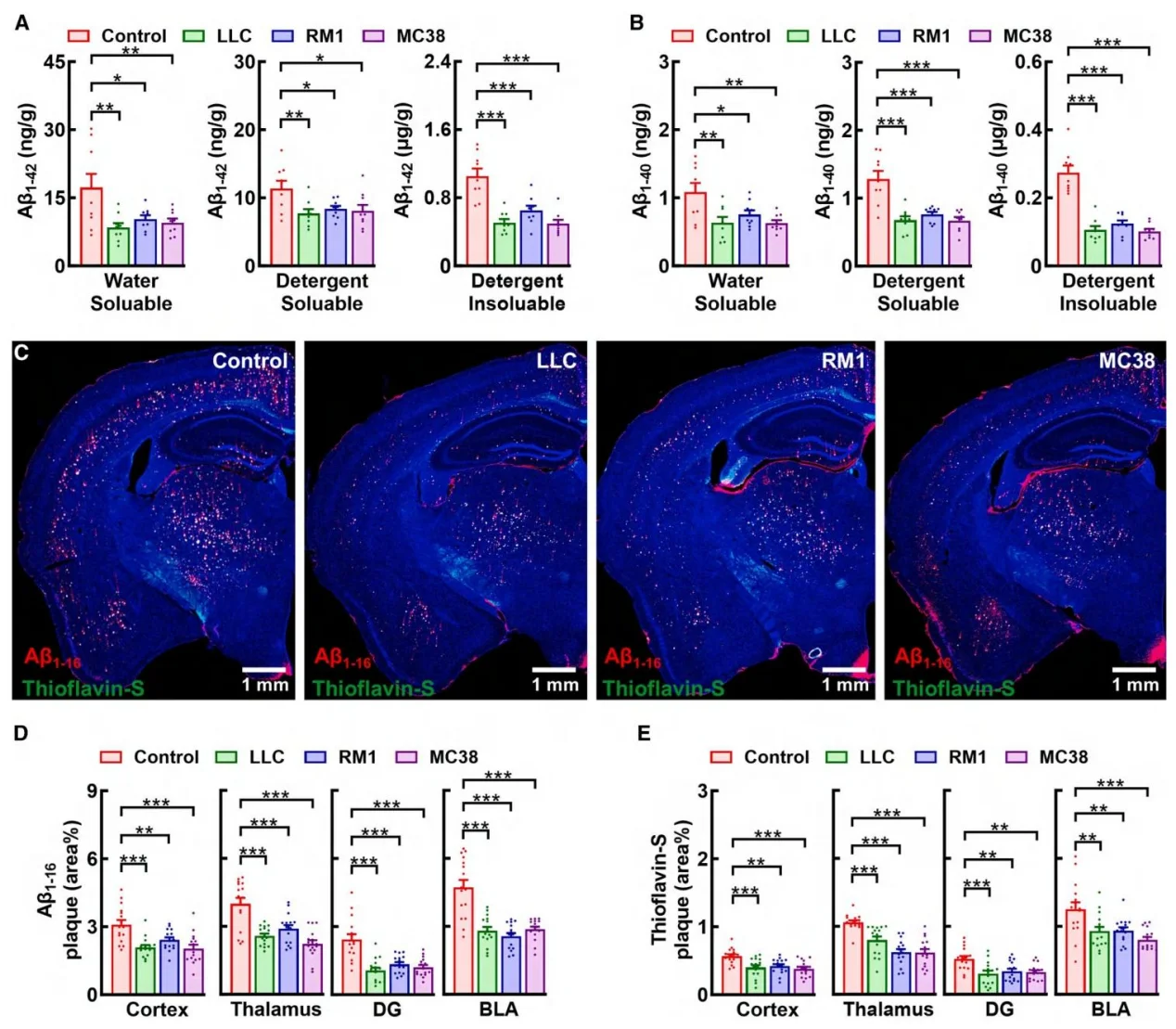
图2.外周癌症减轻淀粉样病理
2. Cyst-C 是癌症介导保护作用的关键分子
癌症患者及荷瘤小鼠血浆中 Cyst-C 水平显著升高,且 CSPs 中 Cyst-C 缺失会完全丧失淀粉样病理抑制作用。补充重组人 Cyst-C 可模拟癌症的保护效应,而 Cyst-CL68Q 突变体(无法结合 TREM2)无此作用。
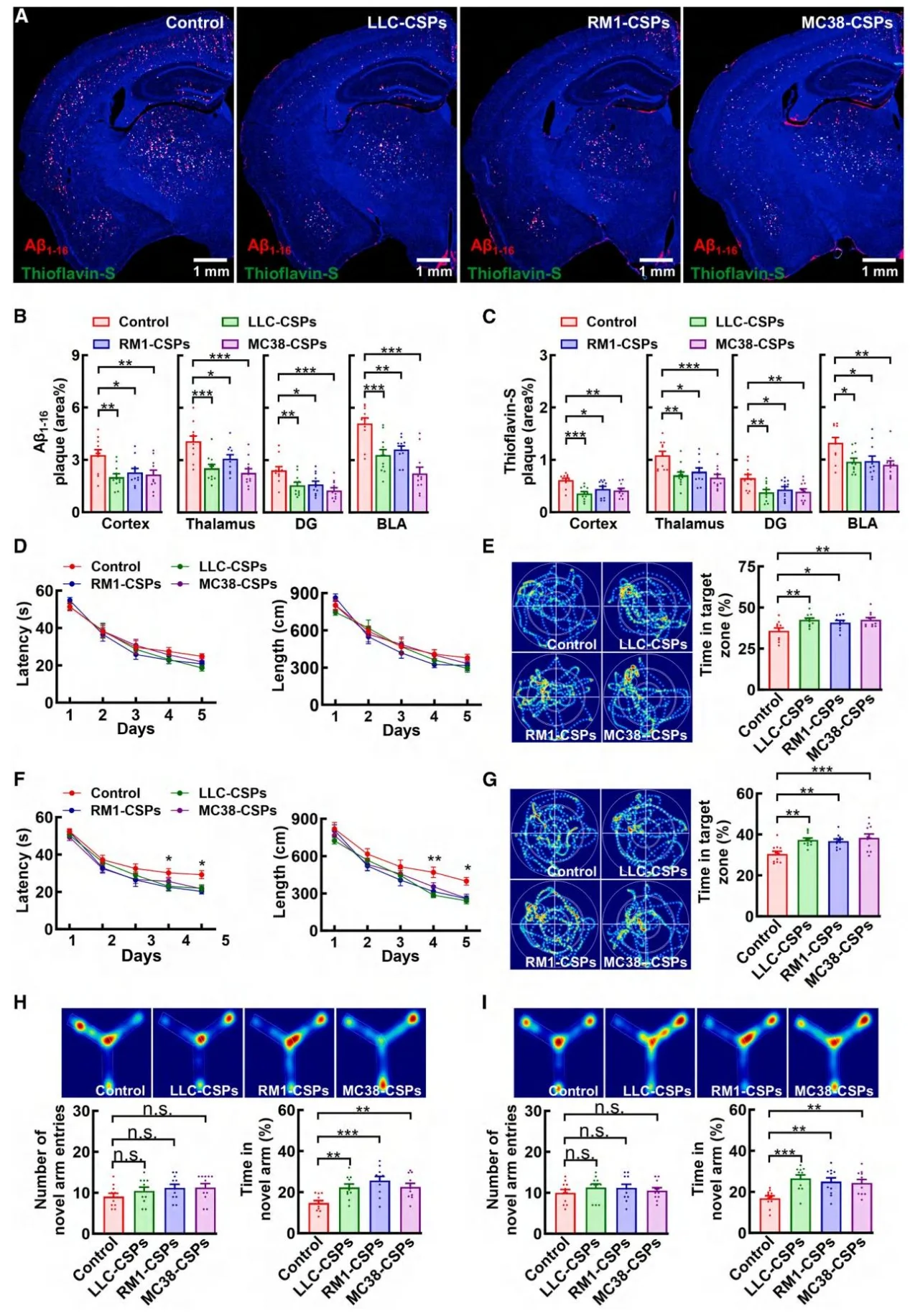
图3.外周癌症通过分泌蛋白(CSPs)抑制淀粉样病理
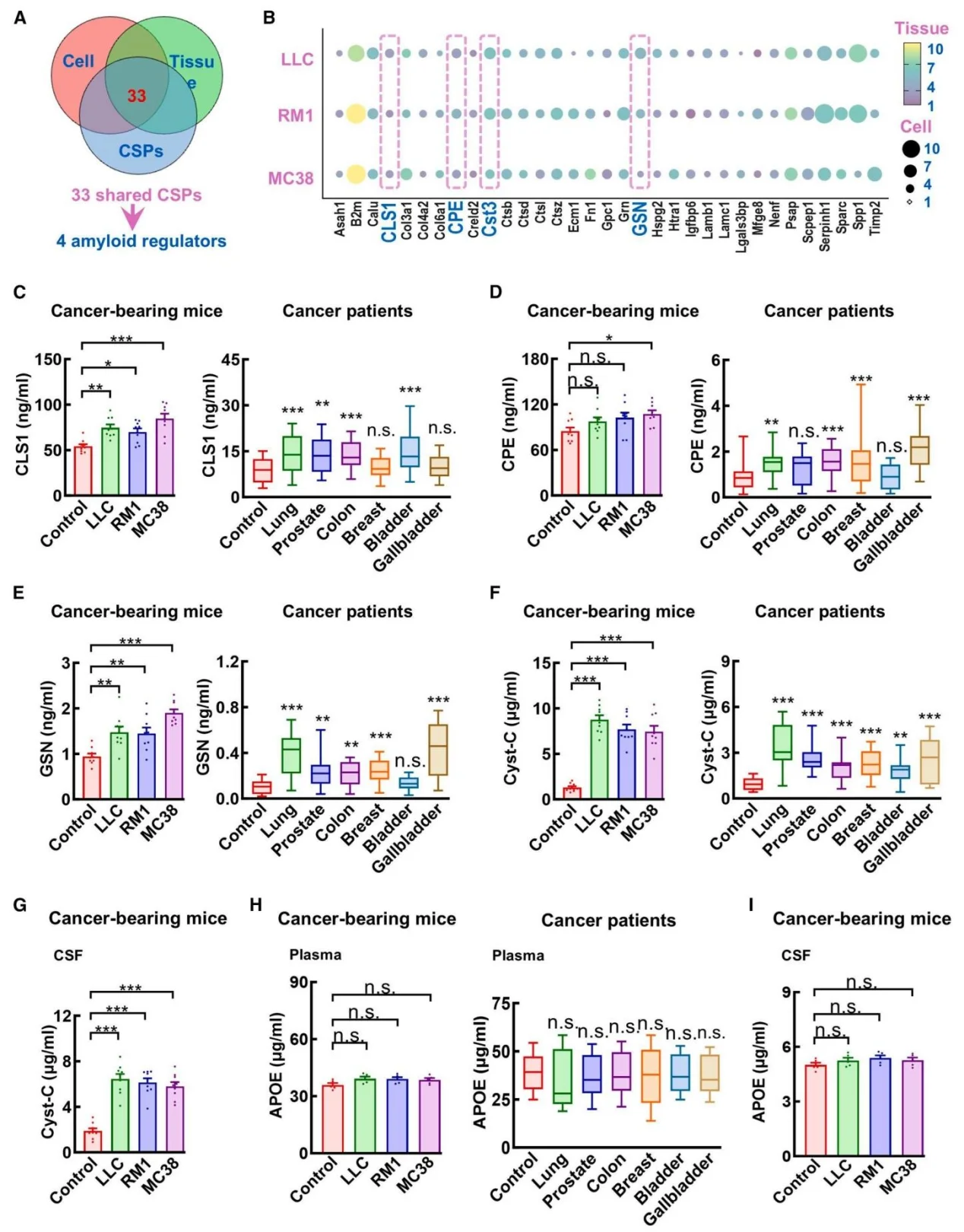
图4.对癌症分泌蛋白(CSPs)中淀粉样蛋白抑制剂的无偏蛋白质组学筛选
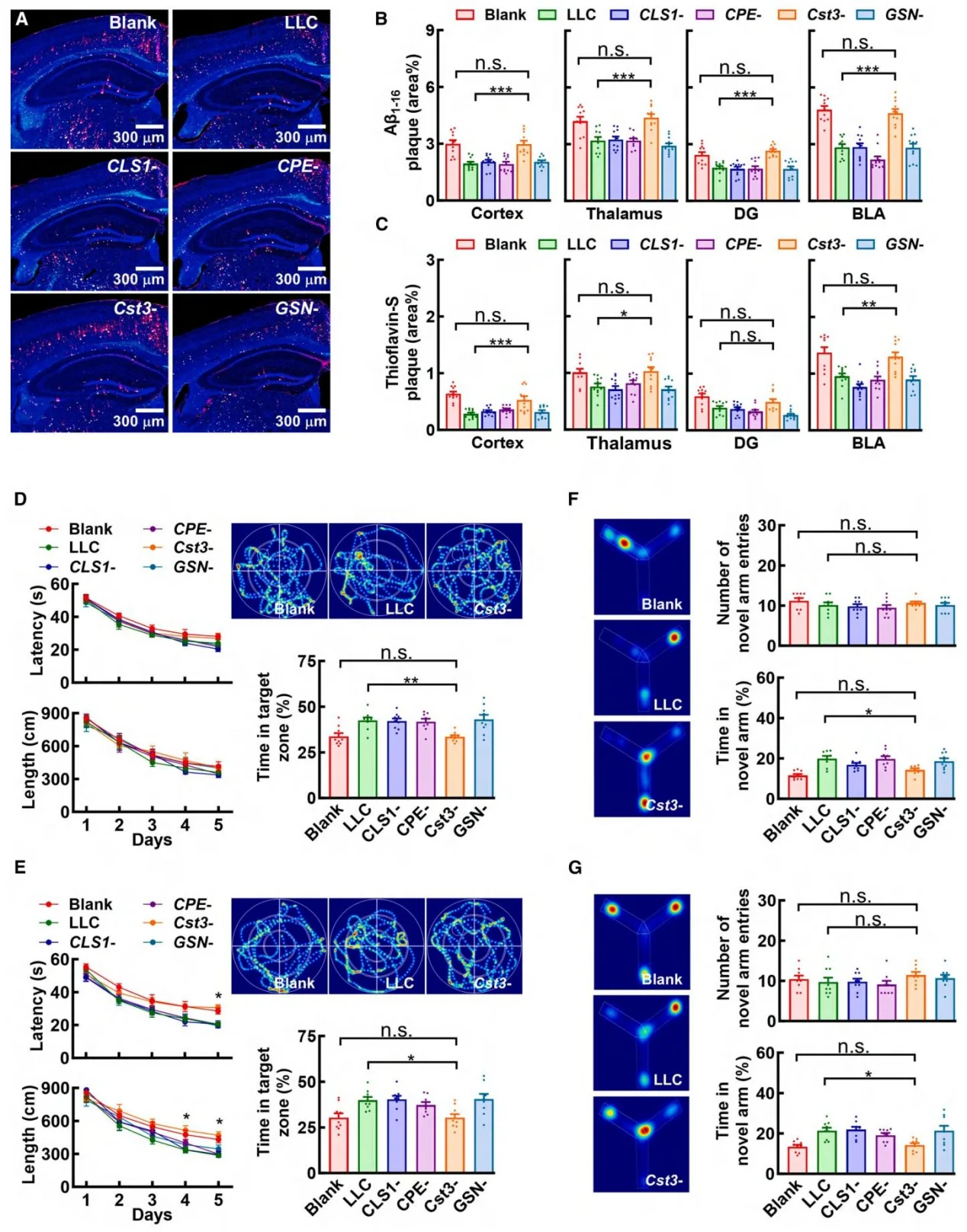
图5.外周癌症通过分泌胱抑素 C(Cyst-C)抑制淀粉样病理
3. Cyst-C 通过血脑屏障发挥作用
13 kDa 的 Cyst-C 可穿透 AD 模型小鼠的血脑屏障,其脑内浓度达到治疗相关水平,而 67 kDa 的白蛋白无法穿透。
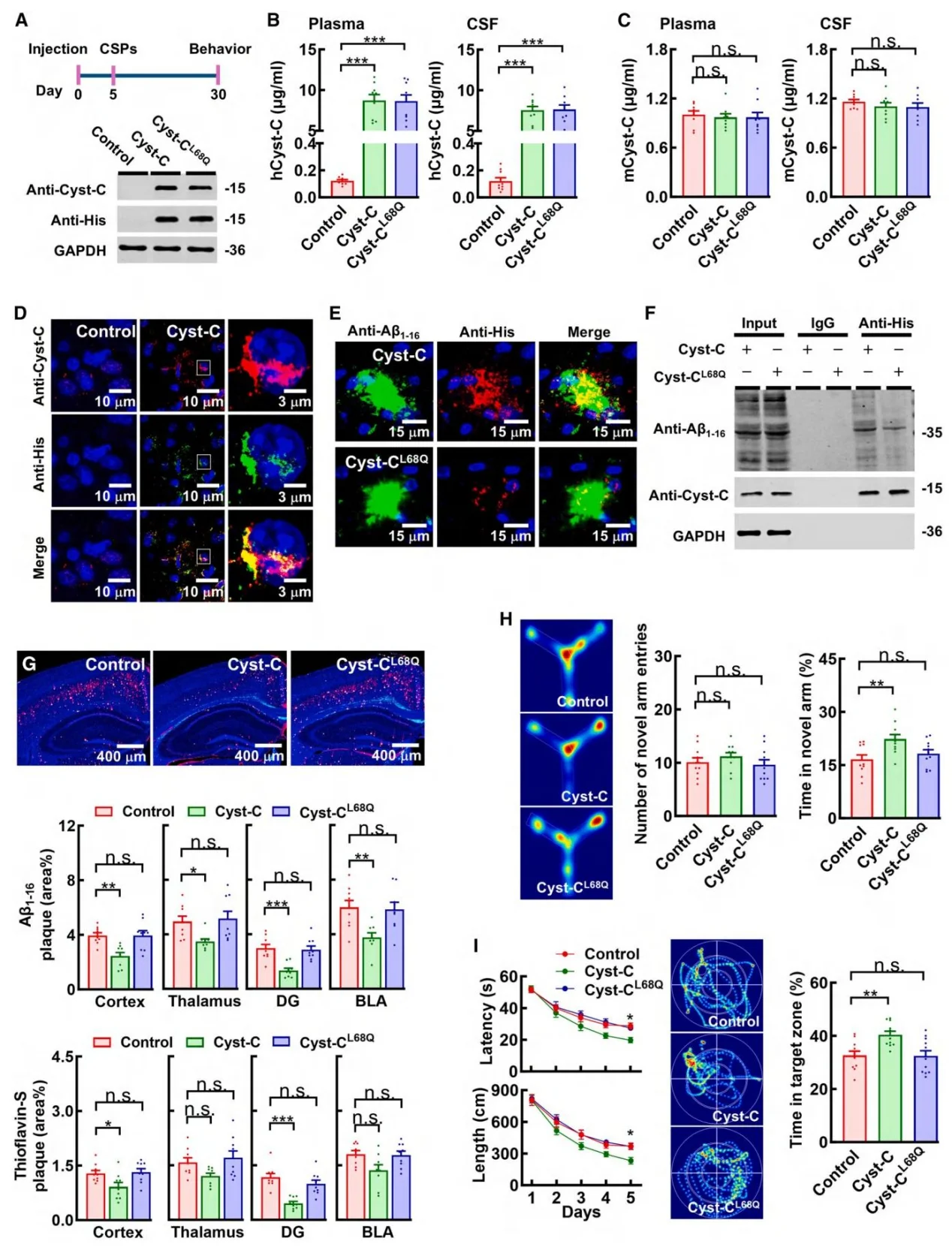
图6.癌细胞分泌的胱抑素 C(Cyst-C)抑制淀粉样病理
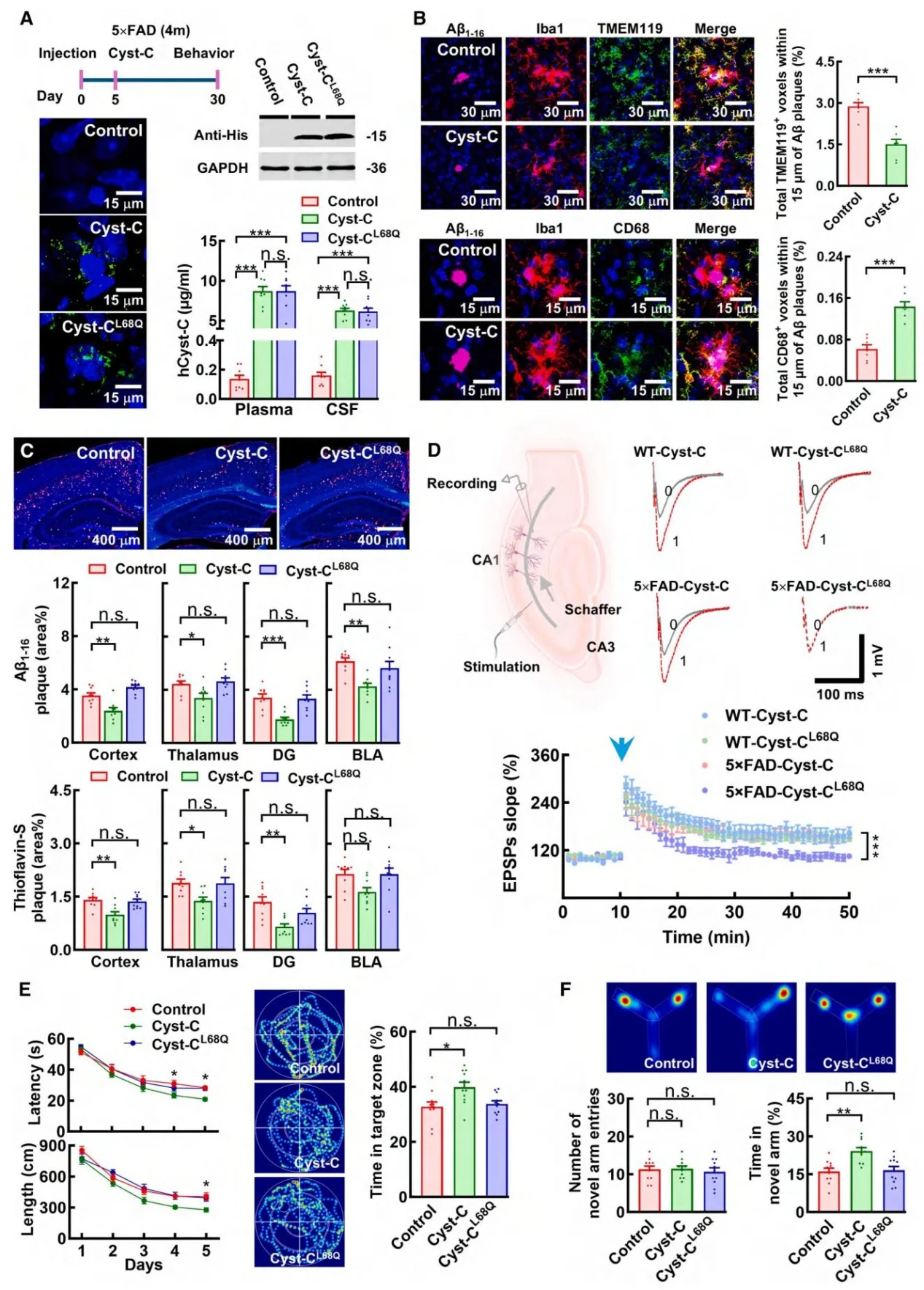
图7.人源胱抑素 C(Cyst-C)抑制淀粉样病理
4. Cyst-C-TREM2 通路是核心机制
Cyst-C 直接结合 Aβ1-42 寡聚体和 TREM2 extracellular domain,TREM2R47H 突变会破坏两者结合。Cyst-C 激活 TREM2 下游 SYK 信号通路,促进小胶质细胞向斑块聚集、增强吞噬功能,加速已形成斑块的降解。小胶质细胞特异性 TREM2 敲除会完全阻断 Cyst-C 的治疗效应。
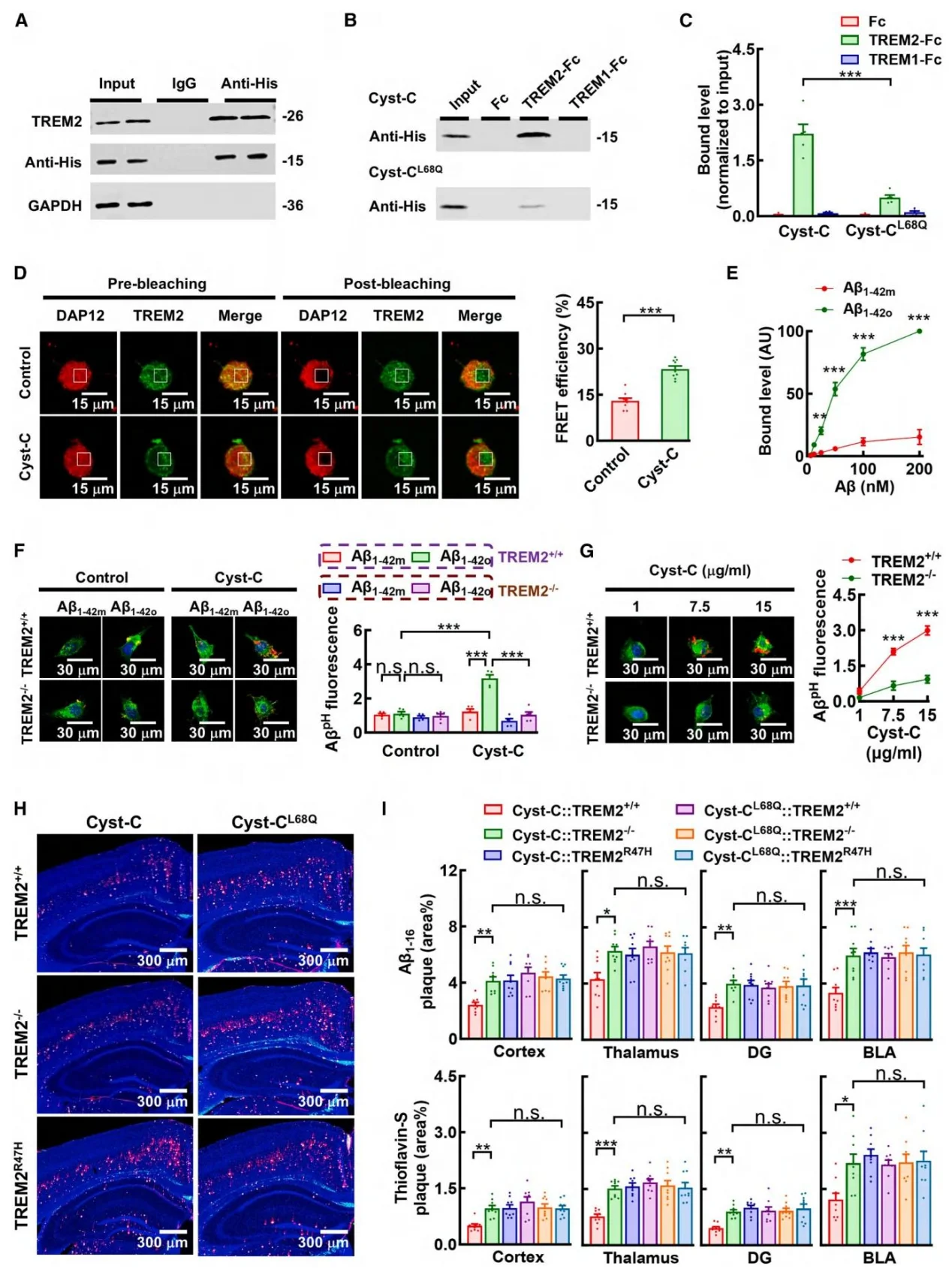
图8.人源胱抑素 C(Cyst-C)通过 TREM2 降解已形成的淀粉样斑块
5. Cyst-C 具有临床转化潜力
重组人 Cyst-C 可改善不同月龄 AD 模型小鼠的认知功能,逆转突触传递长时程增强(LTP)缺陷,且不影响 APP 加工相关酶活性。
研究意义与创新点
- 概念突破: 首次证实外周癌症通过分泌蛋白主动调控 AD 病理进程,建立了 “癌症 - 分泌蛋白 - AD” 的跨界调控网络,拓展了癌症神经科学的研究范畴。
- 机制创新: 鉴定 Cyst-C 为 TREM2 的功能性激动剂,揭示 “Cyst-C 结合 Aβ 寡聚体→激活小胶质细胞 TREM2→降解已形成淀粉样斑块” 的全新机制,突破传统 AD 治疗仅聚焦于阻止 Aβ 生成的局限。
- 治疗新思路: 提供了以 “降解现有斑块” 为核心的 AD 治疗策略,重组 Cyst-C 或其模拟物有望成为精准靶向 AD 病理的新型疗法,且 Cyst-C 可穿透血脑屏障的特性为药物递送提供了天然优势。
- 临床关联价值: 解释了流行病学观察到的癌症与 AD 发病率负相关现象,为后续探索癌症患者 AD 风险降低的临床机制提供了实验基础。
文章小结
本研究通过多模型验证、多组学筛选及分子机制解析,明确外周癌症可通过分泌 Cyst-C,经 TREM2 激活通路降解 AD 模型小鼠的淀粉样斑块并改善认知功能。这一发现不仅阐明了癌症与 AD 之间的跨界调控机制,更打破了传统 AD 治疗的思路局限,为开发靶向 Cyst-C-TREM2 通路的新型疾病修饰疗法提供了坚实的实验依据,具有重要的基础研究价值和临床转化潜力。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有11000+细胞产品(含8000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
CST3基因编码胱抑素C(Cystatin C),是一种重要的蛋白酶抑制剂,参与调节炎症、免疫反应和细胞代谢。 如果您也想针对CST3展开研究,源井生物可为您提供CST3基因敲除细胞,涵盖A549、NCI-H1299等肿瘤细胞系。如果您有个性化基因编辑的需要,欢迎咨询!
联系我们了解更多>>>参考文献
Li X, Tang X, Zeng J, Duan L, Hou Z, Li L, Guo Y, Chai C, Liu J, Wang Y, Zhu LQ, Li H, Zhang T, Wang Y, He A, Lu Y. Peripheral cancer attenuates amyloid pathology in Alzheimer's disease via cystatin-c activation of TREM2. Cell. 2026 Feb 5;189(3):853-871.e31. doi: 10.1016/j.cell.2025.12.020. Epub 2026 Jan 22. PMID: 41576952.











