CRISPR 文库筛选解码激酶降解新机制:单功能抑制剂 “超级激活” 内源性降解通路


引言
靶向蛋白降解(TPD)技术中,PROTACs、分子胶等双功能分子需诱导靶蛋白与 E3 泛素连接酶 proximity 发挥作用,但存在成药性差、脱靶风险高等局限。奥地利科学院 Georg E. Winter 团队在 Nature 发表的重磅研究,通过 CRISPR 文库筛选为核心技术, 系统性揭示单功能激酶抑制剂可通过 “超级激活” 细胞内源性降解通路诱导靶蛋白选择性降解。研究借助 CRISPR 筛选精准定位降解关键调控因子, 阐明了 LYN、BLK、RIPK2 三种激酶的差异化降解机制,突破了传统 TPD 依赖双功能分子的认知, 为单功能降解剂研发提供了全新范式,而 CRISPR 文库筛选正是贯穿全程、破解机制谜题的核心技术支撑。

研究背景
激酶抑制剂是临床应用最广泛的靶向药物之一,但部分抑制剂被发现可诱导靶蛋白降解,其机制多被归因于破坏 HSP90 分子伴侣相互作用。然而,这类现象的普遍性、通用性及深层机制尚未明确。此外,PROTACs 等双功能降解剂虽潜力巨大,但面临膜通透性差、口服生物利用度低、合成难度高等挑战。因此,挖掘单功能小分子诱导靶蛋白降解的规律与机制,对开发新型靶向降解药物具有重要意义。
研究目的
系统鉴定具有降解活性的单功能激酶抑制剂,明确其作用的普遍性与选择性。阐明抑制剂诱导激酶降解的分子机制,突破传统 “分子伴侣剥夺” 的单一认知。建立 “超级激活内源性降解通路” 的理论框架,为单功能降解剂研发提供指导。
研究方法
- 筛选细胞系构建: 针对 LYN、BLK、RIPK2 三种目标激酶,分别构建融合 BFP-P2A-mCherry 的稳定性报告基因细胞系(KBM7 iCas9 或 RKO iCas9 背景),确保降解效应可通过流式细胞术精准量化。
-
文库选择与构建:
- LYN 降解机制研究:采用 泛素 - 蛋白酶体系统(UPS)聚焦型 sgRNA 文库 (含 7801 条 sgRNA),针对性覆盖降解相关基因。
- 通过慢病毒转导 sgRNA 构建 PTEN 敲除单克隆细胞系,通过慢病毒转导过表达载体构建 JUN 过表达细胞系;所有细胞经 STR 鉴定和支原体检测,HEK293T 细胞用于慢病毒包装。
以 MOI=0.1-0.2 进行慢病毒转导,确保每个细胞仅整合 1 条 sgRNA,转导后通过 G418 筛选(1 mg/ml,14 天)获得稳定细胞库,保证 sgRNA 文库覆盖率达 1000×。
- 多组学验证: 结合定量蛋白质组学、化学蛋白质组学(Kinobead profiling)、 proximity 标记(BioID)鉴定降解相关互作蛋白与信号通路。
- 功能验证: 通过 CRISPR-Cas9 基因敲除、药物 rescue 实验、免疫共沉淀、免疫荧光等验证降解机制;利用流式细胞术、Western blot 量化蛋白稳定性与降解效率。
- 结构生物学分析: 借助 AlphaFold3 预测 BLK 与 γ- 分泌酶复合物结构,结合分子动力学模拟解析相互作用模式。
- 机制解析模型: 选取 LYN(HSP90 强依赖型)、BLK(HSP90 弱依赖型)、RIPK2(HSP90 非依赖型)三种代表性激酶,深入剖析降解机制。
研究路线
- 高通量筛选: 建立激酶抑制剂 - 靶蛋白降解图谱,鉴定特异性降解对,分析降解与 HSP90 客户端属性、PROTAC 降解潜力的相关性。
- 机制分类解析: 以 LYN 为模型,阐明 “活性 - 稳定性开关” 介导的降解机制;以 BLK 为模型,揭示 γ- 分泌酶依赖的膜定位调控机制;以 RIPK2 为模型,解析高阶组装诱导的自噬降解机制。
- 理论框架建立: 归纳 “超级激活内源性降解通路” 的共性规律,明确抑制剂诱导靶蛋白形成降解易感状态的核心逻辑。
主要结果
1. 激酶抑制剂诱导降解是普遍现象,具有选择性与特异性
对 98 种激酶(88 种野生型 + 10 种突变体)与 1570 种激酶抑制剂进行动态互作分析,鉴定出 232 种具有降解活性的抑制剂,形成 160 个特异性激酶 - 抑制剂降解对, HER2、ABL1、RAF1 (S257L) 是最易被降解的激酶。 降解活性与激酶的 HSP90 客户端属性显著相关(强 / 弱客户端降解率显著高于非客户端),但约 40% 的降解事件无法用 “分子伴侣剥夺” 解释。抑制剂诱导降解与 PROTACs 的降解谱无相关性,表明二者机制完全不同;突变体激酶与野生型的降解模式差异显著(Jaccard 距离≥0.8),提示突变可改变激酶的降解易感性。随后研究团队从筛选结果中挑出三个典型代表( LYN、BLK、RIPK2 ),它们的降解轨迹清晰、特异性强,作为后续机制研究的核心对象。
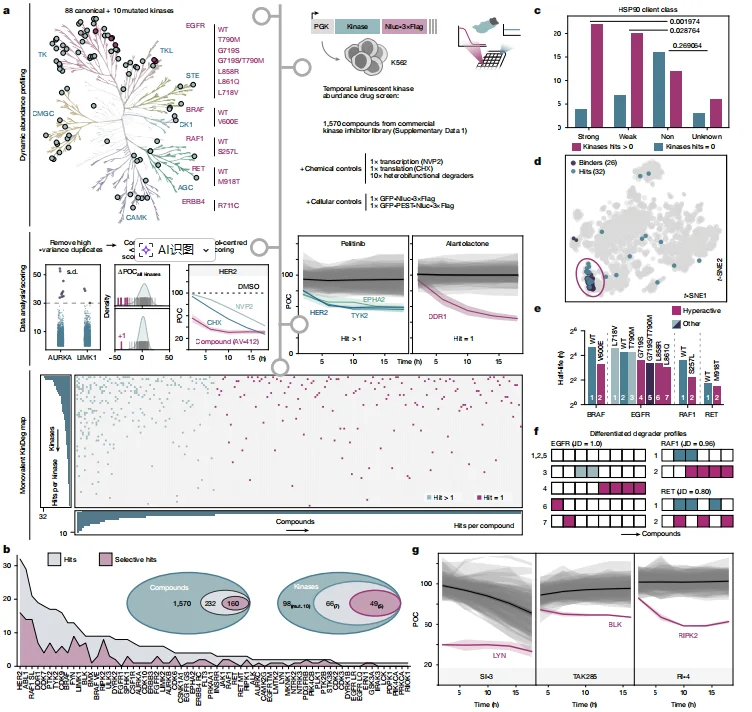
图1. 1,570种单价激酶靶向化合物的激酶降解(KinDeg)图谱
2. LYN 降解机制:抑制上游调控激酶,激活 “活性 - 稳定性开关”
抑制剂 SI-3 通过特异性抑制上游调控激酶 CSK,解除其对 LYN 的负调控,导致 LYN 激活并磷酸化(Y32/Y316 位点),形成双磷酸化降解信号(phosphodegron)。UPS 聚焦型 sgRNA 文库筛选显示, E3 泛素连接酶 CBL 是最强富集基因 (log₂[FC]>1.585,P<0.05),其同源蛋白 CBLB 同样显著富集,提示二者功能冗余。CBL 或 CBLB 单敲除无法阻断 SI-3 诱导的 LYN 降解,而双敲除可完全逆转降解效应,证实二者协同作用;CBL 介导蛋白酶体与溶酶体双途径降解,CBLB 仅依赖蛋白酶体途径。化学挽救实验显示,LYN 降解依赖泛素化(TAK285 可阻断),且同时依赖蛋白酶体和溶酶体通路,与 CBL/CBLB 的双途径降解特性一致;SI-3 处理后 CBL/CBLB 与 LYN 的相互作用显著增强。SI-3 通过优先抑制上游负调控激酶 CSK(K_D=34.60 nM),解除其对 LYN 的抑制,导致 LYN 激活并磷酸化 Y32/Y316 位点,形成双磷酸化降解信号(phosphodegron),双突变体 LYN (Y32A/Y316A) 可完全抵抗降解。
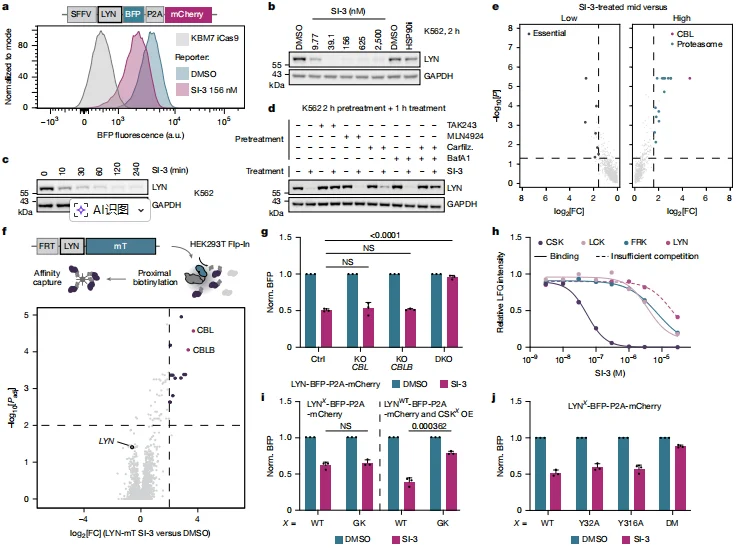
图2. LYN通过经典活性-稳定性转换机制被SI-3快速降解
3. BLK 降解机制:γ- 分泌酶介导膜定位改变,触发胞质降解
全基因组文库筛选后发现,γ- 分泌酶复合物的四个亚基(APH1A、NCSTN、PSEN1、PSENEN)全部高富集,说明 BLK 降解必须靠 γ- 分泌酶。 药理学抑制 γ- 分泌酶(DAPT 预处理)或基因敲除 PSENEN,可完全阻断 TAK285 诱导的 BLK 降解,而 HSP90 抑制剂诱导的 BLK 降解不受影响, 证实 γ- 分泌酶是 TAK285 特异性降解通路的关键。
TAK285 通过网络效应激活 γ- 分泌酶,切割 BLK N 端豆蔻酰化修饰,导致 BLK 从细胞膜转移至胞质并被降解;BLK 的 N 端 7 个氨基酸(含 G2、L3、V4、S6)是降解关键基序,替换该基序可使 SRC 激酶获得 TAK285 降解敏感性。AlphaFold3 结构预测显示,BLK N 端结构域嵌入 γ- 分泌酶活性位点,L3 残基位于疏水口袋,为降解依赖基序提供结构依据。
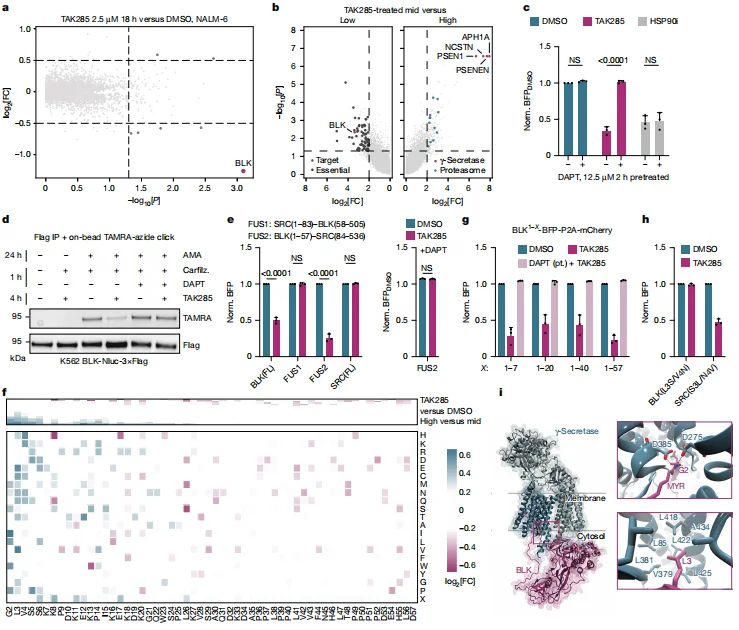
图3.BLK通过TAK285以 γ 分泌酶依赖性方式被降解
4. RIPK2 降解机制:诱导高阶组装体形成,启动自噬降解
全基因组 sgRNA 文库筛选显示,自噬通路关键基因(FIP200)、泛素样蛋白 TMUB1 及 E3 泛素连接酶 BIRC2(cIAP1)、XIAP 显著富集,且富集基因显著富集于溶酶体降解相关 GO 条目。
敲除自噬关键基因 FIP200 或抑制溶酶体酸化(巴佛洛霉素 A1),可显著阻断 RI-4 诱导的 RIPK2 降解;PSMB5 敲除无影响,证实降解依赖巨自噬而非蛋白酶体。TMUB1 敲除会延迟 RIPK2 高阶组装体(RIPosomes)的形成,进而抑制降解;RI-4 通过诱导 RIPK2 的 CARD 结构域依赖型组装,招募 SQSTM1(p62)等自噬相关蛋白,启动自噬降解。BIRC2/XIAP 双敲除或 RIPK2 的 I212D 突变(破坏与 IAP 的结合),会抑制 RIPK2 组装体的清除,证实泛素化修饰在组装体降解中的关键作用。
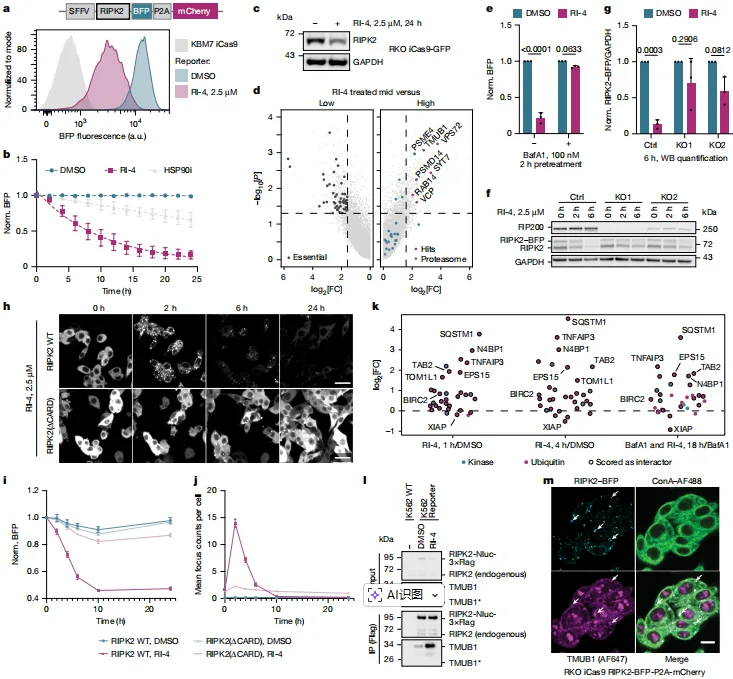
图4.RI-4通过TMUB1介导的多聚化和巨自噬作用使RIPK2失稳
文章小结
本研究通过系统性筛选与机制解析,证实单功能激酶抑制剂可通过诱导靶蛋白形成 “降解易感状态”,激活内源性降解通路实现选择性降解。研究明确了这类降解事件的普遍性与特异性,阐明了 LYN(活性调控)、BLK(定位改变)、RIPK2(高阶组装)三大代表性机制,建立了 “超级激活内源性降解” 的理论框架。这一发现不仅拓展了对小分子 - 靶蛋白互作的认知,更为靶向降解药物研发提供了 “无需双功能设计” 的全新范式,具有重要的临床转化价值。
源井生物CRISPR-iScreen™文库
CRISPR-iScreen™是源井生物自主研发的一项创新技术,旨在实现高效的CRISPR筛选。目前,源井生物拥有超过40种的CRISPR文库现货供应,覆盖人类、小鼠、绿猴及猪等物种的全基因组基因敲除/抑制/激活文库;此外,还有针对激酶、细胞周期、膜蛋白、代谢等相关基因构建的CRISPR敲除/抑制/激活亚文库,助您轻松实现靶点筛选!目前源井拥有150+文库病毒现货,400+文库Cell Pool现货,还提供一站式CRISPR文库(体内/体外)功能筛选服务,随时支持您的研究需求。
联系我们了解更多>>>参考文献
Scholes NS, Bertoni M, Comajuncosa-Creus A, Kladnik K, Guo X, Frommelt F, Hinterndorfer M, Razumkov H, Prokofeva P, Schwalm MP, Born F, Roehm S, Imrichova H, Santini BL, Barone E, Schätz C, Muñoz I Ordoño M, Lechner S, Rukavina A, Serrano I, Abele M, Koren A, Kubicek S, Knapp S, Gray NS, Superti-Furga G, Kuster B, Shi Y, Aloy P, Winter GE. Inhibitors supercharge kinase turnover through native proteolytic circuits. Nature. 2026 Jan;649(8098):1032-1041. doi: 10.1038/s41586-025-09763-9. Epub 2025 Nov 26. PMID: 41299171; PMCID: PMC12823440.










