IF=14.1|源井生物助力探索结直肠癌细胞外泌体向成纤维细胞传递PIK3CA突变促进肿瘤转移的机制


IF=14.1|源井生物助力探索结直肠癌细胞外泌体向成纤维细胞传递PIK3CA突变促进肿瘤转移的机制
2025年5月,中国医科大学方瑾教授团队在“ Advanced Science ”在线发表题为 Colorectal Cancer Cells–Derived Exosomal PIK3CA Mutation DNA Promotes Tumor Metastasis by Activating Fibroblast and Affecting Tumor Metastatic Microenvironment 的最新研究成果。该研究依托源井生物的技术支持,对携带 PIK3CA H1047R 突变的 LS174T 细胞进行基因编辑,将 3140 位核苷酸 G 突变为 A,使 1047 位 Arg 变为 His,构建 PIK3CA 野生型(WT)细胞系,并通过与 MT 细胞(原始突变细胞)比较,助力研究揭示结直肠癌细胞外泌体向成纤维细胞传递 PIK3CA 突变在肿瘤转移中的作用。

研究发现,结直肠癌(CRC)细胞外泌体中的 PIK3CA突变DNA 可以传递至受体成纤维细胞中,并在其中进行转录和翻译,最终通过与磷脂酰肌醇3激酶(PI3K)途径的内源性P85调节亚基相互作用,将成纤维细胞激活为癌症相关成纤维细胞(CAF)。CAF在体内外均能够促进肿瘤细胞转移并分泌高水平的IL6。此外,PIK3CA突变在原发部位和转移部位的CAF中均被检测到,表明它可能通过影响TME来促进肿瘤转移。同时,携带PIK3CA突变的CRC患者IL6分泌水平也升高并且更容易发生肿瘤转移。这些研究结果表明,同时检测血清来源的外泌体PIK3CA突变和血清IL6的分泌可能是一个有希望的CRC的诊断工具,以及同时靶向PIK3CA突变和IL6可能成为治疗CRC的新方法。
一、研究背景
细胞间通讯是促进肿瘤进展和转移的关键因素。肿瘤细胞来源的外泌体可以通过传递肿瘤特征性物质,靶向基质细胞影响肿瘤微环境的稳态进而参与肿瘤的进展和转移。大量研究显示,肿瘤在演进过程中,可以招募成纤维细胞诱导其成为肿瘤相关成纤维细胞(CAF),CAF通过分泌多种细胞因子和细胞外基质参与肿瘤微环境的重塑,进而在促进肿瘤细胞增殖、影响侵袭转移、促进化疗耐药等多方面来调节肿瘤的发展。
肿瘤细胞来源的外泌体还可通过活化成纤维细胞参与肿瘤微环境的形成,但目前的研究多集中于外泌体中蛋白质或RNA对肿瘤微环境的影响,而外泌体如何通过传递异常DNA影响肿瘤微环境的稳态进而参与肿瘤的转移和进展目前较少提及。尽管PIK3CA突变在肿瘤细胞中的作用已经基本阐明,但在肿瘤细胞中直接靶向PIK3CA突变对CRC转移的治疗效果不甚明显。
本研究目的旨在考虑PIK3CA突变DNA是否可以通过肿瘤外泌体向基质细胞传递的方式进一步促进CRC细胞发生转移。
二、研究结果
1. PIK3CA WT和MT细胞衍生的外泌体含有与亲代细胞相同的PIK3CA突变状态
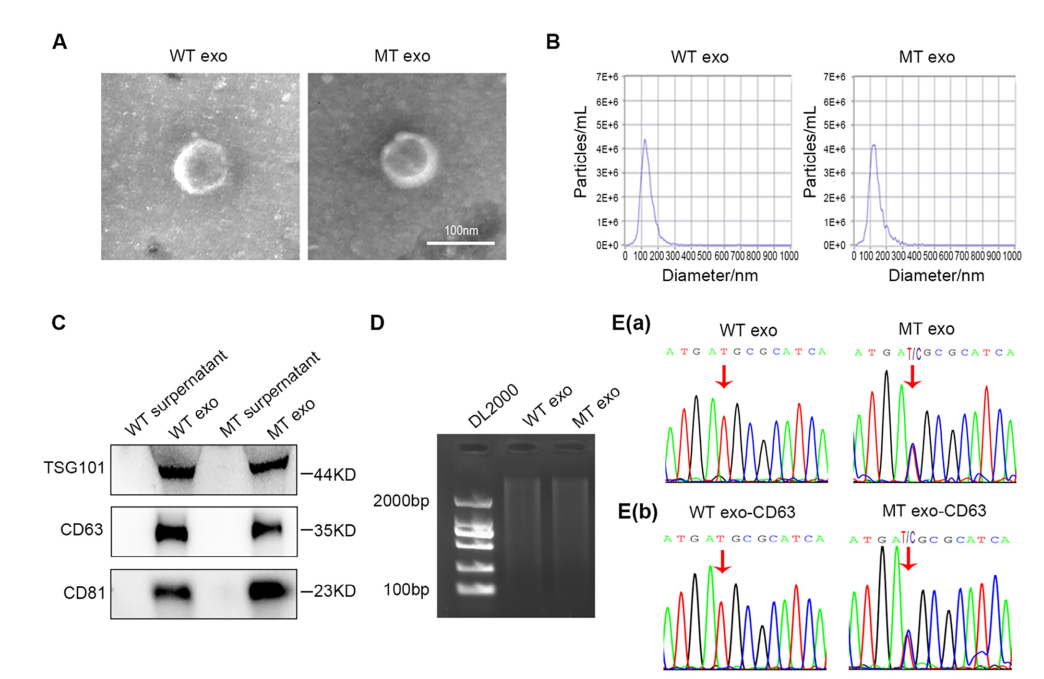
图1 WT和MT细胞来源的外泌体与亲代细胞具有相同的PIK3CA突变状态
研究首先证实MT细胞外泌体中含有PIK3CA突变,而WT细胞外泌体中则没有,说明外泌体中有与亲本细胞相同的PIK3CA突变状态。为了进一步确认提取到的 DNA是来源于外泌体而非其它细胞外囊泡形式,研究团队应用包被外泌体特异性标志物CD63抗体的磁珠和外泌体共孵育,再从孵育后的外泌体中提取DNA,确保提取到的DNA只来源于CD63阳性的外泌体。随后进一步确认MT细胞外泌体中有与亲本细胞相同的 PIK3CA突变。
2. MT细胞来源的外泌体中PIK3CA突变能够水平传递至成纤维细胞
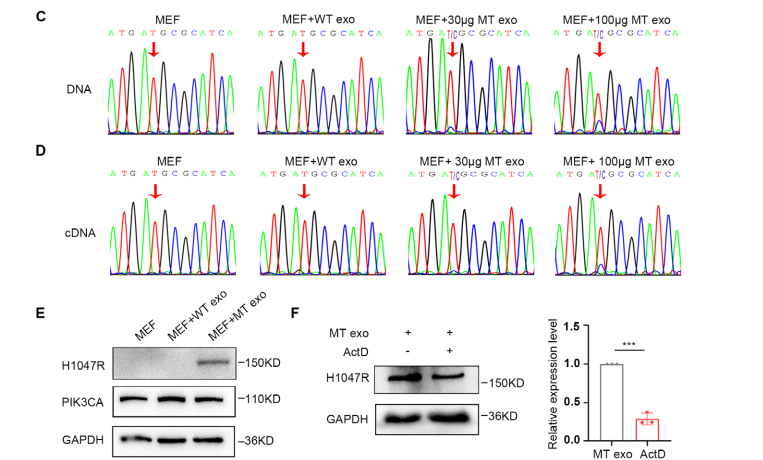
图2 PIK3CA H1047R突变在MT细胞来源的外泌体中向成纤维细胞的水平传递
为了进一步确认MT细胞外泌体中的PIK3CA突变能够被水平递送到 MEF细胞,研究团队将两种细胞的外泌体与MEF细胞共孵育,发现MT细胞外泌体中的PIK3CA突变DNA能够被水平递送到MEF细胞中并进行转录和翻译。随后为了排除外泌体RNA及蛋白传递的影响,将 MEF 细胞用转录抑制剂ActD和MT细胞来源的外泌体共孵育,发现75%的MEF细胞中突变蛋白的表达均由外泌体PIK3CA DNA水平传递而来,并起到主要作用。
3. 外泌体中PIK3CA突变能够激活MEF转化为CAF
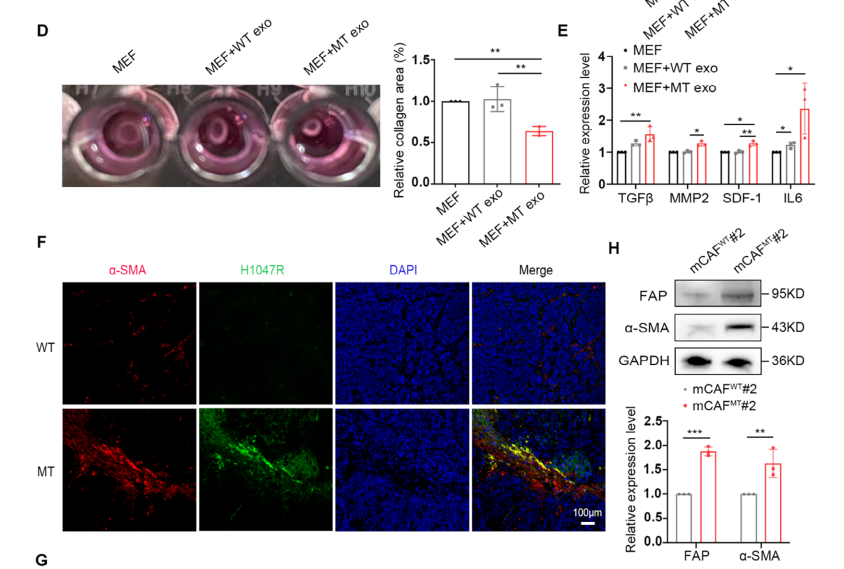
图3 外泌体中的PIK3CA H1047R突变可将小鼠胚胎成纤维细胞(MEFs)激活为癌相关成纤维细胞(CAFs)
MT细胞外泌体处理MEF细胞后,MEF 细胞的收缩能力和分泌细胞因子的能力显著增强,这提示MT细胞外泌体中PIK3CA突变的水平传递具有促进MEF细胞活化为CAF的潜能。体内实验也证实在CAF细胞中存在α-SMA和H1047R表达的共定位,这进一步证明了成纤维细胞的活化与PIK3CA突变的水平传递有关。
4. 外泌体 PIK3CA突变与CRC转移相关
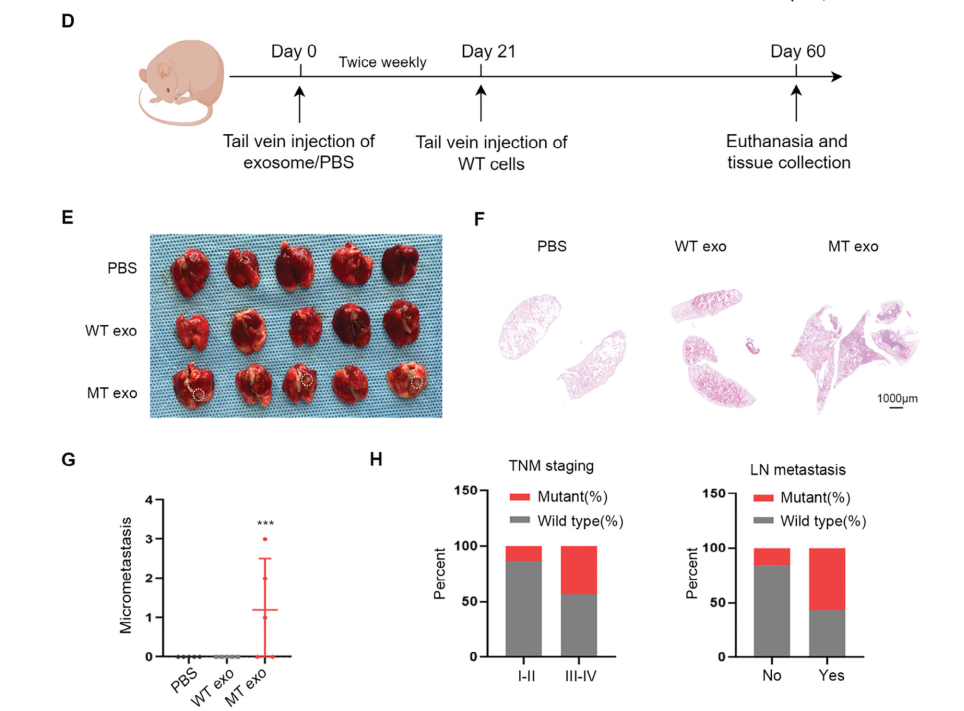
图4 外泌体PIK3CA H1047R突变与结直肠癌转移相关
外泌体还可以建立远端器官转移前微环境,为肿瘤从原发部位的远端转移创造条件。为了探究外泌体 PIK3CA DNA在转移前微环境形成中的潜在作用,研究团队通过尾静脉将WT细胞静脉注射到裸鼠体内,结果发现MT细胞源性外泌体组的肺组织中出现转移灶,这说明外泌体 PIK3CA DNA可以激活远端器官的成纤维细胞,最终促进肿瘤细胞从原发部位的扩散。在CRC患者体内,结果也提示外泌体PIK3CA DNA突变在临床上与CRC转移密切相关。
5. 外泌体PIK3CA突变的水平传播诱导CAF分泌高水平的IL6
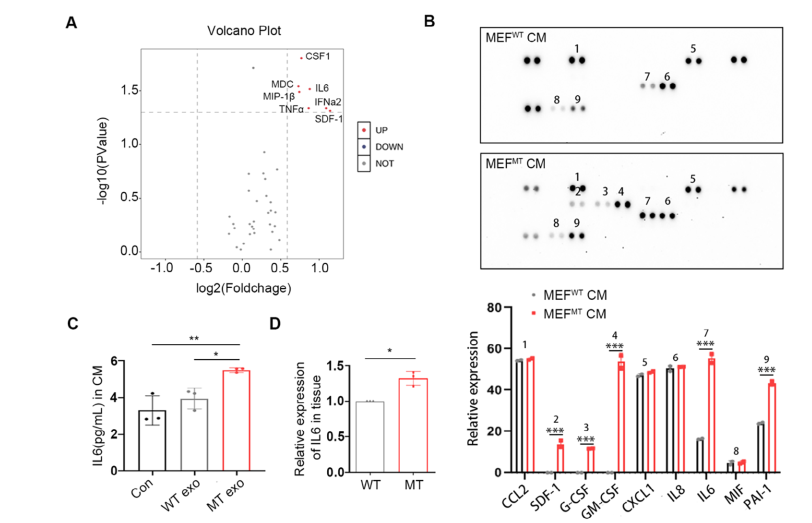
图5 外泌体PIK3CA H1047R突变的水平传播诱导癌相关成纤维细胞分泌更高水平的IL-6
CAF的主要作用是产生旁分泌细胞因子,进而促进肿瘤转移。研究团队使用olink分泌组测序以及细胞因子分析阵列系统对WT和MT细胞外泌体处理后的MEF细胞CM进行了分析,发现IL6水平明显升高。采用ELISA法和real time PCR进行验证得到了相同的结果。
6. CAF细胞通过IL6/IL6R/STAT3信号通路促进WT细胞转移
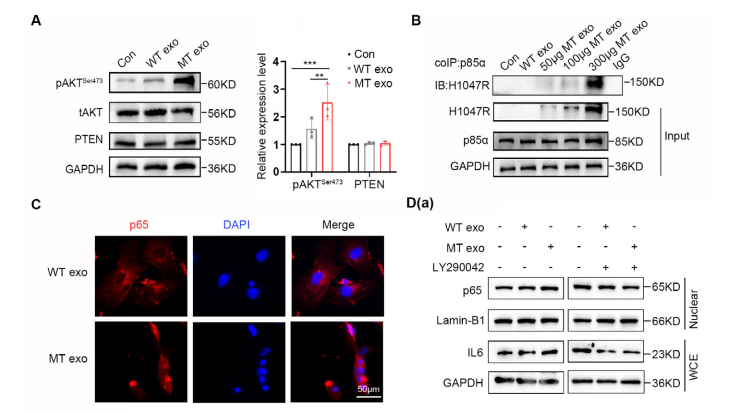
图6 CAFs通过IL6/JAK2/STAT3通路促进结直肠癌转移
进一步的机制研究发现,外泌体PIK3CA DNA 向 MEF 细胞水平传递通过 PI3K/NF-κB 通路将其活化为 CAF,CAF通过IL6/STAT3通路促进WT细胞转移。
研究意义与展望
揭示了独特现象: 发现外泌体PIK3CA DNA向成纤维细胞进行水平传递可以将成纤维细胞活化为CAF,进而促进肿瘤细胞转移。
明确了功能机制: 证实了CRC细胞外泌体中 PIK3CA突变的水平传递在影响肿瘤微环境稳态中的重要作用及促进CRC转移的可能分子机制,并揭示了PIK3CA突变和IL6的联合检测及靶向治疗,可能成为CRC诊断和治疗的新策略。
提供了临床线索: 证实CRC患者IL6的分泌水平与PIK3CA突变率相关,两者均与CRC转移密切相关。
展望未来,研究可进一步聚焦以下方向:
● 开发特异性靶向CAF中PIK3CA突变的抑制剂(如中和抗体、小分子抑制剂),探索其在CRC中的干预效果。
● 证实外泌体中的DNA向受体细胞传递的具体机制。
该研究不仅为理解肿瘤转移机制提供了新视角,也为CRC的早期检测与治疗开辟了新的可能路径。
源井生物提供的支持
在此次方瑾教授团队发表于Advanced Science的研究中,源井生物提供的 PIK3CA点突变的LS174T细胞模型为阐明外泌体源性PIK3CA突变在肿瘤微环境中传递的现象发挥了重要作用。
源井生物重磅推出 点突变细胞 DIY 套餐 !创新加入 HDR-U+分子,同源重组效率飙升至 84% , ¥4980 起即可轻松搞定细胞点突变实验。若想彻底解放双手,我们同步提供全流程 点突变细胞构建服务 ,低至 ¥1.58w ,让科研效率直线上升,聚焦核心研究不费心~
参考文献
Wang.R, Li, WM., lV, YQ. et al. Colorectal Cancer Cells–Derived Exosomal PIK3CA Mutation DNA Promotes Tumor Metastasis by Activating Fibroblast and Affecting Tumor Metastatic Microenvironment. Advanced Science 12,27 (2025). https://doi.org/10.1002/advs.202501792












