新抑癌基因 ECHS1 被发现!填补肝癌早期驱动机制空白


引言
肝细胞癌(HCC)是全球癌症致死主要病因,多数由肝硬化背景下的 发育不良结节(DN,癌前病变) 进展而来,约 30% DN 会恶变。中国科学院分子细胞科学卓越创新中心惠利健团队在 Cancer Cell 发表最新研究,该研究聚焦肝癌前病变(发育不良结节 DN)向极早期肝癌(veHCC)的恶性转化过程,通过 进化相关的结节内结节样本、 多组学测序与空间转录组技术,揭示了 TERT 突变启动癌变、拷贝数变异(CNA)主导恶性转化、免疫荒漠与免疫逃逸双进化模式 的核心机制,改写了肝癌起源于慢性炎症的传统认知,为肝癌早诊早治提供全新靶点。

研究背景
HCC 多从肝硬化背景下的异型增生结节(DN)发展而来,但驱动早期恶性转化的关键遗传与免疫机制仍不明确。既往研究多采用 进化无关 的癌前与癌组织,无法精准解析真实恶变轨迹;且普遍认为 HCC 起源于慢性炎症微环境,但 癌前病变的免疫特征、驱动恶变的关键基因组事件仍不明确。
研究目的
揭示 DN 向 veHCC 恶性转化的核心遗传驱动事件与免疫微环境重塑规律,定义早期致癌演化模式,为早诊与干预提供靶点。
研究方法
- 临床样本筛选 9 年间筛选 44714 例 FFPE 肝脏标本,获得 16 例患者的 17 个进化相关结节内结节样本(DN + 配对 veHCC),另纳入 19 例癌潜能未确定 DN作为对照。
- 多组学测序 全基因组测序(WGS,~35×)、RNA-seq、空间转录组(Visium HD)、多重免疫荧光 / 组化(IHC)。
- 基因操作与功能验证 人肝类器官模型、CRISPR 敲除 / 过表达、EdU 增殖实验。
- 生信分析 突变特征、拷贝数变异(CNA)、细胞类型反卷积(MCP-counter)、细胞通讯分析(SOAPy)、进化树构建(Pairtree)。
研究路线
- 样本鉴定: 确认结节内结节为进化相关的DN与veHCC。
- 癌前驱动筛选: 对比癌易感 / 未确定 DN,锁定TERT 突变为关键起始事件。
- 恶性转化驱动: 明确CNA 累积而非 SNV 是 DN→veHCC 的核心动力。
- 免疫景观解析: 发现 DN 为免疫荒漠表型,部分 veHCC 为炎症型 + 免疫逃逸表型。
- 空间定位: 空间转录组可视化免疫细胞与基质细胞的空间分布。
- 模型提出: 总结CNA 主导型与免疫逃逸型双进化路径。
主要结果
1. 鉴定进化相关的 DN 与 veHCC 样本
研究发现17 个癌易感 DN 与配对 21 个 veHCC 共享 7%~85% 体细胞 SNV,确认为 直系进化关系。 82% 癌易感 DN 存在 TERT 突变 (启动子突变 / HBV 整合 / 拷贝数增加),显著高于癌未确定 DN(32%)。TERT 突变上调 TERT 表达,但 端粒持续缩短 ,提示 TERT 突变是 启动癌变而非逆转端粒损耗。
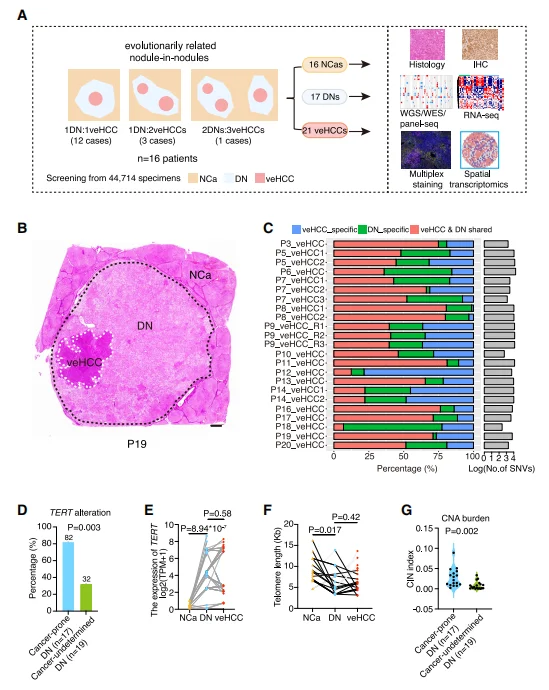
图1.样品采集与表征
2. CNA 是恶性转化的核心驱动事件
N→veHCC 过程中, 蛋白改变型 SNV 数量无显著增加,但CNA 负荷显著上升。 veHCC 特异性出现1p 染色体片段缺失(含 ARID1A、NR0B2 抑癌基因),伴随染色体不稳定性(CIN)升高。功能验证:ECHS1、FGA 敲除显著促进肝类器官增殖,证实其为早期恶变抑癌基因。
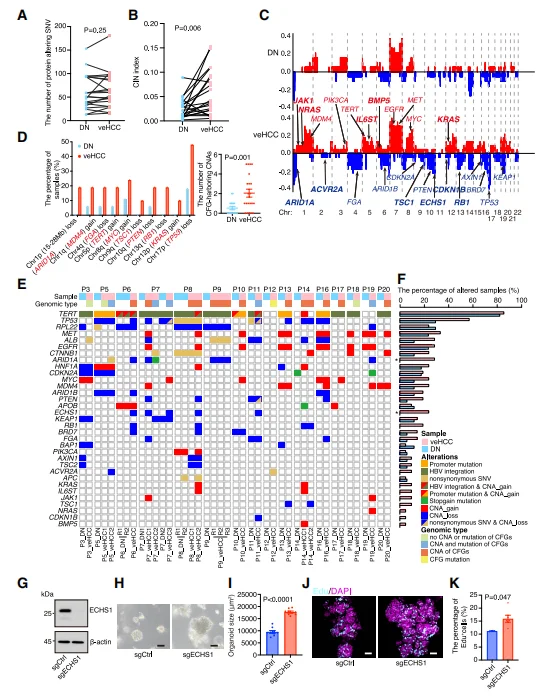
图2.导致DNs恶性转化的关键基因组改变
3. 癌前 DN 呈现 “免疫荒漠” 表型
癌易感 DN炎症通路全面下调(TNFα/NF-κB、IL6/JAK/STAT3),I 型干扰素、趋化因子、TLR 受体表达降低。免疫细胞浸润显著减少: 巨噬细胞、CD4+/CD8+ T 细胞、成纤维细胞、内皮细胞 均低于癌旁组织。结论: HCC 起源于免疫惰性微环境,而非慢性炎症, 颠覆传统认知。
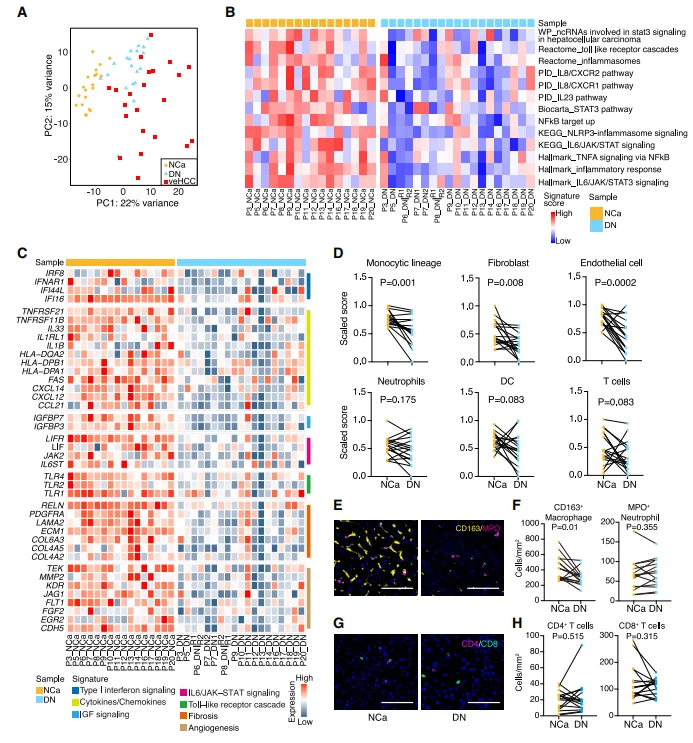
图3.癌前性DNs中的免疫荒漠表型
4. 炎症型 veHCC 同时存在免疫激活与免疫逃逸
43% veHCC 为炎症型:高浸润 T 细胞、树突状细胞(DC),但 CNA 负荷低。炎症型 veHCC 高表达 PD1/PDL1/CTLA4 、Treg 细胞富集、T 细胞耗竭特征显著。同时激活 IL6、TNFα、EMT、KRAS 等致癌通路,实现免疫逃逸 + 恶性进展同步发生。
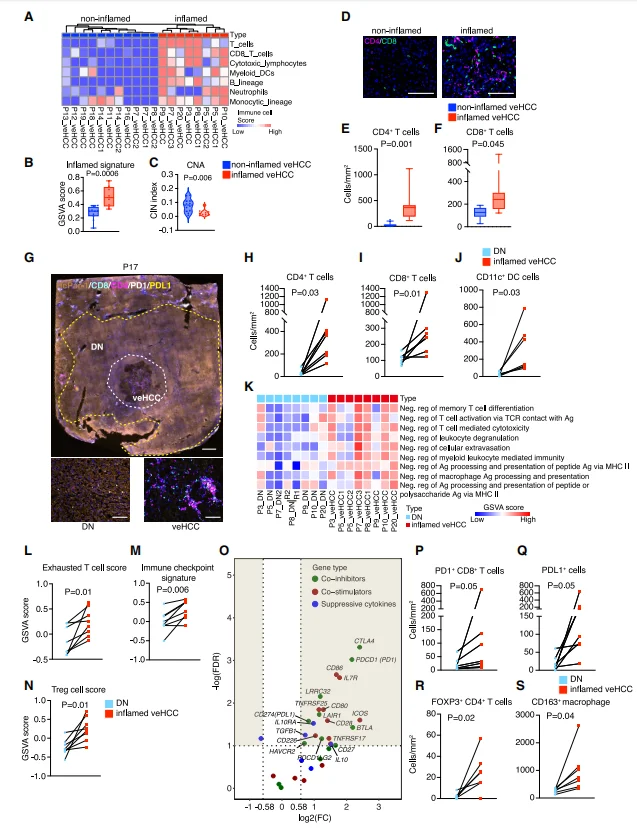
图4.部分病毒性肝细胞癌(veHCCs)中的适应性免疫激活与逃逸机制
5. 空间转录组揭示免疫抑制微环境的空间结构
CD8+ T 细胞与 CD4+ T 细胞、癌相关成纤维细胞(CAF)、巨噬细胞紧密空间互作。 CAF 通过TGF-β 通路介导免疫抑制,与 CD8+ T 细胞共定位区域呈现明显免疫耗竭。部分 veHCC 形成三级淋巴结构(TLS),与免疫逃逸型恶变相关。
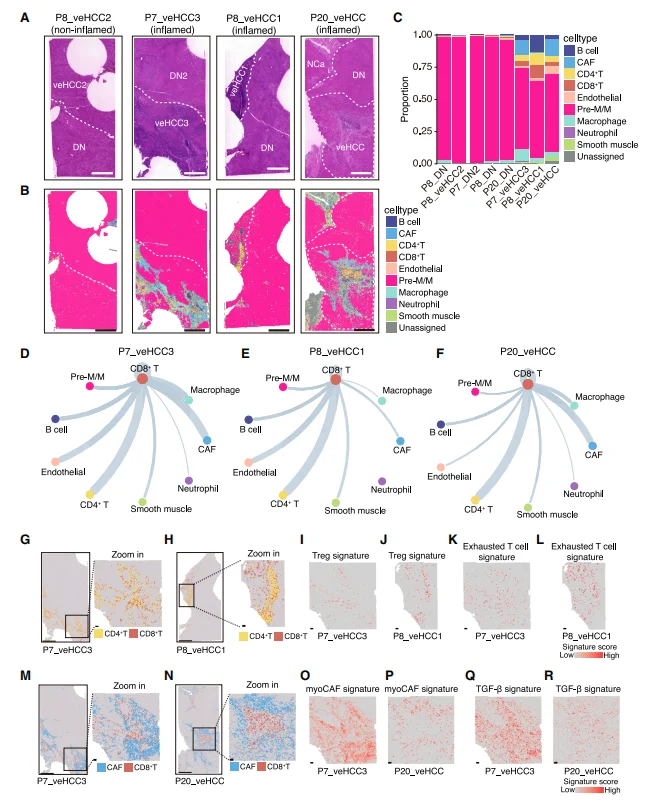
图5.免疫/基质细胞浸润、细胞间通讯及特征性激活的空间转录组学分析
6. 提出肝癌早期恶变双进化模型
基于基因组改变与免疫微环境特征,研究提出肝癌早期恶变存在两种平行进化模式,第一种为 拷贝数变异主导型进展, 以高染色体不稳定性、高拷贝数变异负荷和低免疫浸润为核心特征,TP53 异常改变在该模式中富集;第二种为 炎症型进展伴免疫逃逸, 以低拷贝数变异负荷、高免疫浸润和早期建立免疫逃逸程序为特征,部分病例甚至未出现新增驱动基因突变,此外同一患者体内可同时出现两种进化模式,证明肿瘤异质性在肝癌发生极早期就已形成。
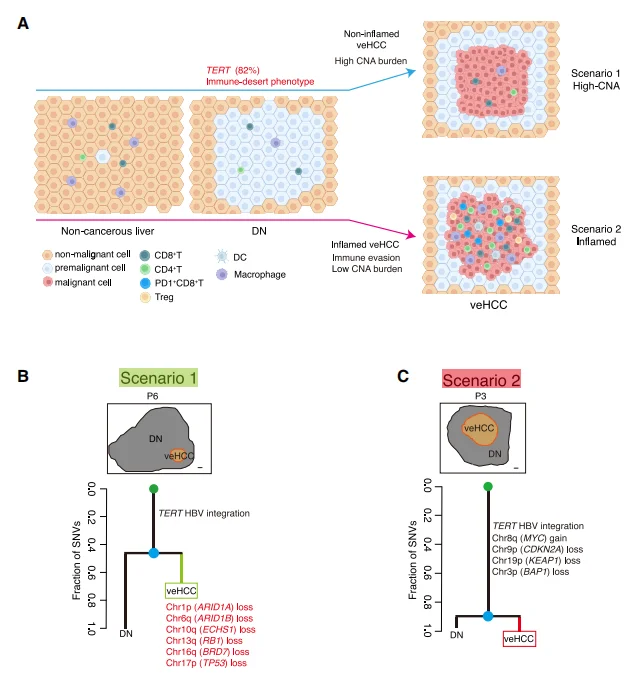
图6.DNs恶性转化的进化情景
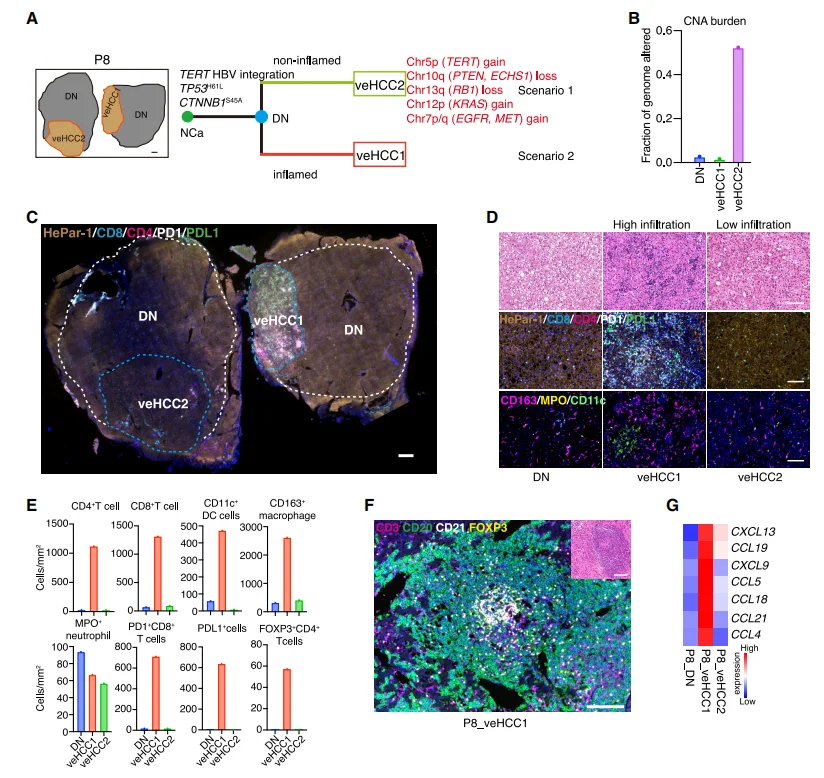
图7.P8的进化情景
研究意义与创新点
- 样本创新: 首次用进化相关结节内结节样本,精准解析肝癌早期恶变轨迹。
- 机制颠覆: 证实 HCC 起源于免疫荒漠而非慢性炎症,TERT 突变是起始事件,CNA 是恶性转化核心。
- 分型突破: 提出双进化模型,为早诊分层、靶向 / 免疫治疗提供依据。
- 靶点发现: 鉴定ECHS1、FGA为早期抑癌基因,TGF-β、免疫检查点为早期干预靶点。
文章小结
本研究通过进化相关的极早期肝癌样本,揭示了TERT 突变启动、CNA 驱动、免疫微环境重塑的肝癌早期恶变规律,提出 CNA 主导与免疫逃逸双进化模型,改写肝癌起源的传统理论,为肝癌 早筛、早诊、精准干预 提供全新分子基础与策略方向。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有11000+细胞产品(含8000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
ECHS1 基因编码的蛋白质在细胞代谢中扮演着关键角色。具体来说,这种蛋白质是一种短链烯酰辅酶A水合酶,主要 参与脂肪酸的β-氧化过程。 脂肪酸的β-氧化是细胞能量产生的重要途径之一,这意味着ECHS1基因的功能直接关系到细胞的能量供应。如果您也想针对 ECHS1 基因进行研究,井生物可为您提供ECHS1基因敲除细胞,涵盖Hep G2、HuH-7、LoVo等细胞系。如果您有个性化基因编辑的需要,欢迎咨询!
立即咨询源井生物技术专家 >>>>源井Luc细胞
源井生物提供超 300种 Luc细胞,经多篇 客户高分文献 引用验证,可稳定表达萤火虫(Firefly)的Luciferase荧光素酶, 特异性强且高度灵敏, 成像质量高,发光强度可精确定量,细胞株代次低、活性高、状态好,能够很好地帮助您进行转录因子调控机制研究、活体成像、细胞示踪等实验。











