技术前沿|编辑效率最高提升 16.2 倍!AcrIIA27 靶向 sgRNA 机制突破 CRISPR 编辑瓶颈


引言
CRISPR-Cas 系统是原核生物的适应性免疫系统,噬菌体进化出抗 CRISPR(Acr)蛋白实现对其的抑制。目前已发现多种 Acr 蛋白通过不同机制抑制 CRISPR-Cas 活性,但靶向 sgRNA 的抑制机制尚未被深入揭示。哈尔滨工业大学黄志伟团队在Nature Structural & Molecular Biology发表最新研究成果,研究通过冷冻电镜解析AcrIIA27与 SpyCas9-sgRNA 复合物的结构,阐明 AcrIIA27 靶向 sgRNA 抑制 Cas9 的分子机制,并基于该机制 提出 PTP RNA 截短策略,显著提升 CRISPR-Cas9 及 TnpB 系统的基因编辑效率与特异性。

研究背景
CRISPR-Cas 系统广泛存在于细菌和古菌中,通过识别并切割入侵的核酸发挥免疫功能。噬菌体为对抗该系统,进化出多种 Acr 蛋白。已报道的 Acr 蛋白抑制机制主要包括干扰 CRISPR-Cas 复合物组装、阻止靶标核酸结合、抑制核酸切割活性等。目前发现的广谱性 Acr 蛋白多靶向 Cas 蛋白的保守结构域,但靶向 sgRNA 实现广谱抑制的 Acr 蛋白尚未被报道。同时,CRISPR-Cas9 及新型编辑器(如 TnpB)存在编辑效率不足、脱靶效应等问题,限制了其应用。探索 Acr 蛋白的抑制机制,有望为优化基因编辑工具提供全新策略。
研究目的
本研究通过解析 AcrIIA27 与 SpyCas9-sgRNA 复合物的冷冻电镜结构,揭示 AcrIIA27 靶向 sgRNA 抑制 Cas9 活性的分子机制,并基于该机制开发提升 CRISPR-Cas 及 TnpB 系统编辑效率的通用策略。
研究路线
- 结构解析: 纯化 SpyCas9-sgRNA-AcrIIA27 复合物,通过冷冻电镜解析其三维结构,确定 AcrIIA27 与 sgRNA 的结合位点。
- 机制验证: 通过点突变、BLI、体外切割实验,验证 AcrIIA27 关键氨基酸残基在结合 sgRNA 及抑制 Cas9 活性中的作用;通过结构比对,阐明其造成空间位阻阻止底物 DNA 结合的机制。
- 广谱性检测: 选取 II-A、II-B、II-C 型 Cas9 同源蛋白,检测 AcrIIA27 对其的抑制活性,明确其广谱抑制特性。
- 编辑工具优化: 基于 AcrIIA27 结合的 sgRNA 区域(PTP RNA),设计截短型 sgRNA/reRNA,在 HEK293F 细胞中验证其对 Cas9 及 TnpB 编辑效率和特异性的提升作用。
- 机制阐释: 结合细胞实验与结构分析,提出 PTP RNA 截短通过消除非特异性蛋白结合、减少空间位阻提升编辑效率的机制。
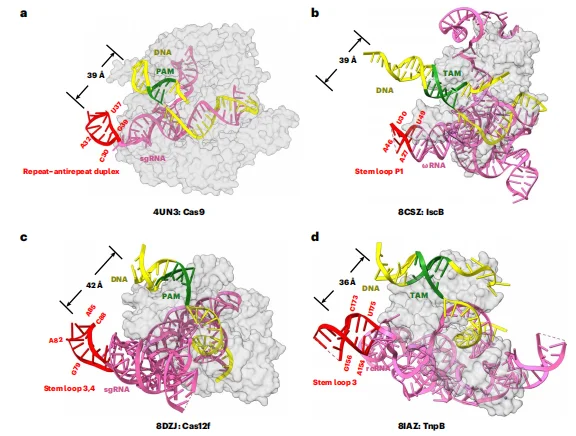
PTP RNA截短策略在多种编辑系统中的应用
主要结果
1.SpyCas9-sgRNA-AcrIIA27 三元复合物结构特征
冷冻电镜结构显示,SpyCas9 呈典型的双叶结构(识别叶 REC 和核酸酶叶 NUC),AcrIIA27 以 1:1 的化学计量比结合在 SpyCas9-sgRNA 复合物上,主要与 sgRNA 的重复 - 反重复双链区域(G21-U45)相互作用,同时与 SpyCas9 的 REC1 和 WED 结构域有少量接触。AcrIIA27 具有独特的折叠方式,包含 3 条 β- 折叠、2 个 α- 螺旋和 3 个环结构(loop1-3),其表面带正电区域嵌入 sgRNA 的沟区,通过静电相互作用和氢键稳定结合。
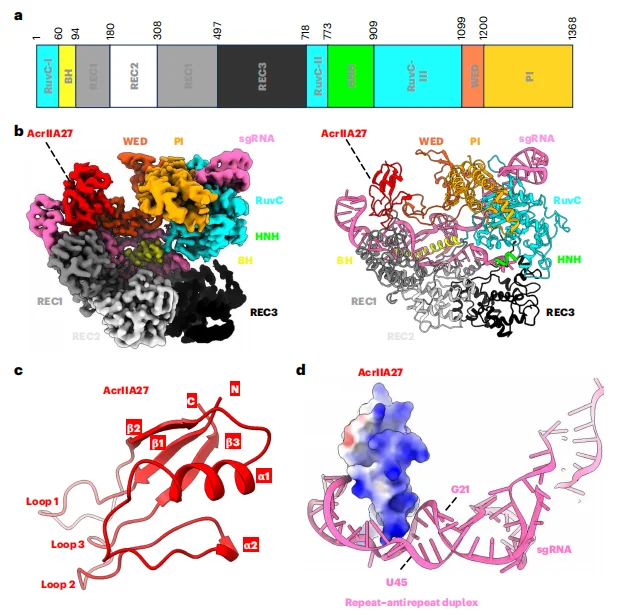
图1.SpyCas9–sgRNA–AcrIIA27三元复合物的冷冻电镜结构
2.AcrIIA27 通过 loops 区域特异性结合 sgRNA
Loop1 的带正电残基(H17、R67、R71、R72)与 sgRNA 的 U24、A26 等核苷酸的磷酸骨架形成静电相互作用;Loop2 的 S48、K50、W51 等残基与 U37、A38 的磷酸骨架形成氢键。BLI 实验证实,野生型 AcrIIA27 与 SpyCas9 的 sgRNA 结合亲和力极强(KD < 1 pM),而 Loop1 和 Loop2 关键残基突变后(如 R66A、R67A),结合亲和力下降超过 10 倍。体外切割实验显示,关键残基突变的 AcrIIA27 对 SpyCas9 的抑制活性显著降低甚至完全丧失;噬菌体噬斑实验进一步验证,这些突变体无法恢复 T5 噬菌体的存活能力。
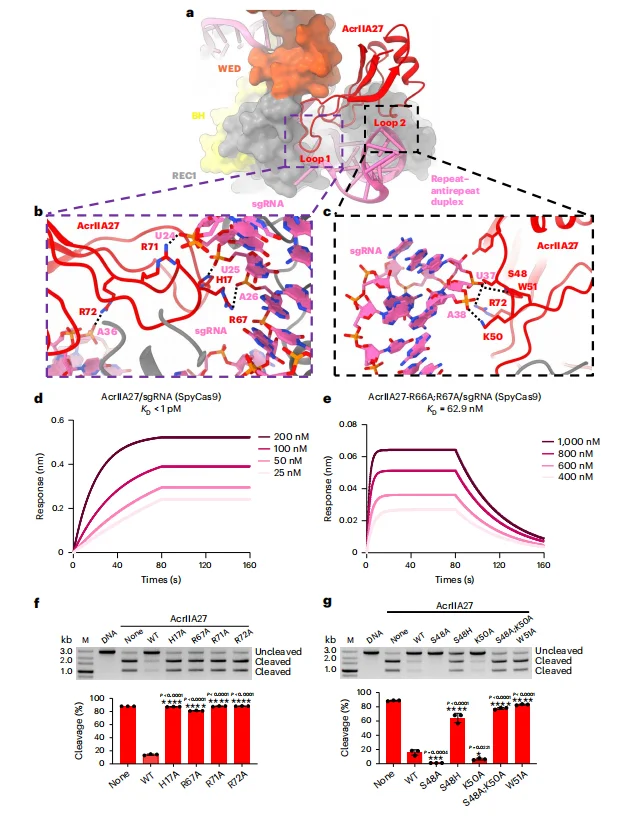
图2.AcrIIA27对sgRNA的识别
3.AcrIIA27 对多种 Cas9 同源蛋白具有广谱抑制活性
系统发育树分析显示,选取的 Cas9 同源蛋白覆盖 II-A(SpyCas9、SauCas9、FrCas9)、II-B(FnCas9)、II-C(Nme1Cas9、Nme2Cas9、GeoCas9)型。体外 DNA 切割实验表明,AcrIIA27 能够有效抑制 II-A 和 II-C 型 Cas9 的活性,对 SpyCas9 的抑制效果优于 AcrIIA4 等特异性抑制剂;但对 II-B 型 FnCas9 无抑制作用。BLI 实验证实,AcrIIA27 与 SauCas9、Nme1Cas9 的 sgRNA 均具有较高结合亲和力,关键残基突变会显著削弱其抑制活性,表明其广谱抑制依赖于与 sgRNA 的结合。
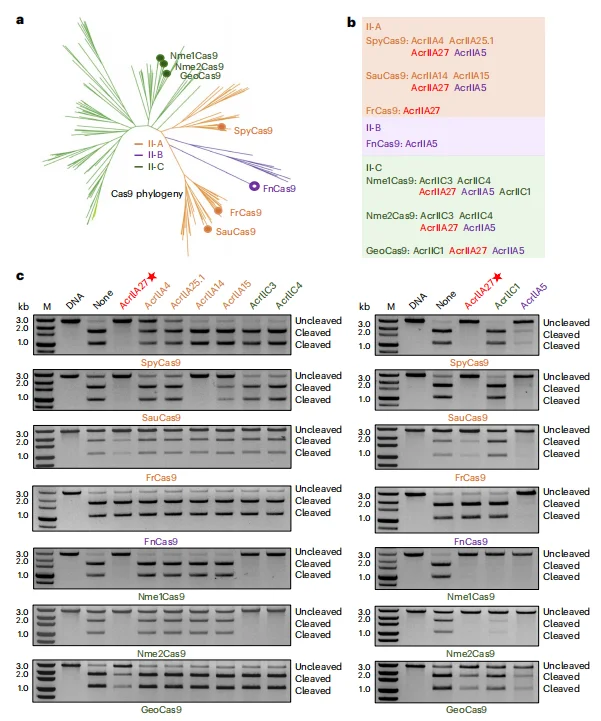
图3.AcrIIA27可抑制II-A型和II-C型Cas9的同源蛋白
4.AcrIIA27 通过空间位阻阻止底物 DNA 结合 Cas9
结构比对发现,AcrIIA27 的 N54-T59 区域与底物 DNA 的 PAM 邻近序列空间位置重叠。体外切割实验显示, 截短 N54-T59 的 AcrIIA27 完全丧失对 SpyCas9 的抑制活性,但其与 sgRNA 的结合亲和力未受影响;截短 sgRNA 上 AcrIIA27 结合的茎环区域(G29-C40)后,AcrIIA27 的抑制作用显著减弱,而 SpyCas9 的切割活性不受影响, 证实 AcrIIA27 通过空间位阻抑制底物 DNA 结合。
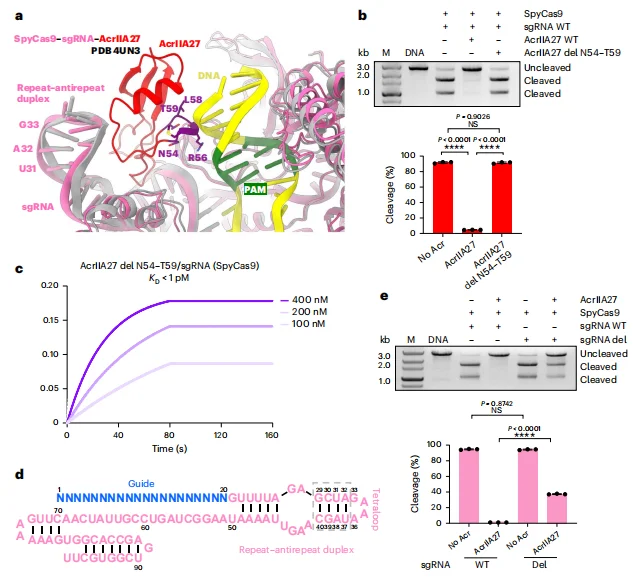
图4.AcrIIA27对SpyCas9的抑制机制
5.PTP RNA 截短策略显著提升基因编辑效率与特异性
针对 SauCas9 的 sgRNA,截短其 PAM 邻近的 PTP RNA 区域(U35-A60)后,在 HEK293F 细胞的多个内源基因位点(如 EMX1、GRIN2B)的编辑效率提升 1.2-2.1 倍。 针对 IS607 TnpB 系统的 reRNA,截短其 TAM 邻近的 PTP RNA 区域(茎环 3 的 MS1 位点)后,在 EMX1、DNMT1 等位点的编辑效率提升 1.5-6.1 倍。脱靶效应分析显示,截短型 PTP RNA 在提升编辑效率的同时,降低了脱靶位点的编辑水平,且编辑效率提升与 reRNA 表达水平无关。 该策略在 ISRin、ISAre 等 TnpB 同源蛋白中同样有效,部分位点编辑效率提升超过 16 倍。
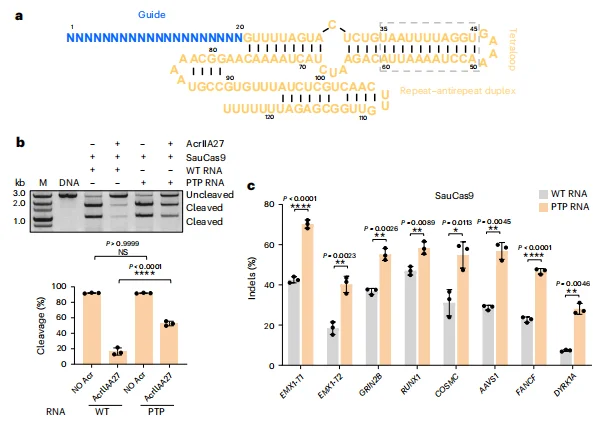
图5.PAM近端RNA截短可提高基因组编辑效率
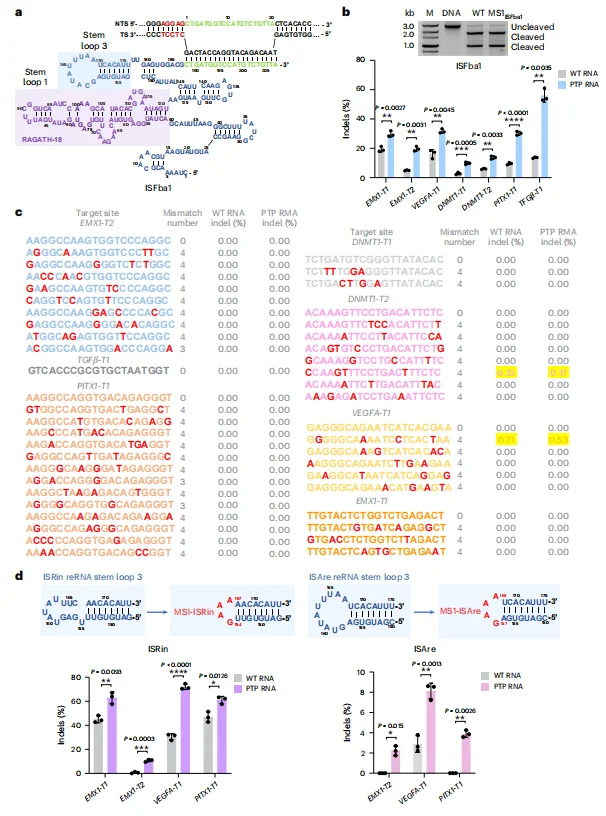
图6.TAM近端RNA截短可提高基因组编辑效率
研究意义与创新点
-
理论意义 首次发现并阐明 AcrIIA27 靶向 sgRNA 的磷酸骨架抑制 Cas9 活性的分子机制,拓展了 Acr 蛋白的抑制模式分类,为筛选新型 Acr 蛋白提供了新方向(如聚焦 RNA 结合蛋白家族)。揭示了 sgRNA 的溶剂暴露区域(PTP RNA)易与细胞内带正电蛋白发生非特异性结合,从而影响编辑效率的现象,为理解 CRISPR 系统的细胞内调控机制提供了新视角。
-
应用价值 提出的 PTP RNA 截短策略具有通用性,可显著提升 CRISPR-Cas9 及 TnpB 等紧凑型编辑器的基因编辑效率与特异性,且无需改造 Cas 蛋白,简化了编辑工具的优化流程。截短后的 sgRNA/reRNA 长度缩短,有助于提升腺相关病毒(AAV)等载体的递送效率,推动基因编辑技术在体内治疗中的应用。
-
技术创新 突破了 Acr 蛋白靶向 Cas 蛋白的传统认知,首次报道靶向 sgRNA 实现广谱抑制的 Acr 蛋白,为开发可调控的基因编辑工具提供了新靶点。从 Acr 蛋白的抑制机制反向推导,提出编辑工具优化策略,实现了基础研究向应用技术的快速转化。
文章小结
本研究通过冷冻电镜结构解析和生化功能验证,阐明了 AcrIIA27 靶向 sgRNA 的 PTP RNA 区域,通过空间位阻抑制 Cas9 活性的分子机制。 基于该机制设计的 PTP RNA 截短策略,能够有效消除非特异性蛋白结合带来的空间位阻,显著提升 CRISPR-Cas9 及 TnpB 系统在人细胞中的基因编辑效率与特异性。 该研究不仅丰富了抗 CRISPR 蛋白的作用机制,更为开发高效、精准的基因编辑工具提供了全新的优化思路,具有重要的理论意义和应用价值。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有11000+细胞产品(含8000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。针对点突变细胞,源井生物自研EZ-HRexTM技术,转染后细胞HDR效率提高至84%。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
未来,源井生物也将不断创新技术,提高编辑效率,为大家提供更优质、高效的科研服务!
联系我们了解更多>>>参考文献
Yu L, Yin M, Zhu Y, Lu Z, Xiao B, Zhou F, Yu Y, Huang Z. An anti-CRISPR targets the sgRNA to block Cas9 and guides the design of enhanced genome editors. Nat Struct Mol Biol. 2026 Jan 19. doi: 10.1038/s41594-025-01741-z. Epub ahead of print. PMID: 41555077.










