研究前沿|核心机制破解:m⁶A 阅读器 YTHDF1 通过调控 NOTCH1 翻译驱动结直肠癌干细胞干性与化疗耐药


引言
结直肠癌(CRC)是全球第三大常见恶性肿瘤,也是第二大致死性癌症,化疗耐药与肿瘤复发是改善患者预后的主要障碍,而癌症干细胞(CSCs)被认为是驱动化疗耐药和肿瘤复发的核心因素。N⁶-甲基腺苷(m⁶A)修饰作为真核生物中最主要的表观遗传调控机制之一,在肿瘤发生发展中发挥关键作用。香港中文大学于君、黄子隽团队在Signal Transduction and Targeted Therapy 杂志上发表最新研究,研究通过多队列临床样本分析、Lgr5 特异性转基因小鼠模型、癌细胞系及类器官实验,系统揭示了 m⁶A 阅读器 YTHDF1 通过 m⁶A 依赖方式结合 NOTCH1 mRNA 的 3'UTR 并促进其翻译,进而增强结直肠癌干细胞干性、促进肿瘤发生并诱导化疗耐药的分子机制。同时,研究证实 靶向 YTHDF1与化疗药物联用可显著提升治疗效果,为克服结直肠癌化疗耐药提供了全新的治疗策略。

研究背景
结直肠癌的临床治疗面临巨大挑战,约 38.5% 的 II-III 期患者在手术联合辅助化疗后仍会复发,转移性结直肠癌患者的化疗响应率亦不理想。化疗药物主要针对高增殖肿瘤细胞,但 CSCs 凭借其自我更新能力可逃避化疗杀伤,成为肿瘤复发的 “种子细胞” 。m⁶A 修饰通过 “ writers”“erasers” 和 “readers” 调控 mRNA 的剪接、翻译和降解,在肿瘤发生中扮演多重角色。 YTHDF1 作为关键的 m⁶A 阅读器,已被证实与结直肠癌的发生发展相关, 但其一 CSC 特异性功能、体内调控机制及在化疗耐药中的作用尚未明确,尤其缺乏基于体内肿瘤微环境的系统性研究。因此,阐明 YTHDF1 在结直肠癌干细胞中的调控网络,对于开发新型靶向治疗策略具有重要意义。
研究目的
本研究旨在明确 m⁶A 阅读器 YTHDF1 在结直肠癌干细胞干性维持与化疗耐药中的作用,揭示其通过调控下游靶基因影响结直肠癌发生发展的分子机制,并验证靶向 YTHDF1 联合化疗在结直肠癌治疗中的潜在应用价值。
研究方法
- 多队列验证: 纳入 6 个独立临床队列(N=184、151、550 等),通过组织芯片(TMA)、qPCR、Western blot 及公共数据库分析,检测 YTHDF1 与 CSC 标志物(CD133、LGR5)及 NOTCH1 的表达相关性,评估 YTHDF1 与化疗响应的关联。
- 转基因小鼠构建: 建立 Lgr5 特异性 Ythdf1 敲入(Ythdf1cki)和敲除(Ythdf1cko)小鼠模型,与 ApcMin/+ 小鼠杂交构建自发性结直肠癌模型,或经 AOM/DSS 诱导构建化学致癌结直肠癌模型。
- 细胞模型: 采用结直肠癌干细胞系(CSC28、LS174TS、POP66)及 HEK293T 细胞,通过过表达 / 敲低 YTHDF1、突变 YTHDF1 的 m⁶A 结合域(K395A/Y397A),验证其功能依赖性。
- 功能验证: 通过极限稀释实验(LDA)检测干细胞自我更新能力;流式细胞术检测凋亡水平;Western blot 检测干细胞标志物、NOTCH1 通路及 DNA 损伤标志物(p-H2AX)表达。
- 机制验证: 通过 MeRIP-qPCR、RIP-qPCR、RNC-qPCR 验证 YTHDF1 与 m⁶A 修饰 NOTCH1 的结合及翻译调控作用;构建 NOTCH1 3'UTR 双荧光素酶报告载体(野生型及 m⁶A 位点突变型),验证调控特异性。
- 药物干预: 使用 VNP 包裹的 siYTHDF1(纳米颗粒递送系统)或 YTHDF1 特异性抑制剂丹酚酸 C(SAC),在细胞系、类器官及小鼠异种移植模型中,评估单独或联合 OXA/5-FU 的治疗效果。
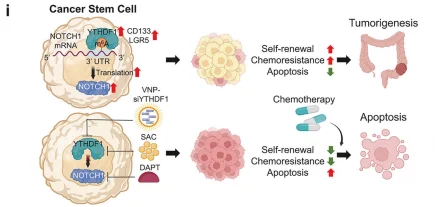
YTHDF1诱导CSC化疗耐药的机制
研究路线
- 临床关联发现: YTHDF1 表达与结直肠癌患者 CSC 标志物(CD133、LGR5)表达正相关,且与化疗耐药相关(多队列临床样本 + TCGA 数据 + 单细胞 RNA 测序验证)。
- 功能验证: YTHDF1 过表达增强结直肠癌干细胞干性、促进肿瘤发生及化疗耐药,敲低则逆转该表型(CSC 细胞系 + 患者来源类器官 + Lgr5 特异性转基因小鼠模型)。
- 机制解析: YTHDF1 以 m⁶A 依赖方式结合 NOTCH1 mRNA 的 3'UTR,促进其翻译并激活 NOTCH 信号通路,进而抑制细胞凋亡与 DNA 损伤,增强干细胞干性与化疗耐药(MeRIP-seq/RNA-seq/Ribo-seq 多组学分析 + 互作实验 + 双荧光素酶报告实验)。
- 治疗验证: VNP 包裹的 siYTHDF1 或 YTHDF1 特异性抑制剂丹酚酸 C(SAC)可靶向抑制 YTHDF1,联合奥沙利铂或 5 - 氟尿嘧啶能显著抑制肿瘤生长,提升化疗疗效(细胞 + 小鼠移植瘤模型 + 类器官实验)。
- 临床转化: YTHDF1 可作为结直肠癌化疗响应的预后生物标志物,靶向 YTHDF1 联合化疗为克服结直肠癌化疗耐药提供全新治疗策略(临床队列关联分析 + 治疗安全性验证)。
主要结果
-
YTHDF1 与结直肠癌干细胞干性正相关
临床样本中,YTHDF1 的 mRNA 及蛋白水平与 CSC 标志物 CD133、LGR5 呈显著正相关(P<0.001),且在 CD133+/LGR5+ CSC 亚群中高表达。细胞实验中, YTHDF1 过表达显著增强 CSC 自我更新能力、球囊形成能力及体内成瘤潜能,而敲低 YTHDF1 或突变其 m⁶A 结合域则完全逆转该效应。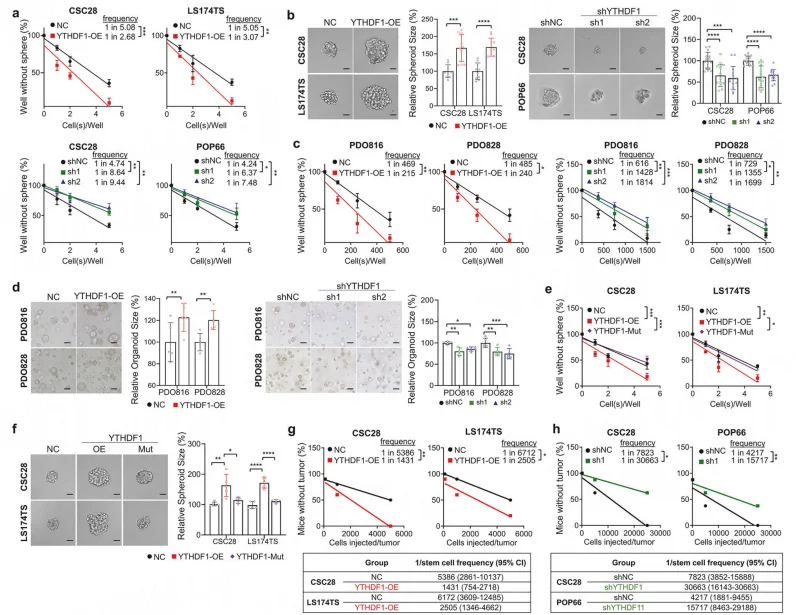
图1.YTHDF1以m6A依赖性方式促进自我更新能力。
-
YTHDF1 通过 m⁶A-NOTCH1 轴调控结直肠癌发生
多组学分析显示, NOTCH1 是 YTHDF1 的关键下游靶基因 ,其 3'UTR 存在 m⁶A 修饰位点,YTHDF1 可直接结合该区域并促进 NOTCH1 翻译(不影响 mRNA 水平)。动物实验中,Ythdf1cki 小鼠的肿瘤数量、负荷显著增加(P<0.05),NOTCH1 下游靶基因(HES1、HEY1)表达上调,而 Ythdf1cko 小鼠则呈现相反表型;DAPT 处理可显著抑制 Ythdf1cki 小鼠的肿瘤发生(P<0.01)。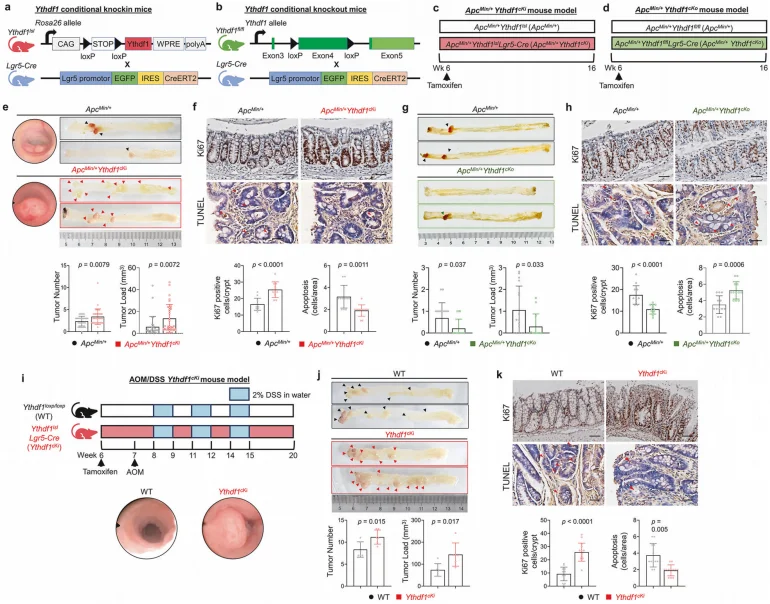
图2.Lgr5特异性Ythdf1条件性敲入小鼠加速结直肠肿瘤发生
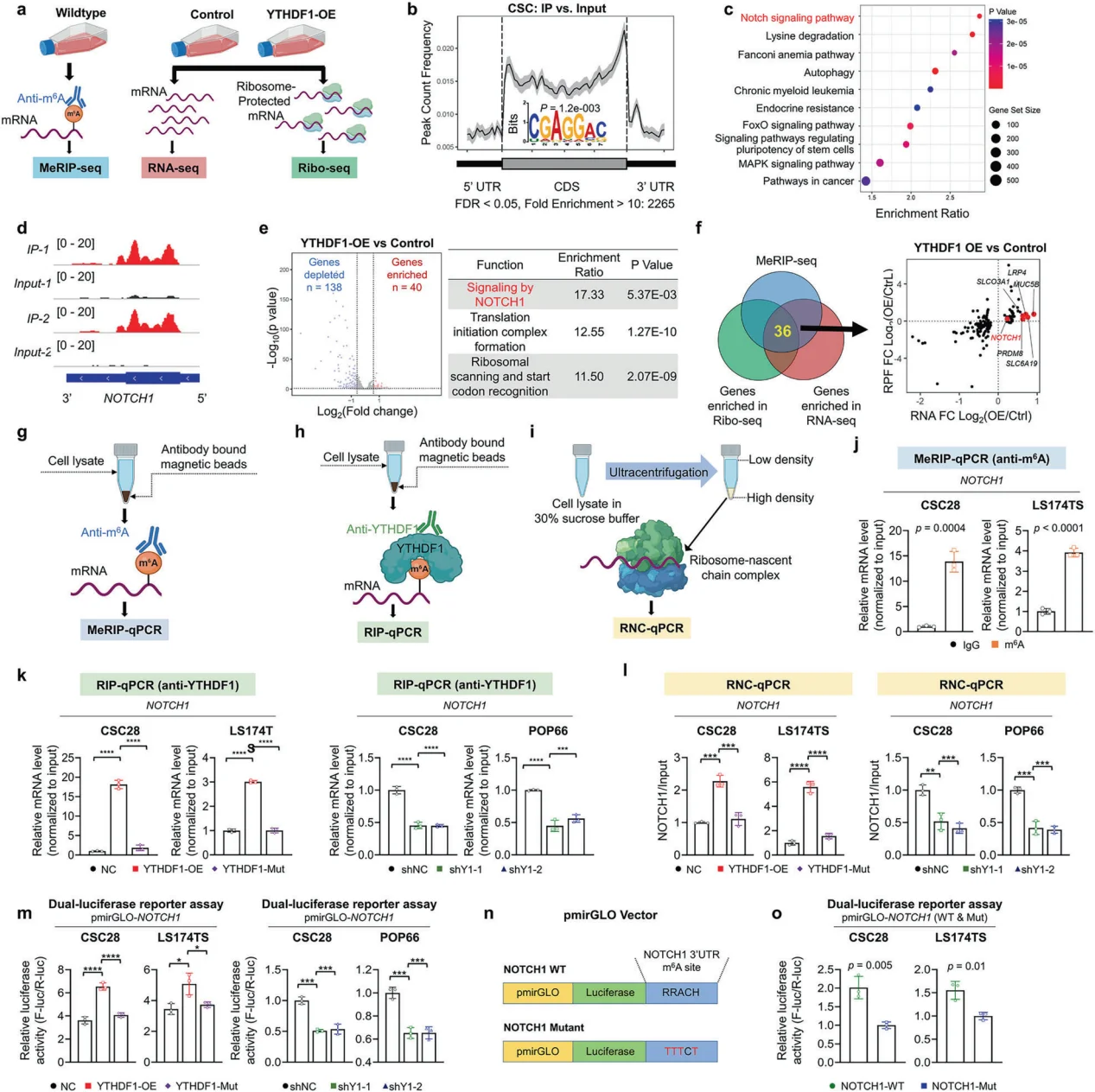
图3.多组学分析揭示NOTCH1是YTHDF1的下游靶点
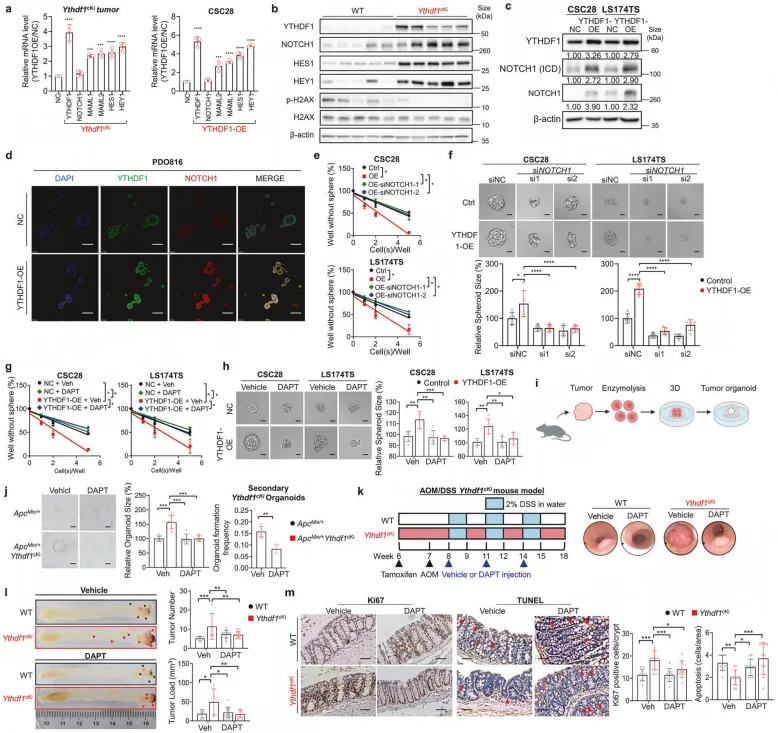
图4.NOTCH1是YTHDF1促进干细胞特性和肿瘤发生的功能靶点
-
YTHDF1 促进结直肠癌化疗耐药
体外实验中,YTHDF1 过表达显著提高 CSC 及类器官对 OXA、5-FU 的 IC50 值,抑制化疗诱导的凋亡及 DNA 损伤(p-H2AX 水平降低);敲低 YTHDF1 则增强化疗敏感性。体内实验中, Ythdf1cki 小鼠对 OXA、5-FU 化疗完全耐药,肿瘤增殖无明显抑制; 而野生型小鼠化疗后肿瘤数量及负荷显著降低(P<0.001)。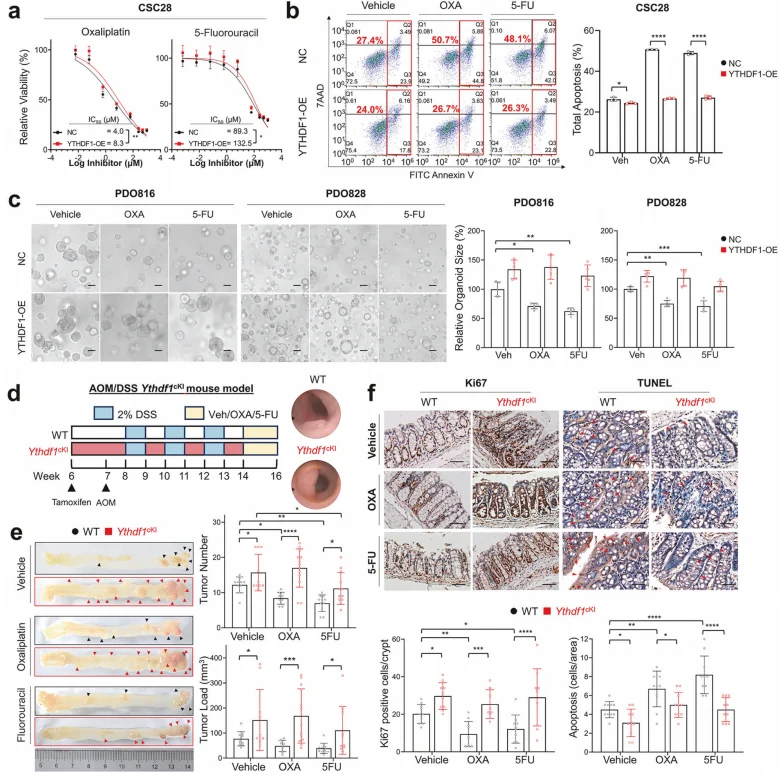
图5.YTHDF1过表达促进结直肠癌的化疗耐药性
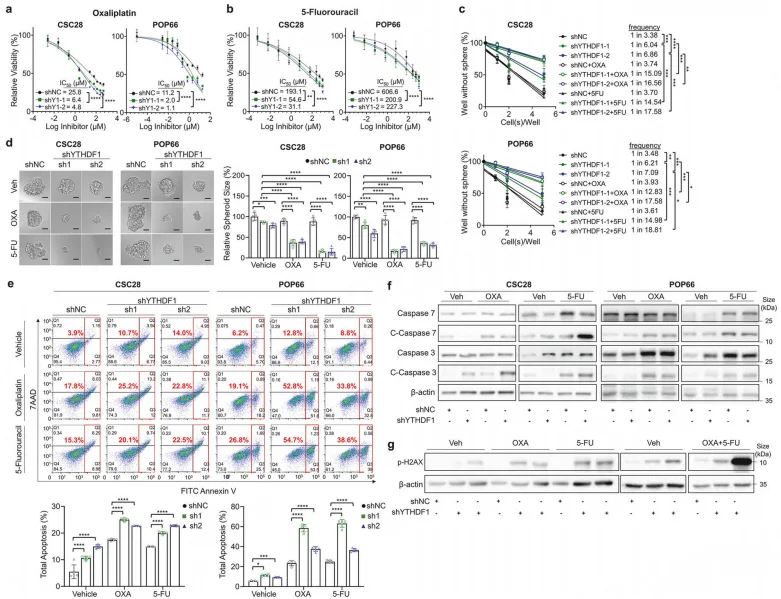
图6.YTHDF1敲低可克服结直肠癌的化疗耐药性
-
靶向 YTHDF1 增强化疗疗效
在异种移植模型中, VNP-siYTHDF1 单独治疗 可抑制肿瘤生长(P<0.05),与 OXA/5-FU 联用后肿瘤抑制效果显著增强(P<0.01),且无明显肝肾功能毒性。YTHDF1 抑制剂 SAC 可显著抑制 CSC 干性及类器官生长,与化疗联用后可协同增强凋亡诱导效应,下调 NOTCH1 表达。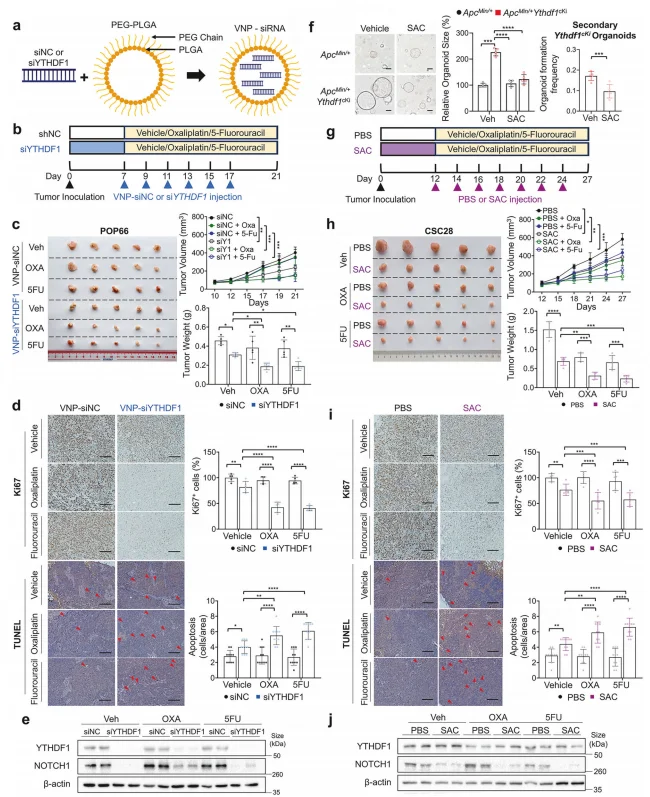
图7.通过VNP-siYTHDF1或丹酚酸C靶向YTHDF1可增强化疗疗效
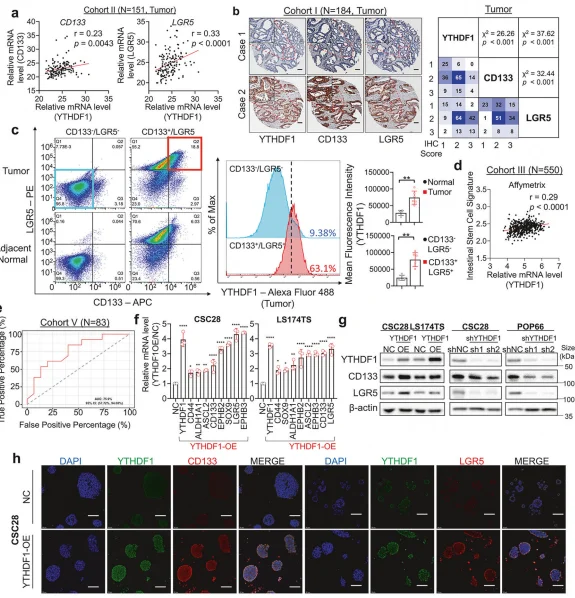
图8.YTHDF1在结直肠癌患者队列中与癌干细胞标志物呈正相关
研究意义与创新点
-
理论意义 首次在 Lgr5 特异性转基因小鼠模型中证实 YTHDF1 的 CSC 特异性调控作用,揭示了 “m⁶A-YTHDF1-NOTCH1” 轴在结直肠癌干细胞干性维持中的核心机制,丰富了 m⁶A 修饰在肿瘤干细胞调控中的理论体系。发现 YTHDF1 通过调控 NOTCH1 翻译影响 DNA 损伤修复,为结直肠癌化疗耐药的分子机制提供了全新解释。
-
临床意义 明确 YTHDF1 可作为结直肠癌化疗响应的潜在预测标志物,为临床化疗方案选择提供参考。提出靶向 YTHDF1 的联合治疗策略,VNP-siYTHDF1 纳米递送系统及天然抑制剂 SAC 的应用,为克服结直肠癌化疗耐药提供了安全有效的新型治疗方向,且 SAC 作为天然化合物具有良好的临床转化潜力。
-
技术创新 整合 MeRIP-seq、RNA-seq 及 Ribo-seq 多组学技术,精准鉴定 YTHDF1 的下游靶基因及调控模式。利用 Lgr5 特异性转基因模型,实现了在体内特异性调控 CSC 中 YTHDF1 的表达,避免了传统细胞系实验缺乏体内微环境的局限性。
文章小结
本研究通过多队列临床样本、特异性转基因小鼠模型、细胞及类器官实验,系统证实了 m⁶A 阅读器 YTHDF1 在结直肠癌干细胞干性维持与化疗耐药中的关键作用。其核心机制为 YTHDF1 通过 m⁶A 依赖方式结合 NOTCH1 mRNA 的 3'UTR 并促进其翻译,激活 NOTCH1 通路,进而增强干细胞自我更新能力并抑制化疗诱导的 DNA 损伤与凋亡。 靶向 YTHDF1 可有效逆转化疗耐药,与奥沙利铂、5 - 氟尿嘧啶联用可显著提升治疗效果。 该研究不仅揭示了结直肠癌化疗耐药的全新分子机制,还为开发精准靶向治疗策略提供了重要的理论依据与潜在药物靶点。
源井生物一直秉持 “让基因编辑更简单” 的核心理念,持续迭代产品与服务,已累计实现13000+基因编辑成功案例,拥有11000+细胞产品(含8000+KO细胞),自主研发的创新技术,基因编辑效率相比于传统方法提升10-20倍。目前源井生物已为超10000个生命科学实验室、药企和CRO公司提供优质的基因编辑服务与产品。
YTHDF1 是 m⁶A 修饰的关键 “阅读者”,可直接调控靶 mRNA 的翻译效率,许多研究证实 YTHDF1是人类癌症免疫治疗的有效治疗靶点。 如果您也想针对YTHDF1展开研究,源井生物可为您提供YTHDF1基因敲除细胞,涵盖Hela、HEK293等热门细胞系。如果您有个性化基因编辑的需要,欢迎咨询!
联系我们了解更多>>>参考文献
Cheung H, Chen H, Chen D, Zhou H, Liang C, Liu W, Cheung AH, Ding Y, Yuan K, Li X, Zhang Y, Wang S, Kang W, To KF, He H, Wong CC, Yu J. YTHDF1 targets the chemotherapy response by suppressing NOTCH1-induced stemness in colorectal cancer. Signal Transduct Target Ther. 2025 Dec 22;10(1):409. doi: 10.1038/s41392-025-02507-1. PMID: 41423446; PMCID: PMC12719390.










