【文献解读】无创检测ACE2表达——放射疗法124I-RBD探针大用处


【文献解读】无创检测ACE2表达——放射疗法124I-RBD探针大用处
背景
2019年底的全球冠状病毒疾病大流行(COVID-19)是由严重急性呼吸系统综合征冠状病毒2型(SARS-CoV-2)引发的。有研究表明,低剂量辐射可以减轻炎症并促进COVID-19的痊愈。血管紧张素转换酶2 (angiotensin-converting enzyme 2, ACE2)是羧肽酶ACE的同源物,是肾素-血管紧张素系统(renin-angiotensin system, RAS)的主要活性肽。SARS-CoV-2的刺突蛋白与人呼吸道上皮细胞的ACE2相互作用导致感染。与靶向病毒本身的抗体药物相比,靶向ACE2的抑制剂探针的开发在理论上更合理,在实践中也更具可能性。受体结合区域(RBD)是病毒和ACE2受体的中间体,因此有研究人员提出利用PET放射性核素修饰RBD可能对SARS-CoV-2的致命入侵具有一定的影响。
利用先进的PET技术监测被标记的RBD的代谢和残留,可以为SARS-CoV-2动物感染提供一个全面的视角。因此,来自北京市肿瘤发生与转化研究教育部重点实验室的Dan Li等研究人员在Acta Pharmacologica Sinica杂志上发表了一篇名为“SARS-CoV-2 receptor binding domain radio-probe: a non-invasive approach for angiotensin-converting enzyme 2 mapping in mic”的文章。他们构建了放射性碘化RBD作为分子靶向探针,在体内无创检测ACE2的表达,并研究抑制ACE2的放射疗法的途径。

124I-RBD抗体对ACE2具有较高的亲和力和选择性
用n -溴代丁二酰亚胺(NBS)介导的方法[124I]NaI标记RBD,纯化后得到比活性为28.9 GBq/nmol的124I-RBD。在盐水中5天放射化学纯度(RCP)在90%以上。通过SPR结合来研究RBD与人ACE2受体的结合能力。采用亲和模型来拟合数据,计算解离常数KD = 14.08 nM(图1)。采用ELISA法检测124I-RBD与人ACE2的结合效力,解离常数KD =75.7 nM(图2)。结果表明,RBD在体外与hACE2有较高的亲和力。
与未转导的HeLa细胞株相比,HeLaACE2+细胞株的ACE2基因表达率高561.2倍。Western blot检测结果显示,HeLaACE2+细胞确实有ACE2的高表达。细胞吸收放射性示踪剂的情况见图3。结果表明,2 h时HeLaACE2+细胞对124I-RBD的摄取值为(2.96±0.35)% ID/106个细胞(无阻塞)和(1.71±0.23)% ID/106个细胞(cold RBD) (P = 0.00038);HeLa细胞对124I-RBD的摄取值分别为(1.96±0.22)% ID/106(无阻塞)和(1.64±0.15)%ID/106 (cold RBD)(P>0.05)(图3)。
在该研究中,源井提供了ACE2过表达的HepG2ACE2+和HeLaACE2+细胞,用于在细胞水平上验证RBD与ACE2的亲和力。源井背靠数百种细胞培养经验,苛求每种细胞的最优MOI值,专家定制方案,以“单克隆”级别的标准构建过表达/干扰稳转株。点击了解更多服务详情>>
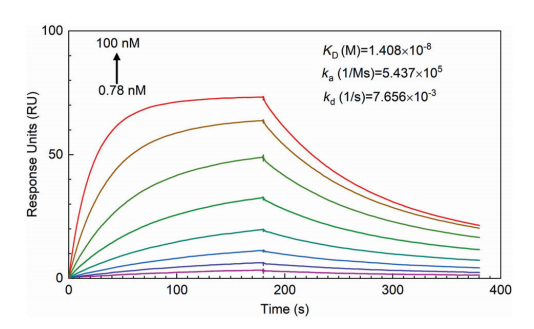
图1 固定化的ACE2作为受体,平衡时SPR 响应单位作为RBD浓度的函数
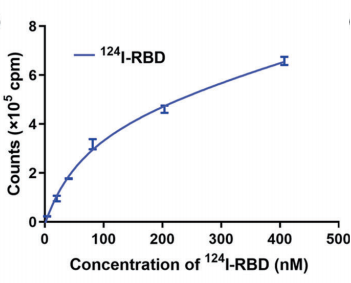
图2 124I-RBD与ACE2的结合亲和力测定
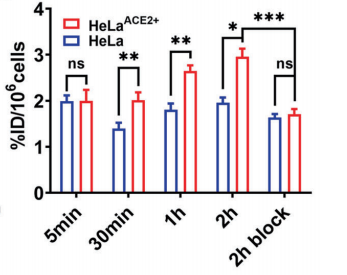
图3 HeLa 和 HeLa ACE2+细胞分别对124I-RBD的摄取,ns指统计学上没有显著差异 *P < 0.05, **P < 0.01, ***P < 0.001.
RBD与ACE2的特异性结合使124I-RBD在肺中滞留
为了研究RBD在肺内的滞留情况,他们采用肺内经支气管给药的方法,注射约50μL体积的0.927 MBq 124I-RBD。肺内的注射124I-RBD后,PET/CT成像显示出肺保持着至少4 h的较长的一段时间的高摄取并且在24 h内肺的SUVmean值依旧是高的。在0.5 h p.i.,肺内可观察到注射的[124I]NaI,但1 h后肺内SUVmean值降至极低水平,说明存在特异性相互作用(图4)。与裸鼠相比,经尾静脉注射124I-RBD后,携带HepG2肿瘤(HepG2ACE2+)的小鼠,肿瘤内摄取更高。在0.5h时,HepG2ACE2+肿瘤部位开始摄取124I-RBD,1h时浓度达到峰值,然后逐渐下降。4h时,肿瘤部位仍有高摄取(图5)。研究人员得出结论,124I-RBD在肺中的滞留是由RBD与ACE2的特异性结合引起的,这对人体的无创绘图是有用的。
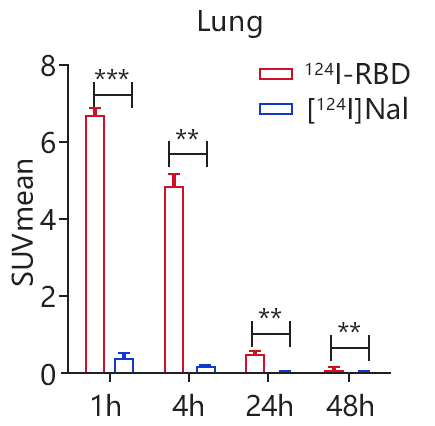
图4 肺内124I- RBD与对照[124I]NaI在不同时间点的SUV变化
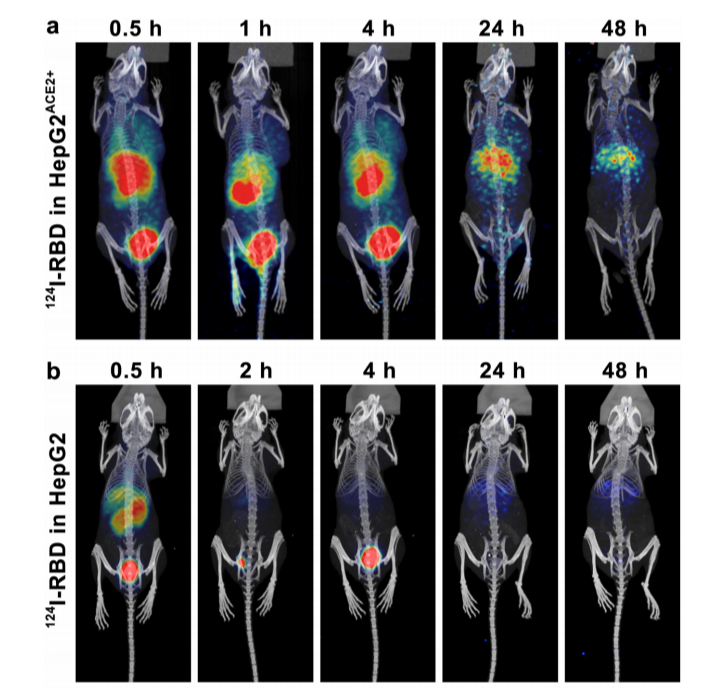
图5 肿瘤模型的Micro-PET成像
在该研究中,研究人员首次成功构建了124I-RBD作为新型的COVID-19分子靶向探针。通过放射性标记RBD探测ACE2的表达可用于无创的ACE2绘图。结合现有文献,提示碘同位素修饰RBD对人ACE2进行靶向监测是可行的,为放射治疗提供了临床前经验。
源井生物是一家专注于细胞基因编辑的企业,可在全球范围内提供优质的基因编辑细胞、稳转细胞株、病毒包装等相关服务,以及近2000种KO细胞现货库,基因敲除试剂盒等基因编辑相关产品,了解更多详情欢迎咨询我们!










