IF=32.4|源井STING1基因敲除细胞助力揭示多胺代谢调控cGAS活性的新机制


IF=32.4|源井STING1基因敲除细胞助力揭示多胺代谢调控cGAS活性的新机制

病毒性疾病,如新型冠状病毒肺炎、流感以及病毒性肝炎等,严重危害人类健康。病毒感染后未被及时清除,在细胞内持续存在,既会使宿主成为重要的传染源,又可诱导慢性进行性疾病甚至肿瘤的发生。
前言
病毒感染机体后,在宿主细胞内快速复制的同时,其产生的遗传物质(如DNA或RNA)会激活免疫系统。环状GMP-AMP(Cyclic GMP-AMP, cGAMP)合成酶(cGAMP synthase, cGAS)是重要的胞浆DNA识别受体,在抗感染及肿瘤免疫中均有重要作用[1,2]。双链DNA(double-stranded DNA, dsDNA)与cGAS结合后,催化GTP和ATP转化为第二信使cGAMP。cGAMP能够激活干扰素刺激基因(Stimulator of interferon genes, STING),进而通过募集TANK结合激酶1(TANK-binding kinase 1, TBK1)启动I型干扰素的表达和炎症反应。然而I型干扰素表达低下,病毒不能被有效清除;炎症反应过强,又会造成自身组织、器官的损伤。因此,深入研究cGAS活性调节机制对于预防和治疗病毒性疾病、避免机体过度活化至关重要。
摘要
近日,山东大学赵伟[3]教授课题组在Immunity杂志(IF=32.4)在线发表了题为“Polyamine metabolism controls B-to-Z DNA transition to orchestrate DNA sensor cGAS activity”的研究论文。该研究采用源井生物构建的敲除STING1基因的HeLa细胞系,发现了多胺代谢通过控制B-to-Z DNA构象转换调节cGAS活性的新机制,对深入认识cGAS活性调节及病毒性疾病的防治提供了理论依据。
研究方法及结果
为了研究细胞内环境对cGAS活性的影响,作者首先将干扰素刺激DNA(ISD)与不同代谢小分子孵育,过滤去除游离小分子后与小鼠腹腔巨噬细胞细胞裂解液反应,发现精胺及亚精胺能够显著抑制ISD诱导的cGAMP生成。在HeLa细胞中,精胺和亚精胺能够抑制HSV-1感染诱导的I型干扰素的表达,但在STING1-/-(编码STING的基因)细胞中则没有抑制作用。
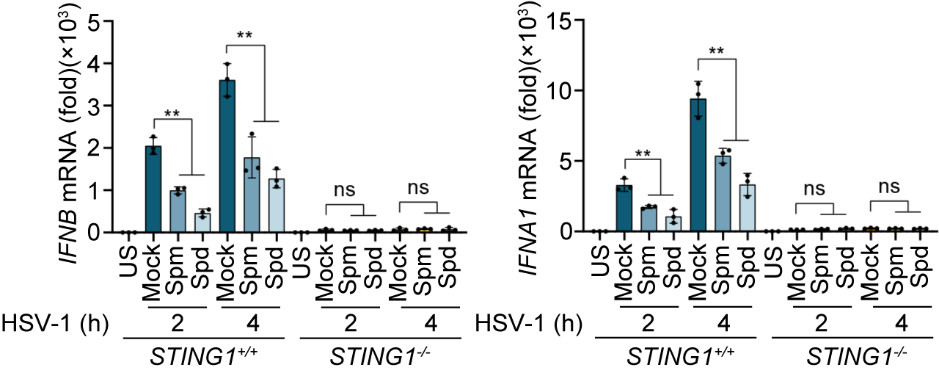
图1 精胺及亚精胺选择性抑制cGAS-STING信号通路
精胺和亚精胺能够抑制HSV-1感染诱导的干扰素刺激基因(ISGs)mRNA的表达,包括干扰素诱导的四肽重复蛋白1 (Ifit1)、Ifit2和Isg15,并促进HSV-1复制。
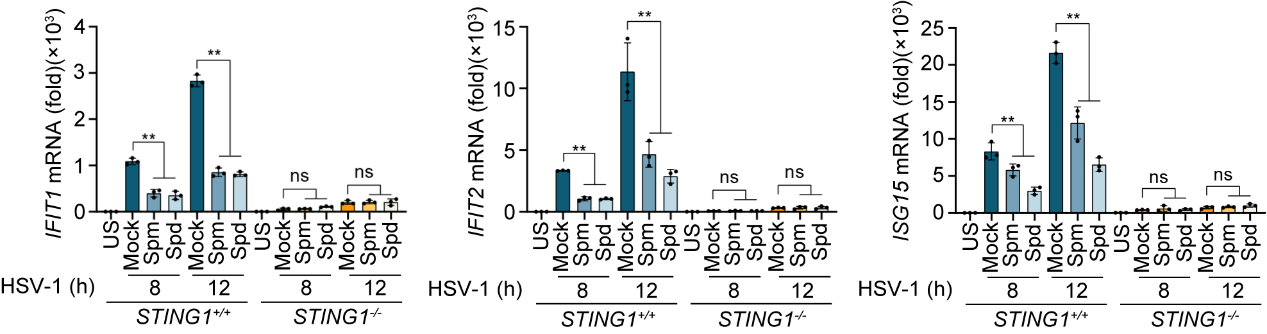
图2 精胺及亚精胺抑制HSV-1感染诱导的干扰素刺激基因(ISGs)的表达
随后作者通过免疫共沉淀及EMSA实验明确了精胺及亚精胺能够抑制ISD与cGAS结合。进一步通过免疫荧光、ChIP等实验发现精胺及亚精胺在细胞水平可以诱导Z-DNA生成;同时,ChIP、免疫共沉淀及竞争实验则表明Z-DNA与cGAS的亲和力远低于B-DNA,说明精胺及亚精胺在体内将DNA诱导成为亲和力更低的Z-DNA,从而避免cGAS的过度活化。
作者进一步探究精胺及亚精胺调节cGAS活性的生理相关性,发现精胺及亚精胺浓度在病毒感染后显著下降,且该过程是由亚精胺/亚精胺N1乙酰转移酶1(SAT1)所调节。SAT1是多胺分解代谢中的限速酶,在病毒感染后表达迅速上升。SAT1可降低细胞中亚精胺和亚精胺水平,通过抑制胞浆中Z-DNA的积累来增强cGAS活化水平,有效清除病毒。此外,补充精胺或亚精胺、敲除Sat1基因均导致小鼠抗HSV-1病毒能力下降。
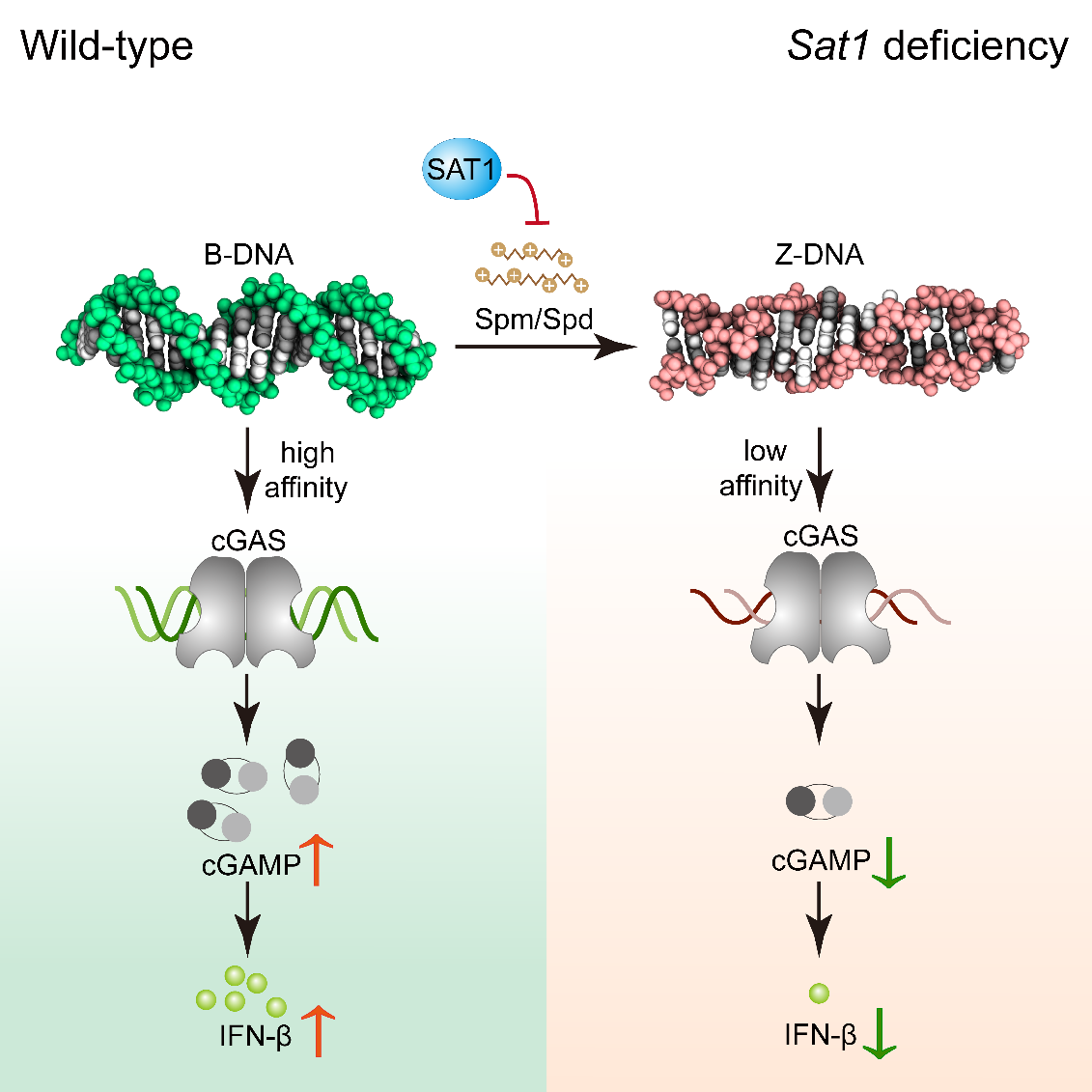
图3 多胺代谢通过控制Z-DNA形成调节cGAS活性模式图
结论
综上所述,该研究发现DNA的两种构象(B-DNA及Z-DNA)与cGAS亲和力不同;内源性代谢小分子精胺和亚精胺及多胺分解代谢关键酶SAT1通过诱导DNA构象转换调节cGAS活性;揭示了一种防止细胞DNA异常识别的新机制,并为治疗cGAS活性异常相关疾病提供了治疗靶点。
参考文献:
[1] Ablasser, A., and Chen, Z.J. (2019). cGAS in action: Expanding roles in immunity and inflammation. Science 363, eaat8657. 10.1126/science.aat8657.
[2] Motwani, M., Pesiridis, S., and Fitzgerald, K.A. (2019). DNA sensing by the cGAS-STING pathway in health and disease. Nat Rev Genet 20, 657-674. 10.1038/s41576-019-0151-1.
[3] Zhao, C., Ma, Y., Zhang, M., Gao, X., Liang, W., Qin, Y., ... & Zhao, W. (2023). Polyamine metabolism controls B-to-Z DNA transition to orchestrate DNA sensor cGAS activity. Immunity.











